EVOSEP ONE プロテオミクス用HPLC
EVOSEP ONEは臨床プロテオミクスを100倍強固に、10倍高速化キャリーオーバーのない多検体プロテオミクスを 不純物はEvotipに留まり、キャリーオーバーなしでSPEダイレクト注入 Evosep Oneは専用のステージチップ(Evotip)を使用します。Evotipはサンプルバイアルとトラップカラムの機能を併せ持った使い捨てのチップです。これにサンプルをロードして脱塩・洗浄後、Evosep…
 生命を脅かす病気との闘いにおける画期的プロジェクトが、英国で2019年9月11日に始動した。 2億ポンド(約264億円)の全ゲノム配列決定プロジェクトが形成され、英国ストックポートに本拠地を置くUK Biobankで約50万人のボランティアの遺伝子コードを調べ配列決定する。UK Biobankは製薬会社や専門機関とパートナーシップを形成している。英国のBoris Johnson 首相は次のように述べている。「英国には、国際的な協力と発見の中心に自らを置くという誇りのある歴史がある。 60年以上前、我々は国際的な研究者チームによってケンブリッジでDNAの発見に至ったが、今日はさらに進んでいる。 現在、我々は世界中の専門家を集めて、英国で世界最大の遺伝学研究プロジェクトに取り組み、生命にかかわる病気の治療を改善し、最終的には命を救おうとしている。 この種の突破には、英国で勉強や働くために世界中から集まる最も光り輝く最高の人材に開かれていなければ不可能だ。 だからこそ、留学生が潜在的な可能性を解き放ち、英国でのキャリアを開始するための新ルートを発表する。」ゲノミクス研究は、真に予測可能で、よりパーソナライズされたヘルスケアシステムを作成する可能性があり、英国はこの分野の研究が提供する機会を掴みたいと望んでいる。そのため、政府は2024年までに500万件のDNA分析を行うことを約束した。新しいプロジェクトは、遺伝子研究を通じて健康を改善し、癌、心臓病、糖尿病、関節炎、認知症を含む広範囲の重篤で生命を脅かす病気の予防、診断、治療を改善することを目指している。
生命を脅かす病気との闘いにおける画期的プロジェクトが、英国で2019年9月11日に始動した。 2億ポンド(約264億円)の全ゲノム配列決定プロジェクトが形成され、英国ストックポートに本拠地を置くUK Biobankで約50万人のボランティアの遺伝子コードを調べ配列決定する。UK Biobankは製薬会社や専門機関とパートナーシップを形成している。英国のBoris Johnson 首相は次のように述べている。「英国には、国際的な協力と発見の中心に自らを置くという誇りのある歴史がある。 60年以上前、我々は国際的な研究者チームによってケンブリッジでDNAの発見に至ったが、今日はさらに進んでいる。 現在、我々は世界中の専門家を集めて、英国で世界最大の遺伝学研究プロジェクトに取り組み、生命にかかわる病気の治療を改善し、最終的には命を救おうとしている。 この種の突破には、英国で勉強や働くために世界中から集まる最も光り輝く最高の人材に開かれていなければ不可能だ。 だからこそ、留学生が潜在的な可能性を解き放ち、英国でのキャリアを開始するための新ルートを発表する。」ゲノミクス研究は、真に予測可能で、よりパーソナライズされたヘルスケアシステムを作成する可能性があり、英国はこの分野の研究が提供する機会を掴みたいと望んでいる。そのため、政府は2024年までに500万件のDNA分析を行うことを約束した。新しいプロジェクトは、遺伝子研究を通じて健康を改善し、癌、心臓病、糖尿病、関節炎、認知症を含む広範囲の重篤で生命を脅かす病気の予防、診断、治療を改善することを目指している。
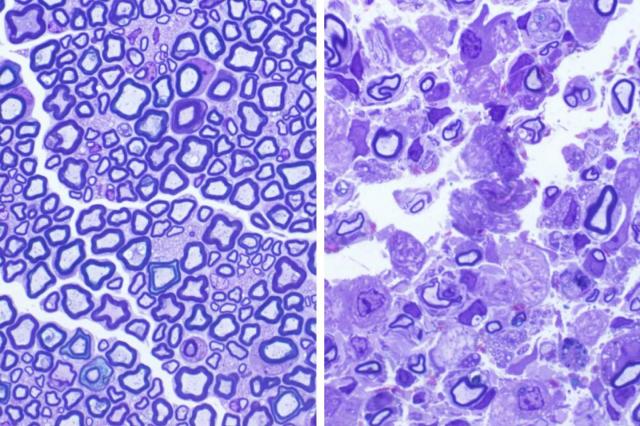 セントルイスのワシントン大学医学部の研究者らは、通常3歳前後で発作、発達退行、および死をもたらす小児の致命的な遺伝子障害「クラッベ病」に至る正確な生化学的パスウェイについて、数十年にわたる謎を解決したようだ。このクラッベ病のヒト疾患マウスモデルを用い、この研究者らは可能な治療戦略を見つけ出した。
セントルイスのワシントン大学医学部の研究者らは、通常3歳前後で発作、発達退行、および死をもたらす小児の致命的な遺伝子障害「クラッベ病」に至る正確な生化学的パスウェイについて、数十年にわたる謎を解決したようだ。このクラッベ病のヒト疾患マウスモデルを用い、この研究者らは可能な治療戦略を見つけ出した。
 新たな研究により、一般集団の左利きに関連するゲノム領域が初めて特定され、その影響が脳の構造と関連付けられた。 この研究は、これらの遺伝的違いを、言語に関連する脳の領域間のつながりと関連付けるものだ。遺伝子が利き手の決定に部分的な役割を担っていることはすでに知られていた。双子の研究では、利き手の変化の25%は遺伝子に起因すると推定されている。しかし、これらの遺伝子は一般集団では確立されていなかった。
新たな研究により、一般集団の左利きに関連するゲノム領域が初めて特定され、その影響が脳の構造と関連付けられた。 この研究は、これらの遺伝的違いを、言語に関連する脳の領域間のつながりと関連付けるものだ。遺伝子が利き手の決定に部分的な役割を担っていることはすでに知られていた。双子の研究では、利き手の変化の25%は遺伝子に起因すると推定されている。しかし、これらの遺伝子は一般集団では確立されていなかった。
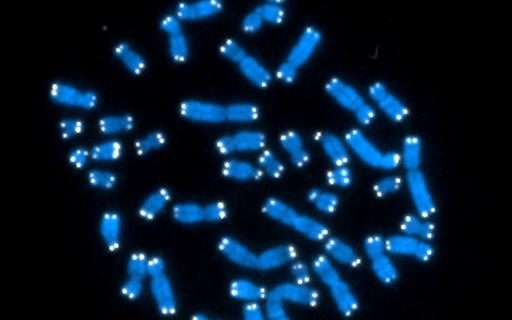 メリーランド大学(UMD)と国立衛生研究所の新しい研究により、酵素テロメラーゼの新しい役割が明らかになった。 これまで正常組織におけるテロメラーゼの唯一の既知の役割は、胚細胞、精子細胞、成体幹細胞、免疫細胞など、定期的に分裂する特定の細胞を保護することとされていた。 科学者は、無制限の細胞分裂を促進する癌性腫瘍を除き、他のすべての細胞ではテロメラーゼがオフになっていると考えていた。
メリーランド大学(UMD)と国立衛生研究所の新しい研究により、酵素テロメラーゼの新しい役割が明らかになった。 これまで正常組織におけるテロメラーゼの唯一の既知の役割は、胚細胞、精子細胞、成体幹細胞、免疫細胞など、定期的に分裂する特定の細胞を保護することとされていた。 科学者は、無制限の細胞分裂を促進する癌性腫瘍を除き、他のすべての細胞ではテロメラーゼがオフになっていると考えていた。
 最近オハイオ州立大学医学部に移ったKrystof Bankiewicz MD, PhD(写真)が率いる研究は、ニーマン・ピックA型疾患の遺伝子置換療法が非ヒト霊長類で安全に使用でき、マウスで治療効果があることを示している。これらの研究成果は、ジャーナルScience Translational Medicineで2019年8月21日にオンラインで公開された。 この論文は、「ニーマン・ピック病A型に対するアデノ随伴ウイルスベクター血清型9ベースの遺伝子治療(Adeno-Associated Viral Vector Serotype 9–Based Gene Therapy for Niemann-Pick Disease Type A.)」と題されている。
最近オハイオ州立大学医学部に移ったKrystof Bankiewicz MD, PhD(写真)が率いる研究は、ニーマン・ピックA型疾患の遺伝子置換療法が非ヒト霊長類で安全に使用でき、マウスで治療効果があることを示している。これらの研究成果は、ジャーナルScience Translational Medicineで2019年8月21日にオンラインで公開された。 この論文は、「ニーマン・ピック病A型に対するアデノ随伴ウイルスベクター血清型9ベースの遺伝子治療(Adeno-Associated Viral Vector Serotype 9–Based Gene Therapy for Niemann-Pick Disease Type A.)」と題されている。
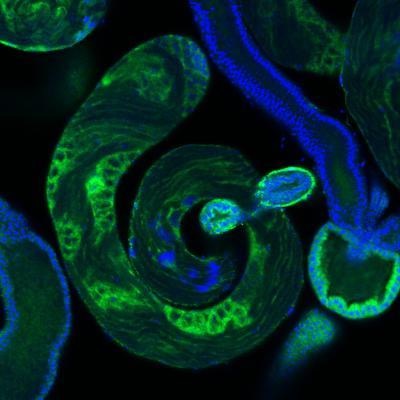 性別の戦いでは、遺伝的観点から、男性は革新的な側面を持っているように見える。精巣は精子の単なる工場以上のものであることが発見された。精巣は、種の進化の原料である新しい遺伝子の出現のホットスポットとしても機能している。ロックフェラー大学のチームは、ミバエを使用し、精子の発育中に自然のイノベーションの試みがどのように機能するかについて重要な洞察を得た。
性別の戦いでは、遺伝的観点から、男性は革新的な側面を持っているように見える。精巣は精子の単なる工場以上のものであることが発見された。精巣は、種の進化の原料である新しい遺伝子の出現のホットスポットとしても機能している。ロックフェラー大学のチームは、ミバエを使用し、精子の発育中に自然のイノベーションの試みがどのように機能するかについて重要な洞察を得た。
 オタゴ大学(ニュージーランド)の2人の科学者によるサルマラリア研究のブレークスルーが、再発型ヒトマラリアを診断・治療するのに役立つかもしれない。 マラリアは蚊を媒介とする感染症で、特にアジア、太平洋、南アメリカで毎年2億人以上の症例が発生しており、人間や他の動物にも影響を及ぼす。 症状には発熱、疲労感、嘔吐、頭痛などがあり、重度の場合、発作、昏睡、または死を引き起こす可能性がある。マラリアの再発は三日熱マラリア原虫によって引き起こされるが、最も広く分布しており、人間のマラリアの原因を治療するのは困難だ。三日熱マラリアに対する新しい薬とワクチンを開発するための現在の努力は、試験管(in vitro)培養法の欠如により妨げられてきた。しかし、世界初の発見で、Adelina Chua 博士と Jessica Ong 氏は、再発性三日熱マラリア原虫に密接に関連したサルマラリア寄生虫を培養するためのin vitro法を開発した。「我々は三日熱マラリアを培養することはできないが、今ではほぼ同一の姉妹種を培養することができ、新しい抗マラリア薬を開発し、迅速にテストする前例のない機会を得た。」とオタゴ大学微生物学部の博士候補者は説明した。この研究からの興味深いスピンオフは、人間の再発性マラリアに対して開発された薬物は、ニュージーランド本土の絶滅危惧種である黄色目ペンギン(画像)を殺す鳥マラリアに対しても作用する可能性が高いことだという。 「我々が開発する以前は、再発性マラリアを標的とした抗マラリア薬をスクリーニングするためのハイスループットモデルは無かった。」とOng 氏は述べた。 「我々のモデルは、医薬品開発だけでなく、ワクチンおよび診断研究でも重要な役割を果たすだろう。」2019年8月12日にNature Communicationsのオンラインで公開されたこの新しいマラリア培養法に関する論文は、「マラリア原虫カニクイザル赤血球期の堅牢な連続体外培養(Robust Continuous in Vitro Culture of the Plasmodium cynomolgi Erythrocytic Stages.)」と題されている。
オタゴ大学(ニュージーランド)の2人の科学者によるサルマラリア研究のブレークスルーが、再発型ヒトマラリアを診断・治療するのに役立つかもしれない。 マラリアは蚊を媒介とする感染症で、特にアジア、太平洋、南アメリカで毎年2億人以上の症例が発生しており、人間や他の動物にも影響を及ぼす。 症状には発熱、疲労感、嘔吐、頭痛などがあり、重度の場合、発作、昏睡、または死を引き起こす可能性がある。マラリアの再発は三日熱マラリア原虫によって引き起こされるが、最も広く分布しており、人間のマラリアの原因を治療するのは困難だ。三日熱マラリアに対する新しい薬とワクチンを開発するための現在の努力は、試験管(in vitro)培養法の欠如により妨げられてきた。しかし、世界初の発見で、Adelina Chua 博士と Jessica Ong 氏は、再発性三日熱マラリア原虫に密接に関連したサルマラリア寄生虫を培養するためのin vitro法を開発した。「我々は三日熱マラリアを培養することはできないが、今ではほぼ同一の姉妹種を培養することができ、新しい抗マラリア薬を開発し、迅速にテストする前例のない機会を得た。」とオタゴ大学微生物学部の博士候補者は説明した。この研究からの興味深いスピンオフは、人間の再発性マラリアに対して開発された薬物は、ニュージーランド本土の絶滅危惧種である黄色目ペンギン(画像)を殺す鳥マラリアに対しても作用する可能性が高いことだという。 「我々が開発する以前は、再発性マラリアを標的とした抗マラリア薬をスクリーニングするためのハイスループットモデルは無かった。」とOng 氏は述べた。 「我々のモデルは、医薬品開発だけでなく、ワクチンおよび診断研究でも重要な役割を果たすだろう。」2019年8月12日にNature Communicationsのオンラインで公開されたこの新しいマラリア培養法に関する論文は、「マラリア原虫カニクイザル赤血球期の堅牢な連続体外培養(Robust Continuous in Vitro Culture of the Plasmodium cynomolgi Erythrocytic Stages.)」と題されている。
 オーストラリアのガルバン医学研究所が率いる国際研究チームは、膵臓癌の主な死因である攻撃的な膵臓癌細胞がどのように環境を変化させ、体の他の部位への転移を行うのか明らかにした。研究者らは、一部の膵臓腫瘍は「perlecan」と呼ばれる分子をより多く生成し、周囲の環境を改造することを発見した。この分子により、癌細胞は体の他の部位に拡散しやすくなり、化学療法に耐性を示すという。マウスモデルにおいて、研究者らは、perlecanのレベルを下げることで膵臓癌の広がりを減らし、化学療法に対する反応を改善することを示した。 ガルバン医学研究所のInvasion and Metastasis Laboratory 所長のPaul Timpson 准教授、およびMatrix and Metastasis Group のリーダーであるThomas Cox 博士が率いたこの研究は、膵臓癌およびその他の癌を有する人のためのより効果的な治療選択肢へ希望をもたらすかもしれない。Nature Communicationsで2019年8月12日にオンラインで公開されたこの論文は、「膵臓癌細胞によって駆動されるCAF階層p53-Statusにより、perlecanを介し転移性および化学療法抵抗性の環境が作り出される(CAF Hierarchy Driven by Pancreatic Cancer Cell p53-Status Creates a Pro-Metastatic and Chemoresistant Environment via Perlecan.)」と題されている。「膵臓癌は非常に攻撃的であり、ほとんどの症例が診断されるまでに、腫瘍はしばしば手術不能となる」とTimpson 准教授は述べた。 「この研究で発見したことは、化学療法の効率を改善し、腫瘍の進行と広がりを軽減する可能性がある、膵臓癌を治療するための二面的なアプローチだ。」
オーストラリアのガルバン医学研究所が率いる国際研究チームは、膵臓癌の主な死因である攻撃的な膵臓癌細胞がどのように環境を変化させ、体の他の部位への転移を行うのか明らかにした。研究者らは、一部の膵臓腫瘍は「perlecan」と呼ばれる分子をより多く生成し、周囲の環境を改造することを発見した。この分子により、癌細胞は体の他の部位に拡散しやすくなり、化学療法に耐性を示すという。マウスモデルにおいて、研究者らは、perlecanのレベルを下げることで膵臓癌の広がりを減らし、化学療法に対する反応を改善することを示した。 ガルバン医学研究所のInvasion and Metastasis Laboratory 所長のPaul Timpson 准教授、およびMatrix and Metastasis Group のリーダーであるThomas Cox 博士が率いたこの研究は、膵臓癌およびその他の癌を有する人のためのより効果的な治療選択肢へ希望をもたらすかもしれない。Nature Communicationsで2019年8月12日にオンラインで公開されたこの論文は、「膵臓癌細胞によって駆動されるCAF階層p53-Statusにより、perlecanを介し転移性および化学療法抵抗性の環境が作り出される(CAF Hierarchy Driven by Pancreatic Cancer Cell p53-Status Creates a Pro-Metastatic and Chemoresistant Environment via Perlecan.)」と題されている。「膵臓癌は非常に攻撃的であり、ほとんどの症例が診断されるまでに、腫瘍はしばしば手術不能となる」とTimpson 准教授は述べた。 「この研究で発見したことは、化学療法の効率を改善し、腫瘍の進行と広がりを軽減する可能性がある、膵臓癌を治療するための二面的なアプローチだ。」
 膵臓癌は、治療選択肢が限られている最も致命的な癌の1つだ。 通常、進行期まで症状がなく、多くの抗がん療法に抵抗する能力があるため、特に予後不良である。 その発達に関与する遺伝子を特定することで、より早期の診断と改善された治療が可能になると考えられる。現在、マサチューセッツ総合病院(MGH)、ブリガムアンドウィメンズ病院、およびダナファーバーがん研究所の研究者が率いる研究チームは、特定の遺伝子の突然変異が、研究対象のある家族の膵臓癌の遺伝型と関連していることを発見した。 膵臓癌の約10%は遺伝性であると考えられている(後述するJimmy Carter 前大統領の家族の膵臓癌の議論を参照)。研究グループはまた、彼らが特定したような突然変異が腫瘍の発生に寄与するメカニズムを明らかにした。 2019年8月12日にNature Geneticsでオンライン公開されたこの研究では、複数のメンバーが膵臓癌にかかっている家族のゲノム配列を決定した。 解析により、RAS癌遺伝子ファミリー様3(RABL3)遺伝子の変異が明らかになった。 この論文は「RABL3の突然変異はKRASのプレニル化を変化させ、遺伝性膵臓癌に関連する。(Mutations in RABL3 Alter KRAS Prenylation and Are Associated with Hereditary Pancreatic Cancer.)」と題されている。この遺伝子突然変異の影響を評価するために、研究者らはゼブラフィッシュでそれを再現した。ゼブラフィッシュは、癌リスクに対する新たに発見された遺伝子突然変異の影響を研究するための大集団モデルである。 突然変異を持っている魚は、加速された頻度で癌を発症した。 追加の研究により、RABL3によって発現されるタンパク質はRASシグナル伝達経路の構成要素と相互作用することが明らかになり、これは様々な形態の癌および他の状態に関係している。 異常なRASパスウェイシグナル伝達はほとんどの膵臓癌で見られるため、RABL3がRASパスウェイにどのように影響するかを研究することで、標的療法の新しい戦略を提供できるという。「この仕事は、患者の話とその家族の歴史から始め、遺伝的手法を使用して遺伝子突然変異を特定し、ゼブラフィッシュ・モデルで最終的に確認した代表例だ。」とMGHの消化器内科のチーフである上級著者のWolfram Goessling医師は述べた。
膵臓癌は、治療選択肢が限られている最も致命的な癌の1つだ。 通常、進行期まで症状がなく、多くの抗がん療法に抵抗する能力があるため、特に予後不良である。 その発達に関与する遺伝子を特定することで、より早期の診断と改善された治療が可能になると考えられる。現在、マサチューセッツ総合病院(MGH)、ブリガムアンドウィメンズ病院、およびダナファーバーがん研究所の研究者が率いる研究チームは、特定の遺伝子の突然変異が、研究対象のある家族の膵臓癌の遺伝型と関連していることを発見した。 膵臓癌の約10%は遺伝性であると考えられている(後述するJimmy Carter 前大統領の家族の膵臓癌の議論を参照)。研究グループはまた、彼らが特定したような突然変異が腫瘍の発生に寄与するメカニズムを明らかにした。 2019年8月12日にNature Geneticsでオンライン公開されたこの研究では、複数のメンバーが膵臓癌にかかっている家族のゲノム配列を決定した。 解析により、RAS癌遺伝子ファミリー様3(RABL3)遺伝子の変異が明らかになった。 この論文は「RABL3の突然変異はKRASのプレニル化を変化させ、遺伝性膵臓癌に関連する。(Mutations in RABL3 Alter KRAS Prenylation and Are Associated with Hereditary Pancreatic Cancer.)」と題されている。この遺伝子突然変異の影響を評価するために、研究者らはゼブラフィッシュでそれを再現した。ゼブラフィッシュは、癌リスクに対する新たに発見された遺伝子突然変異の影響を研究するための大集団モデルである。 突然変異を持っている魚は、加速された頻度で癌を発症した。 追加の研究により、RABL3によって発現されるタンパク質はRASシグナル伝達経路の構成要素と相互作用することが明らかになり、これは様々な形態の癌および他の状態に関係している。 異常なRASパスウェイシグナル伝達はほとんどの膵臓癌で見られるため、RABL3がRASパスウェイにどのように影響するかを研究することで、標的療法の新しい戦略を提供できるという。「この仕事は、患者の話とその家族の歴史から始め、遺伝的手法を使用して遺伝子突然変異を特定し、ゼブラフィッシュ・モデルで最終的に確認した代表例だ。」とMGHの消化器内科のチーフである上級著者のWolfram Goessling医師は述べた。
 ワシントン大学医学部の科学者が率いる国際的な研究者チームは、遅発性および早発性双方のアルツハイマー病リスクに影響を及ぼす遺伝子ペアを特定した。 これまでアルツハイマー病に関与していたほとんどの遺伝子は、メッセージを伝達するニューロンに影響を及ぼし、脳の異なる領域が互いに通信できるようにするものだった。 しかし、新たに特定された遺伝子は、まったく異なる細胞集団、つまり脳の免疫細胞に影響を及ぼす。
ワシントン大学医学部の科学者が率いる国際的な研究者チームは、遅発性および早発性双方のアルツハイマー病リスクに影響を及ぼす遺伝子ペアを特定した。 これまでアルツハイマー病に関与していたほとんどの遺伝子は、メッセージを伝達するニューロンに影響を及ぼし、脳の異なる領域が互いに通信できるようにするものだった。 しかし、新たに特定された遺伝子は、まったく異なる細胞集団、つまり脳の免疫細胞に影響を及ぼす。
 ノースカロライナ(NC)州立大学の研究者らは、弾性ポリマーが広域スペクトルの抗菌特性を有し、メチシリン耐性黄色ブドウ球菌(MRSA)を含むさまざまなウイルスや薬剤耐性菌を数分で殺すことができることを発見した。「このポリマーのいくつかの興味深い挙動を観察し、我々は抗菌材料を作製するためにその可能性をより深く調べることを決めた。 このポリマーは、病院や診療所などの臨床環境や、病原体の伝播が悲惨な結果をもたらす可能性がある高齢者向け施設で特に有用だ。」 ノースカロライナ州立大学の化学および生体分子工学の著名な教授であり、この研究に関する論文の共著者であるRich Spontak博士は語った。このポリマーの抗菌特性は、スルホン酸基で化学修飾(または機能化)された一連の繰り返しユニットに水を引き付ける独自の分子構造に由来する。 「バクテリアがポリマーと接触すると、バクテリアの表面の水がポリマーのスルホン酸官能基と相互作用し、バクテリアを素早く殺す酸性溶液を生成する」と、論文の共著者で准教授であるReza Ghiladi博士は述べた。 「これらの酸性溶液は、ポリマー中のスルホン酸官能基の数を制御することにより、調整することができる。」この研究は、2019年7月17日にMaterials Horizonのオンラインで公開された。 このオープンアクセスの論文は、「薬剤耐性バクテリアを数分で殺す本質的に自己殺菌性の帯電マルチブロックポリマー(Inherently Self-Sterilizing Charged Multiblock Polymers That Kill Drug-Resistant Microbes in Minutes.)」と題されている。
ノースカロライナ(NC)州立大学の研究者らは、弾性ポリマーが広域スペクトルの抗菌特性を有し、メチシリン耐性黄色ブドウ球菌(MRSA)を含むさまざまなウイルスや薬剤耐性菌を数分で殺すことができることを発見した。「このポリマーのいくつかの興味深い挙動を観察し、我々は抗菌材料を作製するためにその可能性をより深く調べることを決めた。 このポリマーは、病院や診療所などの臨床環境や、病原体の伝播が悲惨な結果をもたらす可能性がある高齢者向け施設で特に有用だ。」 ノースカロライナ州立大学の化学および生体分子工学の著名な教授であり、この研究に関する論文の共著者であるRich Spontak博士は語った。このポリマーの抗菌特性は、スルホン酸基で化学修飾(または機能化)された一連の繰り返しユニットに水を引き付ける独自の分子構造に由来する。 「バクテリアがポリマーと接触すると、バクテリアの表面の水がポリマーのスルホン酸官能基と相互作用し、バクテリアを素早く殺す酸性溶液を生成する」と、論文の共著者で准教授であるReza Ghiladi博士は述べた。 「これらの酸性溶液は、ポリマー中のスルホン酸官能基の数を制御することにより、調整することができる。」この研究は、2019年7月17日にMaterials Horizonのオンラインで公開された。 このオープンアクセスの論文は、「薬剤耐性バクテリアを数分で殺す本質的に自己殺菌性の帯電マルチブロックポリマー(Inherently Self-Sterilizing Charged Multiblock Polymers That Kill Drug-Resistant Microbes in Minutes.)」と題されている。
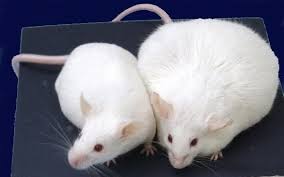 ユニバーシティ・オブ・ユタ・ヘルスの研究者は、マウスが肥満になるのを防ぐ腸の特定のクラスの細菌を特定し、同じ微生物が同様に人の体重を制御する可能性があることを示唆した。クロストリジウムと呼ばれるこの有益なバクテリアは、腸に生息する何兆ものバクテリアや他の微生物の総称であるマイクロバイオームの一部である。Scienceの2019年7月26日号で発表されたこの研究では、健康なマウスには20から30のバクテリアのクラスであるクロストリジウムが豊富にあることを示しているが、免疫系が損なわれたマウスは加齢とともに腸からこれらの微生物を失うという。健康的な食事を与えられたとしても、免疫系が損なわれたマウスは必然的に肥満になるが、この種の微生物を戻すことでマウスはスリムになった。この論文のタイトルは「T細胞が媒介する微生物叢の調節が肥満を防ぐ(T Cell-Mediated Regulation of the Microbiota Protects Against Obesity.)」と題されている。ユニバーシティ・オブ・ユタ・ヘルスの病理学の准教授であるJune Round博士は、研究助教授W. Zac Stephens博士および、当時大学院生だったCharisse Petersen博士と共に研究を率いた。「この痩身効果の原因となる最低限の細菌が見つかった。この生物が何をしていて、治療に価値があるかどうかを理解できる可能性がある」とRound博士は言う。この研究結果はすでに進むべき方向を指し示している。
ユニバーシティ・オブ・ユタ・ヘルスの研究者は、マウスが肥満になるのを防ぐ腸の特定のクラスの細菌を特定し、同じ微生物が同様に人の体重を制御する可能性があることを示唆した。クロストリジウムと呼ばれるこの有益なバクテリアは、腸に生息する何兆ものバクテリアや他の微生物の総称であるマイクロバイオームの一部である。Scienceの2019年7月26日号で発表されたこの研究では、健康なマウスには20から30のバクテリアのクラスであるクロストリジウムが豊富にあることを示しているが、免疫系が損なわれたマウスは加齢とともに腸からこれらの微生物を失うという。健康的な食事を与えられたとしても、免疫系が損なわれたマウスは必然的に肥満になるが、この種の微生物を戻すことでマウスはスリムになった。この論文のタイトルは「T細胞が媒介する微生物叢の調節が肥満を防ぐ(T Cell-Mediated Regulation of the Microbiota Protects Against Obesity.)」と題されている。ユニバーシティ・オブ・ユタ・ヘルスの病理学の准教授であるJune Round博士は、研究助教授W. Zac Stephens博士および、当時大学院生だったCharisse Petersen博士と共に研究を率いた。「この痩身効果の原因となる最低限の細菌が見つかった。この生物が何をしていて、治療に価値があるかどうかを理解できる可能性がある」とRound博士は言う。この研究結果はすでに進むべき方向を指し示している。
 CRISPRを基盤としたツールは、疾患関連遺伝子変異を標的にする能力に革命をもたらした。 CRISPRテクノロジーは、Cas9およびCas12酵素でDNAをターゲットにすることや、Cas13酵素でRNAをターゲットにすることなど、遺伝子とその発現を操作するツールファミリーとして成長している。 このラインナップは、突然変異に取り組むためのさまざまな戦略を提供する。
CRISPRを基盤としたツールは、疾患関連遺伝子変異を標的にする能力に革命をもたらした。 CRISPRテクノロジーは、Cas9およびCas12酵素でDNAをターゲットにすることや、Cas13酵素でRNAをターゲットにすることなど、遺伝子とその発現を操作するツールファミリーとして成長している。 このラインナップは、突然変異に取り組むためのさまざまな戦略を提供する。
 南カリフォルニア大学にあるUSC Viterbi School of Engineeringの新研究は、老化プロセスがどのように機能するか理解するための鍵となるかもしれない。 研究結果は高齢の人の健康を大幅に改善することができるより良い癌治療と革命的な新薬への道を開くポテンシャルを秘めている。化学工学および材料科学の助教授であるNick Graham博士のチーム、生物科学と生物医学工学の教授であるScott Fraser博士、そしてZohrab A. Kaprielianの工学博士であるPin Wang博士は、2019年5月28日にJournal of Biological Chemistryに「ヌクレオチド合成の阻害はヒト乳腺上皮細胞の複製老化を促進する(Inhibition of Nucleotide Synthesis Promotes Replicative Senescence of Human Mammary Epithelial Cells.)」と題された論文を発表した。
南カリフォルニア大学にあるUSC Viterbi School of Engineeringの新研究は、老化プロセスがどのように機能するか理解するための鍵となるかもしれない。 研究結果は高齢の人の健康を大幅に改善することができるより良い癌治療と革命的な新薬への道を開くポテンシャルを秘めている。化学工学および材料科学の助教授であるNick Graham博士のチーム、生物科学と生物医学工学の教授であるScott Fraser博士、そしてZohrab A. Kaprielianの工学博士であるPin Wang博士は、2019年5月28日にJournal of Biological Chemistryに「ヌクレオチド合成の阻害はヒト乳腺上皮細胞の複製老化を促進する(Inhibition of Nucleotide Synthesis Promotes Replicative Senescence of Human Mammary Epithelial Cells.)」と題された論文を発表した。
 コリアンダー(パクチー)を含むハーブは、民間療法の抗けいれん薬として長い歴史がある。 今までハーブがどのように働いたか根本的なメカニズムの多くは未知のままだった。 新しい研究でカリフォルニア大学アーバインスクールオブメディカル校の研究者らは、コリアンダーが癲癇や他の病気によく見られる特定の発作を効果的に遅らせることを可能にする分子作用を明らかにした。2019年7月16日にThe FASEB Journalにオンラインで発表されたこの研究は、非常に強力なKCNQチャンネル活性化剤としてのコリアンダー(Coriandrum sativum)の分子作用を説明している。 この論文は「コリアンダーリーフは強力なカリウムチャンネル活性化抗けいれん薬である(Cilantro Leaf Harbors A Potent Potassium Channel–Activating Anticonvulsant.)」と題されている。カリフォルニア大学アーバインスクールオブメディカル校の生理学生物生物学博士でこの調査の主任研究員であるGeoff Abbott博士は、次のように述べている。 「具体的には、ドデセナールと呼ばれるコリアンダーの1つの成分がカリウムチャネルの特定の部分に結合してそれらを開き、細胞の興奮性を低下させることが解った。この発見は、抗けいれん薬としてのコリアンダーのより効果的な使用、またはより安全でより有効な抗けいれん薬を開発するためのドデセナールの改良につながる可能性があり重要だ。」
コリアンダー(パクチー)を含むハーブは、民間療法の抗けいれん薬として長い歴史がある。 今までハーブがどのように働いたか根本的なメカニズムの多くは未知のままだった。 新しい研究でカリフォルニア大学アーバインスクールオブメディカル校の研究者らは、コリアンダーが癲癇や他の病気によく見られる特定の発作を効果的に遅らせることを可能にする分子作用を明らかにした。2019年7月16日にThe FASEB Journalにオンラインで発表されたこの研究は、非常に強力なKCNQチャンネル活性化剤としてのコリアンダー(Coriandrum sativum)の分子作用を説明している。 この論文は「コリアンダーリーフは強力なカリウムチャンネル活性化抗けいれん薬である(Cilantro Leaf Harbors A Potent Potassium Channel–Activating Anticonvulsant.)」と題されている。カリフォルニア大学アーバインスクールオブメディカル校の生理学生物生物学博士でこの調査の主任研究員であるGeoff Abbott博士は、次のように述べている。 「具体的には、ドデセナールと呼ばれるコリアンダーの1つの成分がカリウムチャネルの特定の部分に結合してそれらを開き、細胞の興奮性を低下させることが解った。この発見は、抗けいれん薬としてのコリアンダーのより効果的な使用、またはより安全でより有効な抗けいれん薬を開発するためのドデセナールの改良につながる可能性があり重要だ。」
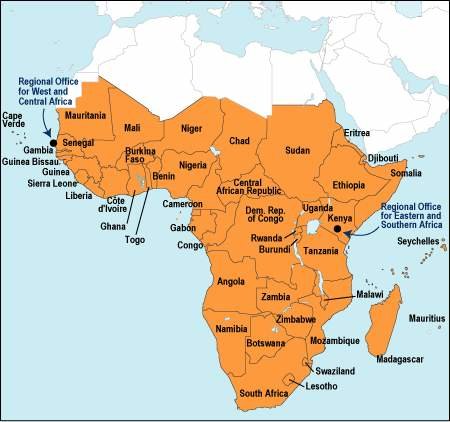 NIHの研究者らは、サハラ以南のアフリカ人における2型糖尿病の過去最大のゲノム研究を報告した。この研究は、ナイジェリア、ガーナ、およびケニアからの5,000人以上の個人データに基づく。 研究者らは、既知のゲノム変異体を確認し、サハラ以南のアフリカの集団における疾患感受性に影響を与える可能性がある新規遺伝子ZRANB3を同定した。 この遺伝子は他の集団における2型糖尿病の発症にも影響を及ぼし、さらなる研究成果が期待される。ネイチャーコミュニケーションズに2019年7月19日オンラインで発表されたこの研究では、研究者は、アフリカ大陸で行われた単一で最大の糖尿病ゲノム協会研究であるアフリカアメリカ糖尿病研究を通して参加者に利用できるゲノムデータを分析した。 5,231人から入手可能な情報を使用して、研究者は多くのゲノム変異体が2型糖尿病と有意に関連していることを発見した。このオープンアクセスの論文は、「ZRANB3は、ベータ細胞量とインスリン反応に関連するアフリカ特有の2型糖尿病遺伝子座(ZRANB3 Is an African-Specific Type 2 Diabetes Locus Associated with Beta-Cell Mass and Insulin Response.)」と題されている。この調査結果は、他の研究がほとんどヨーロッパの祖先集団の2型糖尿病にすでに関与しているという多くのバリアントの結果を再現している。 この研究は、国立ヒトゲノム研究所(NHGRI)、国立糖尿病消化器病研究所、および国立衛生研究所の資金によって実施された。この論文の共著者であり、NHGRI Medical Genomics and Metabolic Genetics Branchの上席研究員であるFrancis S. Collins博士は、次のように述べている。
NIHの研究者らは、サハラ以南のアフリカ人における2型糖尿病の過去最大のゲノム研究を報告した。この研究は、ナイジェリア、ガーナ、およびケニアからの5,000人以上の個人データに基づく。 研究者らは、既知のゲノム変異体を確認し、サハラ以南のアフリカの集団における疾患感受性に影響を与える可能性がある新規遺伝子ZRANB3を同定した。 この遺伝子は他の集団における2型糖尿病の発症にも影響を及ぼし、さらなる研究成果が期待される。ネイチャーコミュニケーションズに2019年7月19日オンラインで発表されたこの研究では、研究者は、アフリカ大陸で行われた単一で最大の糖尿病ゲノム協会研究であるアフリカアメリカ糖尿病研究を通して参加者に利用できるゲノムデータを分析した。 5,231人から入手可能な情報を使用して、研究者は多くのゲノム変異体が2型糖尿病と有意に関連していることを発見した。このオープンアクセスの論文は、「ZRANB3は、ベータ細胞量とインスリン反応に関連するアフリカ特有の2型糖尿病遺伝子座(ZRANB3 Is an African-Specific Type 2 Diabetes Locus Associated with Beta-Cell Mass and Insulin Response.)」と題されている。この調査結果は、他の研究がほとんどヨーロッパの祖先集団の2型糖尿病にすでに関与しているという多くのバリアントの結果を再現している。 この研究は、国立ヒトゲノム研究所(NHGRI)、国立糖尿病消化器病研究所、および国立衛生研究所の資金によって実施された。この論文の共著者であり、NHGRI Medical Genomics and Metabolic Genetics Branchの上席研究員であるFrancis S. Collins博士は、次のように述べている。
 世界で初めて、科学者たちは幹細胞を心臓組織に向かわせる新しい方法を発見した。 英国のブリストル大学の研究者によって先導され、最近発表されたこの研究結果は、英国で全死亡の4分の1以上を引き起こす心血管疾患の治療の根本的な改善につながるという。この英国王立化学協会のオープンアクセスジャーナルに掲載された論文は「幹細胞を心筋に向ける改変人工膜結合タンパク質(Designer Artificial Membrane Binding Proteins to Direct Stem Cells to the Myocardium.)」と題されている。今日まで、患者またはドナーから採取して増殖し、患者の損傷した心臓組織を再生するために注入した幹細胞が有望な結果を生み出している。 しかし、これらの次世代細胞療法は実用化されつつあるが、幹細胞の分布に関連する重大な課題が残っている。循環細胞が接触する様々な組織シンクと心臓内の高い血流の組み合わせは、幹細胞の大部分が肺と脾臓に行き着くことを意味している。現在、ブリストル大学の細胞分子医学部の研究者らは、幹細胞が心臓組織の「ホーム」になるように、幹細胞を特殊なタンパク質で修飾することによってこれを克服する方法を見つけた。研究の筆頭著者であるAdam Perriman博士は、UKRI未来リーダーズフェローで細胞治療技術会社CytoSeek( https://www.cytoseek.uk/ )の創設者であり、次のように説明している。
世界で初めて、科学者たちは幹細胞を心臓組織に向かわせる新しい方法を発見した。 英国のブリストル大学の研究者によって先導され、最近発表されたこの研究結果は、英国で全死亡の4分の1以上を引き起こす心血管疾患の治療の根本的な改善につながるという。この英国王立化学協会のオープンアクセスジャーナルに掲載された論文は「幹細胞を心筋に向ける改変人工膜結合タンパク質(Designer Artificial Membrane Binding Proteins to Direct Stem Cells to the Myocardium.)」と題されている。今日まで、患者またはドナーから採取して増殖し、患者の損傷した心臓組織を再生するために注入した幹細胞が有望な結果を生み出している。 しかし、これらの次世代細胞療法は実用化されつつあるが、幹細胞の分布に関連する重大な課題が残っている。循環細胞が接触する様々な組織シンクと心臓内の高い血流の組み合わせは、幹細胞の大部分が肺と脾臓に行き着くことを意味している。現在、ブリストル大学の細胞分子医学部の研究者らは、幹細胞が心臓組織の「ホーム」になるように、幹細胞を特殊なタンパク質で修飾することによってこれを克服する方法を見つけた。研究の筆頭著者であるAdam Perriman博士は、UKRI未来リーダーズフェローで細胞治療技術会社CytoSeek( https://www.cytoseek.uk/ )の創設者であり、次のように説明している。
 たった2つの水素原子の位置をずらすだけの小さな化学変化が健康なマウスとインスリン抵抗性および脂肪肝を持つマウスとの違いを引き起こし、糖尿病と心臓病の主な危険因子になることを突き止めた。この変化を加えることで、高脂肪食を与えられたマウスにおけるこれらの症状の発症を防ぎ、肥満マウスにおける前糖尿病を逆転させた。 科学者たちは、dihydroceramide desaturase 1(DES1)と呼ばれる酵素を失活させることで代謝性疾患の流れを変えた。酵素がセラミドと呼ばれる脂肪脂質から水素を除去するのを止めれば、体内のセラミドの総量を減らす効果がある。
たった2つの水素原子の位置をずらすだけの小さな化学変化が健康なマウスとインスリン抵抗性および脂肪肝を持つマウスとの違いを引き起こし、糖尿病と心臓病の主な危険因子になることを突き止めた。この変化を加えることで、高脂肪食を与えられたマウスにおけるこれらの症状の発症を防ぎ、肥満マウスにおける前糖尿病を逆転させた。 科学者たちは、dihydroceramide desaturase 1(DES1)と呼ばれる酵素を失活させることで代謝性疾患の流れを変えた。酵素がセラミドと呼ばれる脂肪脂質から水素を除去するのを止めれば、体内のセラミドの総量を減らす効果がある。
 鎌状赤血球症(Sickle cell disease:SCD)は、両方の親がヘモグロビン遺伝子の突然変異の保因者である場合に遺伝する貧血の一種だ。 現在、この疾患は、侵襲的検査を実施しなければ妊娠中に診断することができないが、流産リスクを伴うので、両親によって診断を拒否されることがある。現在、英国のバーミンガムにあるNonacus Ltd.と協力して、英国のロンドンにあるGuy's and St Thomas' NHS Foundation Trust and Viapath Analyticsの研究者らは、この疾患の非侵襲的出生前診断を開発した。 この発表は、2019年6月16日に欧州人類遺伝学会(ESHG)の年次総会で行われた。この発表は、「無細胞DNAの次世代シークエンシングによる鎌状赤血球症の非侵襲的出生前診断(Non-Invasive Prenatal Diagnosis of Sickle Cell Disease by Next-Generation Sequencing of Cell-Free DNA.)」と題されている。Guy's and St Thomasの研究員であるJulia van Campen博士は、次のように説明している。「無細胞胎児DNA(母体血流中を循環する胎児由来のDNA)を使用して鎌状赤血球症の検査方法を開発した。 無細胞胎児DNA検査はすでにいくつかの疾患で利用可能だが、英国で最も一般的に要求されている出生前検査の1つであるにもかかわらず、技術的困難により鎌状赤血球症の検査法の開発が妨げられている。」鎌状赤血球症の赤ちゃんを産むリスクがあるカップルでは、各パートナーがヘモグロビン遺伝子の変異を保有している。つまり、どの胎児でも四分の1の確率で両方の変異を受け継ぐため、鎌状赤血球症の影響を受ける。 このように受け継がれた状態の非侵襲的出生前診断(Non-invasive prenatal diagnosis :NIPD)は困難だ。「鎌状赤血球症のための非侵襲的出生前アッセイの開発は以前から試みられているが、現在まで成功していない。」とvan Campen博士は言う。 研究者らは24人の妊娠中の鎌状赤血球症キャリアのサンプルを分析した。
鎌状赤血球症(Sickle cell disease:SCD)は、両方の親がヘモグロビン遺伝子の突然変異の保因者である場合に遺伝する貧血の一種だ。 現在、この疾患は、侵襲的検査を実施しなければ妊娠中に診断することができないが、流産リスクを伴うので、両親によって診断を拒否されることがある。現在、英国のバーミンガムにあるNonacus Ltd.と協力して、英国のロンドンにあるGuy's and St Thomas' NHS Foundation Trust and Viapath Analyticsの研究者らは、この疾患の非侵襲的出生前診断を開発した。 この発表は、2019年6月16日に欧州人類遺伝学会(ESHG)の年次総会で行われた。この発表は、「無細胞DNAの次世代シークエンシングによる鎌状赤血球症の非侵襲的出生前診断(Non-Invasive Prenatal Diagnosis of Sickle Cell Disease by Next-Generation Sequencing of Cell-Free DNA.)」と題されている。Guy's and St Thomasの研究員であるJulia van Campen博士は、次のように説明している。「無細胞胎児DNA(母体血流中を循環する胎児由来のDNA)を使用して鎌状赤血球症の検査方法を開発した。 無細胞胎児DNA検査はすでにいくつかの疾患で利用可能だが、英国で最も一般的に要求されている出生前検査の1つであるにもかかわらず、技術的困難により鎌状赤血球症の検査法の開発が妨げられている。」鎌状赤血球症の赤ちゃんを産むリスクがあるカップルでは、各パートナーがヘモグロビン遺伝子の変異を保有している。つまり、どの胎児でも四分の1の確率で両方の変異を受け継ぐため、鎌状赤血球症の影響を受ける。 このように受け継がれた状態の非侵襲的出生前診断(Non-invasive prenatal diagnosis :NIPD)は困難だ。「鎌状赤血球症のための非侵襲的出生前アッセイの開発は以前から試みられているが、現在まで成功していない。」とvan Campen博士は言う。 研究者らは24人の妊娠中の鎌状赤血球症キャリアのサンプルを分析した。
 世界中で感染症を減らす上で最も成功した介入の1つであるワクチン接種だが、新生児を保護する上では依然として有効性が限られている。 マサチューセッツ総合病院(MGH)、MITおよびハーバード大学によるラゴン研究所の研究は、妊娠中のワクチン誘発免疫がどのようにして胎児に移るのかを決定した。これはより効果的な母体ワクチンの開発に影響を与えるだろう。Cellの6月27日号に掲載されたこの論文のタイトルは「Fcグリカンによる胎盤抗体導入の媒介調節(Fc Glycan-Mediated Regulation of Placental Antibody Transfer)」と題されている。「新生児は、子供自身の成長と同じく、自ら有益・有害な微生物の両方に対処することを学ぶ必要がある真新しい免疫システムと一緒にこの世界に到着する。」と、Cell論文の共著者でラゴン研究所およびマサチューセッツ総合病院(MGH)医学部のGalit Alter博士(写真)は語った。「新生児の免疫システムが敵と味方を区別することを学ぶのを助けるために、母親は胎盤を介して抗体を胎児に移す。胎盤がこの絶対的に不可欠な機能を果たす規則は知られていなかったが、これが解明されれば新生児を保護するためのより強力なワクチンとなるだろう。」はしかなど一部の病気に対する母親の抗体は母親から乳児に移すことができ、子供が個々のワクチン接種に十分な年齢になるまである程度の保護を提供するが、ポリオのような他の深刻な病気に対する抗体はあまり効率的に移転されない。抗体が母親から子供へと伝達されるメカニズムを調査するために、Alter博士と彼女のチーム(前MGH産科婦人科、現在はWeill Cornell Medicineの産婦人科長である共著者のLaura Riley医師を含む)はシステム血清学と呼ばれる新しいツールを使用して、母親の血液サンプルと、乳児への胎盤への血液、栄養素、および免疫因子を含む臍帯から百日咳に対する抗体の品質を比較した。
世界中で感染症を減らす上で最も成功した介入の1つであるワクチン接種だが、新生児を保護する上では依然として有効性が限られている。 マサチューセッツ総合病院(MGH)、MITおよびハーバード大学によるラゴン研究所の研究は、妊娠中のワクチン誘発免疫がどのようにして胎児に移るのかを決定した。これはより効果的な母体ワクチンの開発に影響を与えるだろう。Cellの6月27日号に掲載されたこの論文のタイトルは「Fcグリカンによる胎盤抗体導入の媒介調節(Fc Glycan-Mediated Regulation of Placental Antibody Transfer)」と題されている。「新生児は、子供自身の成長と同じく、自ら有益・有害な微生物の両方に対処することを学ぶ必要がある真新しい免疫システムと一緒にこの世界に到着する。」と、Cell論文の共著者でラゴン研究所およびマサチューセッツ総合病院(MGH)医学部のGalit Alter博士(写真)は語った。「新生児の免疫システムが敵と味方を区別することを学ぶのを助けるために、母親は胎盤を介して抗体を胎児に移す。胎盤がこの絶対的に不可欠な機能を果たす規則は知られていなかったが、これが解明されれば新生児を保護するためのより強力なワクチンとなるだろう。」はしかなど一部の病気に対する母親の抗体は母親から乳児に移すことができ、子供が個々のワクチン接種に十分な年齢になるまである程度の保護を提供するが、ポリオのような他の深刻な病気に対する抗体はあまり効率的に移転されない。抗体が母親から子供へと伝達されるメカニズムを調査するために、Alter博士と彼女のチーム(前MGH産科婦人科、現在はWeill Cornell Medicineの産婦人科長である共著者のLaura Riley医師を含む)はシステム血清学と呼ばれる新しいツールを使用して、母親の血液サンプルと、乳児への胎盤への血液、栄養素、および免疫因子を含む臍帯から百日咳に対する抗体の品質を比較した。
 アメリカがん協会の予測が正確であれば、今年は、乳癌、脳腫瘍、卵巣癌、または前立腺癌よりも、膵臓癌でより多くの人々が死亡するだろう。 膵臓癌が非常に致命的である1つの理由は、伝統的な化学療法に対する耐性である。しかし、ウェストバージニア大学医学部の外科腫瘍専門医Brian Boone医師は、FOLFIRINOX(フォルフィリノックス:癌治療薬の新しい組み合わせ)により膵臓癌が安全に除去するには血管に近すぎる「切除可能なボーダーライン」にある患者のアウトカムを改善できるかどうかを調査している。
アメリカがん協会の予測が正確であれば、今年は、乳癌、脳腫瘍、卵巣癌、または前立腺癌よりも、膵臓癌でより多くの人々が死亡するだろう。 膵臓癌が非常に致命的である1つの理由は、伝統的な化学療法に対する耐性である。しかし、ウェストバージニア大学医学部の外科腫瘍専門医Brian Boone医師は、FOLFIRINOX(フォルフィリノックス:癌治療薬の新しい組み合わせ)により膵臓癌が安全に除去するには血管に近すぎる「切除可能なボーダーライン」にある患者のアウトカムを改善できるかどうかを調査している。
 英国の研究チームは動脈硬化の背後にあるメカニズムを動物実験で確認し、通常ニキビの治療に使用される一般的な薬が動脈硬化の効果的な治療法になり得ることを示した。ケンブリッジ大学とキングスカレッジロンドン校が率いるチームは、かつてDNAを修復する目的で細胞内にのみ存在すると考えられていた分子も、認知症・心臓病・高血圧に関連する動脈硬化の原因であることを見出した。骨のようなカルシウム沈着物の蓄積、動脈の硬化および臓器および組織への血流の制限によって引き起こされる動脈硬化に対する治療法は現在ない。ブリティッシュハート財団からの助成金により、研究者はPoly(ADP-Ribose)または通常DNA修復と関連する分子のPARも動脈の石灰化を推進することを発見した。さらに、慢性腎臓病のラットを使い、ニキビの治療によく使われる抗生物質であるミノサイクリンが、循環系のカルシウムの蓄積を防ぐことにより動脈硬化を治療できることを発見した。この研究は、10年以上の基礎研究の成果であり、2019年6月11日にCell Reportsにオンラインで掲載された。 このオープンアクセスの論文は「Poly(ADP-Ribose)はDNA損傷応答とバイオミネラリゼーションに関連する“Poly(ADP-Ribose) Links the DNA Damage Response and Biomineralization.”」と題されている。「動脈硬化は、年齢が上がるにつれて誰にでも起こり、透析中の患者では加速され、子供でさえ石灰化動脈は発達する。しかし、今までのところ、このプロセスを制御するもの、つまり治療法は知られていない。」 ケンブリッジ大学化学部のMelinda Duer博士は、キングスカレッジロンドン校のCathy Shanahan博士と長期共同研究の一環としてこの研究を推進した。
英国の研究チームは動脈硬化の背後にあるメカニズムを動物実験で確認し、通常ニキビの治療に使用される一般的な薬が動脈硬化の効果的な治療法になり得ることを示した。ケンブリッジ大学とキングスカレッジロンドン校が率いるチームは、かつてDNAを修復する目的で細胞内にのみ存在すると考えられていた分子も、認知症・心臓病・高血圧に関連する動脈硬化の原因であることを見出した。骨のようなカルシウム沈着物の蓄積、動脈の硬化および臓器および組織への血流の制限によって引き起こされる動脈硬化に対する治療法は現在ない。ブリティッシュハート財団からの助成金により、研究者はPoly(ADP-Ribose)または通常DNA修復と関連する分子のPARも動脈の石灰化を推進することを発見した。さらに、慢性腎臓病のラットを使い、ニキビの治療によく使われる抗生物質であるミノサイクリンが、循環系のカルシウムの蓄積を防ぐことにより動脈硬化を治療できることを発見した。この研究は、10年以上の基礎研究の成果であり、2019年6月11日にCell Reportsにオンラインで掲載された。 このオープンアクセスの論文は「Poly(ADP-Ribose)はDNA損傷応答とバイオミネラリゼーションに関連する“Poly(ADP-Ribose) Links the DNA Damage Response and Biomineralization.”」と題されている。「動脈硬化は、年齢が上がるにつれて誰にでも起こり、透析中の患者では加速され、子供でさえ石灰化動脈は発達する。しかし、今までのところ、このプロセスを制御するもの、つまり治療法は知られていない。」 ケンブリッジ大学化学部のMelinda Duer博士は、キングスカレッジロンドン校のCathy Shanahan博士と長期共同研究の一環としてこの研究を推進した。
 メキシコ東部原産のサソリの毒液は、単なる毒素以上のものかもしれない。 スタンフォード大学とメキシコ国立大学の研究者らは、この毒には細菌感染と戦うのを助ける2色に変わる化合物も含まれていることを発見した。 チームはサソリの毒から化合物を分離するだけでなく、それらを実験室で合成し、実験室で作られた毒が組織サンプルとマウスでブドウ球菌と薬剤耐性結核菌を殺すことを確認した。
メキシコ東部原産のサソリの毒液は、単なる毒素以上のものかもしれない。 スタンフォード大学とメキシコ国立大学の研究者らは、この毒には細菌感染と戦うのを助ける2色に変わる化合物も含まれていることを発見した。 チームはサソリの毒から化合物を分離するだけでなく、それらを実験室で合成し、実験室で作られた毒が組織サンプルとマウスでブドウ球菌と薬剤耐性結核菌を殺すことを確認した。
 ビル&メリンダ・ゲイツ財団が資金提供しているGlobal Dietary Databaseプロジェクトの一環として行われた新研究による予備的な発見は、不十分な果物と野菜の消費量が、毎年何百万もの心臓病と脳卒中による死因となっていることを明らかにした。 この研究では、7人に1人の心血管死が十分な果物を食べていないことに起因し、12人に1人の心血管死が十分な野菜を食べていないことに起因すると推定された。
ビル&メリンダ・ゲイツ財団が資金提供しているGlobal Dietary Databaseプロジェクトの一環として行われた新研究による予備的な発見は、不十分な果物と野菜の消費量が、毎年何百万もの心臓病と脳卒中による死因となっていることを明らかにした。 この研究では、7人に1人の心血管死が十分な果物を食べていないことに起因し、12人に1人の心血管死が十分な野菜を食べていないことに起因すると推定された。
 2019年5月31日号のScience誌における新しい報告によると、非常に長命としてよく知られている哺乳類である南アフリカに生息するほくろラット種の類縁が、わさびの有効成分であるイソチオシアン酸アリル(AITC)への暴露により疼痛への免疫が起こる初めてのエビデンスが発見された。これらのげっ歯類がどのようにしてこの特定の種類の疼痛に鈍感になるように進化したのかを理解することは、ヒトの疼痛を解決するための新たな方向を指し示す可能性があるとこの研究者は言う。
2019年5月31日号のScience誌における新しい報告によると、非常に長命としてよく知られている哺乳類である南アフリカに生息するほくろラット種の類縁が、わさびの有効成分であるイソチオシアン酸アリル(AITC)への暴露により疼痛への免疫が起こる初めてのエビデンスが発見された。これらのげっ歯類がどのようにしてこの特定の種類の疼痛に鈍感になるように進化したのかを理解することは、ヒトの疼痛を解決するための新たな方向を指し示す可能性があるとこの研究者は言う。
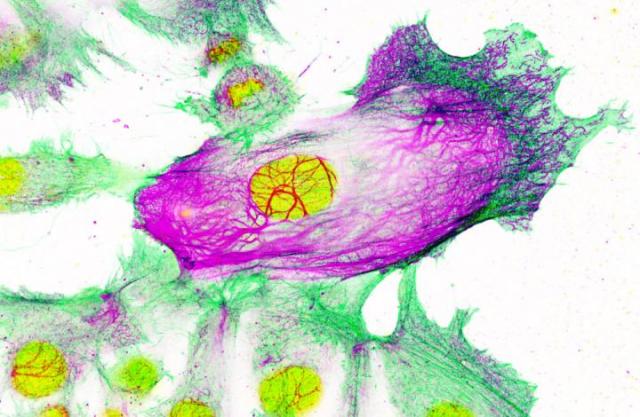 LondonのImperial CollegeおよびInstitute of Cancer Researchの科学者が率いる初期段階の研究で、乳がん細胞における遺伝的「スイッチ」が一種の内部足場の形成を促進することが確認された。この足場は、髪を強く保つのを助けるケラチンタンパク質に関連するケラチン80と呼ばれるタンパク質でできている。この足場の量を増やすと、がん細胞がより硬くなる。研究者らによれば、細胞が凝集して血流に乗って体の他の部分に移動するのを助けるかもしれない。研究者らは、アロマターゼ阻害剤と呼ばれる一般的な乳がん薬で治療されたヒト乳がん細胞を研究した。研究チームは、同じスイッチが乳がん細胞の薬剤抵抗性に関与していることを発見した(つまり、がんが回復すれば薬はもはや有効ではない)。このスイッチを別の薬物で標的にすると、この耐性を逆転させることができ、癌が拡大する可能性が低くなる可能性があるとImperial Collegeの外科の研究を率いるLuca Magnani博士は説明している。アロマターゼ阻害剤は癌細胞を殺すのに効果的だが、術後10年以内に約30%の患者が再発。さらに悪いことに、癌が再発したとき、それは通常体の周りに拡がって、治療が困難である。」この新しい研究の結果は、2019年5月9日にNature Communicationsにオンラインで発表された。 オープンアクセスの論文は、「SREBP1は内分泌抵抗性ERα乳癌におけるケラチン80依存性細胞骨格変化および侵襲的行動を促進する(SREBP1 Drives Keratin-80-Dependent Cytoskeletal Changes and Invasive Behavior in Endocrine-Resistant ERα Breast Cancer.)」と題されている。Magnani博士は、「これまでのところ理由は分からなかったが、我々の初期段階の研究では、転写因子と呼ばれる一種の遺伝子スイッチが癌細胞を増殖させるだけでなく、この遺伝子スイッチを標的とすることは癌細胞が薬物に対して抵抗性になるのを防ぎ、他の体の部分に広がるのを防ぐことができる。」
LondonのImperial CollegeおよびInstitute of Cancer Researchの科学者が率いる初期段階の研究で、乳がん細胞における遺伝的「スイッチ」が一種の内部足場の形成を促進することが確認された。この足場は、髪を強く保つのを助けるケラチンタンパク質に関連するケラチン80と呼ばれるタンパク質でできている。この足場の量を増やすと、がん細胞がより硬くなる。研究者らによれば、細胞が凝集して血流に乗って体の他の部分に移動するのを助けるかもしれない。研究者らは、アロマターゼ阻害剤と呼ばれる一般的な乳がん薬で治療されたヒト乳がん細胞を研究した。研究チームは、同じスイッチが乳がん細胞の薬剤抵抗性に関与していることを発見した(つまり、がんが回復すれば薬はもはや有効ではない)。このスイッチを別の薬物で標的にすると、この耐性を逆転させることができ、癌が拡大する可能性が低くなる可能性があるとImperial Collegeの外科の研究を率いるLuca Magnani博士は説明している。アロマターゼ阻害剤は癌細胞を殺すのに効果的だが、術後10年以内に約30%の患者が再発。さらに悪いことに、癌が再発したとき、それは通常体の周りに拡がって、治療が困難である。」この新しい研究の結果は、2019年5月9日にNature Communicationsにオンラインで発表された。 オープンアクセスの論文は、「SREBP1は内分泌抵抗性ERα乳癌におけるケラチン80依存性細胞骨格変化および侵襲的行動を促進する(SREBP1 Drives Keratin-80-Dependent Cytoskeletal Changes and Invasive Behavior in Endocrine-Resistant ERα Breast Cancer.)」と題されている。Magnani博士は、「これまでのところ理由は分からなかったが、我々の初期段階の研究では、転写因子と呼ばれる一種の遺伝子スイッチが癌細胞を増殖させるだけでなく、この遺伝子スイッチを標的とすることは癌細胞が薬物に対して抵抗性になるのを防ぎ、他の体の部分に広がるのを防ぐことができる。」
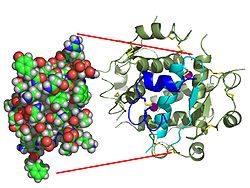 医学界のネッシー探しに例えられるかもしれない発見が、ジョンズホプキンス医学、IBM Research、および他の4つの共同研究機関からなる研究チームによって行われた。1型糖尿病の発症に重要な役割を果たす可能性がある疑わしい「X細胞」として、「悪役ハイブリッド」免疫系細胞についての存在が初めて報告された。Cellの2019年5月30日号の特集として発表された新しい論文の中で、異常なリンパ球(一種の白血球) - 正式には二重発現細胞(DE)細胞として知られている - を報告している。
医学界のネッシー探しに例えられるかもしれない発見が、ジョンズホプキンス医学、IBM Research、および他の4つの共同研究機関からなる研究チームによって行われた。1型糖尿病の発症に重要な役割を果たす可能性がある疑わしい「X細胞」として、「悪役ハイブリッド」免疫系細胞についての存在が初めて報告された。Cellの2019年5月30日号の特集として発表された新しい論文の中で、異常なリンパ球(一種の白血球) - 正式には二重発現細胞(DE)細胞として知られている - を報告している。
 自閉症の人はしばしば腸の問題に苦しんでいるが、誰もその理由が分からなかった。 オーストラリア・メルボルンのRMIT大学の研究者らは、脳と腸の両方に見られる同じ遺伝子変異が原因であることを突き止めた。この発見は自閉症における腸 - 脳神経系のつながりを確認し、腸を標的とすることによって自閉症に関連する行動の問題を緩和することができる潜在的な治療法の探求における新たな方向性を開くものだ。2019年5月22日にAutism Researchにオンラインで論文が掲載されたこの論文は「Neuroligin‐3の自閉症関連r451c変異を発現する患者およびマウスの胃腸機能障害(Gastrointestinal Dysfunction in Patients and Mice Expressing the Autism‐Associated r451c Mutation in Neuroligin‐3.)」と題されており、イェーテボリ大学とルンド大学(スウェーデン)、ベイラー医科大学(アメリカ)、ミンホー大学(ポルトガル)、ラ・トローブ大学、メルボルン大学、フロリー神経科学研究所、モナシュ大学との共同研究によるものである。RMIT大学のElisa Hill-Yardin准教授(写真)は、「自閉症を理解しようとする科学者たちはずっと脳を見てきたので、腸神経系との関連は最近探究され始めたばかりだ」と述べた。「我々は脳と腸が同じニューロンを多数共有していることに気づいており、今回初めて、それらが自閉症関連の遺伝子突然変異も共有していることを確認した。」とHill-Yardin博士は述べた。 「自閉症患者の最大90%が腸の問題に苦しんでおり、それが彼らとその家族の日常生活に重大な影響を及ぼす可能性がある。」我々の調査結果は、これらの胃腸の問題は 自閉症の行動問題。 臨床医、家族、研究者にとって、それはまったく新しい考え方であり、自閉症の人々の生活の質を向上させるための治療法の探索視野を広げるものだ。」
自閉症の人はしばしば腸の問題に苦しんでいるが、誰もその理由が分からなかった。 オーストラリア・メルボルンのRMIT大学の研究者らは、脳と腸の両方に見られる同じ遺伝子変異が原因であることを突き止めた。この発見は自閉症における腸 - 脳神経系のつながりを確認し、腸を標的とすることによって自閉症に関連する行動の問題を緩和することができる潜在的な治療法の探求における新たな方向性を開くものだ。2019年5月22日にAutism Researchにオンラインで論文が掲載されたこの論文は「Neuroligin‐3の自閉症関連r451c変異を発現する患者およびマウスの胃腸機能障害(Gastrointestinal Dysfunction in Patients and Mice Expressing the Autism‐Associated r451c Mutation in Neuroligin‐3.)」と題されており、イェーテボリ大学とルンド大学(スウェーデン)、ベイラー医科大学(アメリカ)、ミンホー大学(ポルトガル)、ラ・トローブ大学、メルボルン大学、フロリー神経科学研究所、モナシュ大学との共同研究によるものである。RMIT大学のElisa Hill-Yardin准教授(写真)は、「自閉症を理解しようとする科学者たちはずっと脳を見てきたので、腸神経系との関連は最近探究され始めたばかりだ」と述べた。「我々は脳と腸が同じニューロンを多数共有していることに気づいており、今回初めて、それらが自閉症関連の遺伝子突然変異も共有していることを確認した。」とHill-Yardin博士は述べた。 「自閉症患者の最大90%が腸の問題に苦しんでおり、それが彼らとその家族の日常生活に重大な影響を及ぼす可能性がある。」我々の調査結果は、これらの胃腸の問題は 自閉症の行動問題。 臨床医、家族、研究者にとって、それはまったく新しい考え方であり、自閉症の人々の生活の質を向上させるための治療法の探索視野を広げるものだ。」
 英国サリー大学、米国インディアナ大学医学部ユージーンおよびマリリングリックアイ研究所そしてロンドン大学の科学者らによる研究によると、天然物から失明のいくつかの原因を治療するための画期的な答えを得ることができたという。 科学者らは、増殖性糖尿病性網膜症などの退行性眼疾患の原因を治療するために有用である可能性が高い植物群から化合物を発見し、試験を実施した。 目の中の新しい血管細胞の異常な成長は、未熟児(未熟児網膜症)、糖尿病患者(増殖性糖尿病性網膜症)、および高齢者(湿性加齢黄斑変性症)を含む多くのタイプの失明に関連している。論文の中で、サリー大学の科学者は、アメリカのインディアナ大学とロンドンのキングストン大学の専門家と共に、ヒヤシンス科植物で発見されたホモイソフラボノイドおよびそれらの合成誘導体について試験を行った。2019年4月5日にアメリカ化学会のJournal of Natural Productsにオンラインで発表されたこの論文は、「ヒヤシンス科由来の天然および合成ホモイソフラボノイドの抗血管新生活性(sensu APGII)(The Antiangiogenic Activity of Naturally Occurring and Synthetic Homoisoflavonoids from the Hyacinthaceae (sensu APGII))」と題されている。
英国サリー大学、米国インディアナ大学医学部ユージーンおよびマリリングリックアイ研究所そしてロンドン大学の科学者らによる研究によると、天然物から失明のいくつかの原因を治療するための画期的な答えを得ることができたという。 科学者らは、増殖性糖尿病性網膜症などの退行性眼疾患の原因を治療するために有用である可能性が高い植物群から化合物を発見し、試験を実施した。 目の中の新しい血管細胞の異常な成長は、未熟児(未熟児網膜症)、糖尿病患者(増殖性糖尿病性網膜症)、および高齢者(湿性加齢黄斑変性症)を含む多くのタイプの失明に関連している。論文の中で、サリー大学の科学者は、アメリカのインディアナ大学とロンドンのキングストン大学の専門家と共に、ヒヤシンス科植物で発見されたホモイソフラボノイドおよびそれらの合成誘導体について試験を行った。2019年4月5日にアメリカ化学会のJournal of Natural Productsにオンラインで発表されたこの論文は、「ヒヤシンス科由来の天然および合成ホモイソフラボノイドの抗血管新生活性(sensu APGII)(The Antiangiogenic Activity of Naturally Occurring and Synthetic Homoisoflavonoids from the Hyacinthaceae (sensu APGII))」と題されている。
 子宮頸部の前癌を治療するための新しい免疫療法により、臨床試験に参加した3分の1の女性が病変とHPV感染の両方を完全に排除することに成功した。この注射(治療用ワクチン)には、子宮頸部上皮内腫瘍(CIN: cervical intraepithelial neoplasia)として知られるほぼすべての子宮頸癌前駆体の原因となるハイリスクのヒトパピローマウイルス(HPV: human papilloma virus)を攻撃する免疫系反応を引き起こす3種類のタンパク質遺伝子が含まれている。「HPVに感染している女性を治療するための製品は殆ど無い。比較的簡単で成功率がこのようなものを見たのは今回が初めてで、非常にエキサイティングだ。」とミシガン大学医学部の家族医学および産科婦人科教授のDiane Harper博士(写真)は述べた。頸部前癌病変は3段階の重症度に分類される。CIN 2病変はしばしば自然に消失するが、CIN 3病変に進行することもある。 CIN 3が最も重症で、成長が非常に遅い疾患だが、30年以内にCIN 3病変の半分以下が癌になることがある。「しかし、CIN 3のどの女性ががんになるのか、どの女性ががんにならないのかを判断する方法は無い。したがって、CIN 2または3の女性はすべてがんになる可能性があるものとして扱う」とHarper博士は語った。この研究では、CIN2またはCIN3と診断された192人の女性が登録し、129人がワクチン接種を受け、63人がプラセボ投与を受けた。 大腿部に3回、1週間に1回、3週間、女性に注射を3回行った。 6ヵ月後、女性はCIN 2/3のための標準的な外科的処置で治療され、切除された組織を検査した。ワクチン接種を受けた女性は、HPV感染症の種類に関わらず、プラセボグループの女性の2倍以上のCIN消失を確認した。 結果はより重症のCIN3で最も顕著であった:ワクチンを投与された人の36%でCIN3が排除されたのに対し、プラセボグループの女性ではCIN3の排除は見られなかった。手術後もう2年半の間参加者を追跡した長期の追跡調査では、プラセボよりワクチン接種を受けた人々のほうが優れていることを示し、ワクチン群のより多くの女性がHPVを完全に排除したままであった。この研究は、2019年4月4日にGynecologic Oncologyにオンラインで発表された。 このオープンアクセスの論文は、「子宮頸部上皮内悪性腫瘍グレード2および3におけるTipapkinogen Sovacivec治療用HPVワクチンの有効性および安全性:2.5年の追跡調査を伴う無作為化対照第II相試験(The Efficacy and Safety of Tipapkinogen Sovacivec Therapeutic HPV Vaccine in Cervical Intraepithelial Neoplasia Grades 2 and 3: Randomized Controlled Phase II Trial with 2.5 Years of Follow-Up.)」と題されている。
子宮頸部の前癌を治療するための新しい免疫療法により、臨床試験に参加した3分の1の女性が病変とHPV感染の両方を完全に排除することに成功した。この注射(治療用ワクチン)には、子宮頸部上皮内腫瘍(CIN: cervical intraepithelial neoplasia)として知られるほぼすべての子宮頸癌前駆体の原因となるハイリスクのヒトパピローマウイルス(HPV: human papilloma virus)を攻撃する免疫系反応を引き起こす3種類のタンパク質遺伝子が含まれている。「HPVに感染している女性を治療するための製品は殆ど無い。比較的簡単で成功率がこのようなものを見たのは今回が初めてで、非常にエキサイティングだ。」とミシガン大学医学部の家族医学および産科婦人科教授のDiane Harper博士(写真)は述べた。頸部前癌病変は3段階の重症度に分類される。CIN 2病変はしばしば自然に消失するが、CIN 3病変に進行することもある。 CIN 3が最も重症で、成長が非常に遅い疾患だが、30年以内にCIN 3病変の半分以下が癌になることがある。「しかし、CIN 3のどの女性ががんになるのか、どの女性ががんにならないのかを判断する方法は無い。したがって、CIN 2または3の女性はすべてがんになる可能性があるものとして扱う」とHarper博士は語った。この研究では、CIN2またはCIN3と診断された192人の女性が登録し、129人がワクチン接種を受け、63人がプラセボ投与を受けた。 大腿部に3回、1週間に1回、3週間、女性に注射を3回行った。 6ヵ月後、女性はCIN 2/3のための標準的な外科的処置で治療され、切除された組織を検査した。ワクチン接種を受けた女性は、HPV感染症の種類に関わらず、プラセボグループの女性の2倍以上のCIN消失を確認した。 結果はより重症のCIN3で最も顕著であった:ワクチンを投与された人の36%でCIN3が排除されたのに対し、プラセボグループの女性ではCIN3の排除は見られなかった。手術後もう2年半の間参加者を追跡した長期の追跡調査では、プラセボよりワクチン接種を受けた人々のほうが優れていることを示し、ワクチン群のより多くの女性がHPVを完全に排除したままであった。この研究は、2019年4月4日にGynecologic Oncologyにオンラインで発表された。 このオープンアクセスの論文は、「子宮頸部上皮内悪性腫瘍グレード2および3におけるTipapkinogen Sovacivec治療用HPVワクチンの有効性および安全性:2.5年の追跡調査を伴う無作為化対照第II相試験(The Efficacy and Safety of Tipapkinogen Sovacivec Therapeutic HPV Vaccine in Cervical Intraepithelial Neoplasia Grades 2 and 3: Randomized Controlled Phase II Trial with 2.5 Years of Follow-Up.)」と題されている。
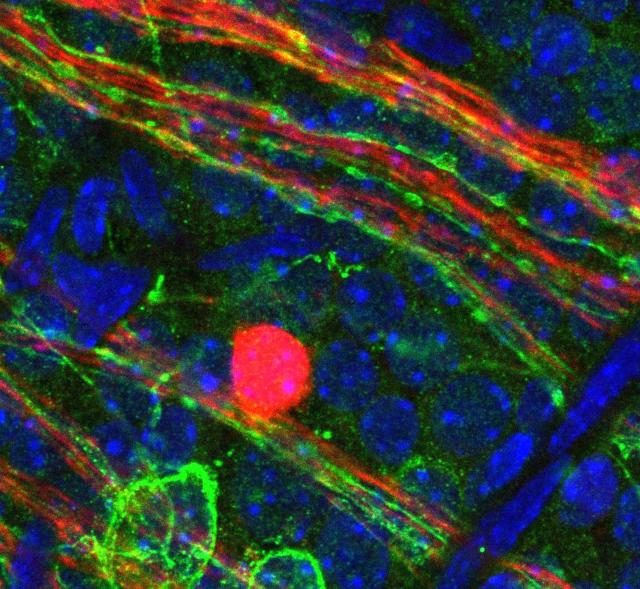 シンシナティ小児病院医療センターの研究チームによって、眼の中で血管の発達を調節する光依存性分子パスウェイが発見された。未熟児網膜症(ROP:retinopathy of prematurity)と近視(近視眼症)の未熟児を救うために光線療法を使うことが可能になるかもしれないことを示唆している。2019年4月1日にNature Cell Biologのオンラインで発表されたこの論文のタイトルは「オプシン5-ドーパミン パスウェイが眼の光依存性血管発達を媒介する(An Opsin 5–Dopamine Pathway Mediates Light-Dependent Vascular Development in the Eye.)」と題されている。
シンシナティ小児病院医療センターの研究チームによって、眼の中で血管の発達を調節する光依存性分子パスウェイが発見された。未熟児網膜症(ROP:retinopathy of prematurity)と近視(近視眼症)の未熟児を救うために光線療法を使うことが可能になるかもしれないことを示唆している。2019年4月1日にNature Cell Biologのオンラインで発表されたこの論文のタイトルは「オプシン5-ドーパミン パスウェイが眼の光依存性血管発達を媒介する(An Opsin 5–Dopamine Pathway Mediates Light-Dependent Vascular Development in the Eye.)」と題されている。
 ウィスコンシン大学マディソン校の生物統計学および医学生物情報学科の助教授Qiongshi Lu博士とその同僚による新しい研究によると、遺伝子は人の顔の美しさを決定する役割を果たすが、その役割は性別によって異なるという。2019年4月4日にPLOS Geneticsに掲載されたこのオープンアクセス論文は「ゲノムワイド関連解析(GWAS)は顔の魅力の性特異的遺伝的構造を明らかにする(Genome-Wide Association Study Reveals Sex-Specific Genetic Architecture of Facial Attractiveness.)」と題されている。人は美しさに夢中になる傾向がある - 人の魅力は学業成績、キャリアの成功、そして所得階層の上位移動に関連している。しかし、その重要性にもかかわらず、科学者たちはかわいい顔を持つことの遺伝的根拠についてほとんど何も知らなかった。現在の研究では、研究者らは4,383人の個人からの遺伝情報を用いてゲノムワイド関連解析(GWAS)を行い、顔の美しさに関連するゲノムの部分を特定した。彼らは、ヨーロッパ人の祖先を持つ参加者からの魅力に基づいて年鑑の写真を採点し、得点を各人の遺伝情報と比較した。 研究者らは、顔の魅力に関連するいくつかの遺伝子を同定したが、それらの役割および他のヒトの特徴との関連性は性別によって異なる。女性では、美しさに関連する特定の遺伝的変異も体重に影響を与える遺伝子に関連しているように見えたが、男性では、顔の魅力の変異は血中コレステロールレベルに影響を及ぼす遺伝子に関連していた。 この研究は、顔の魅力の根底にある遺伝的要因への新しい洞察を提供し、美と他の人間の特性との間の複雑な関係を浮き彫りにしている。「人間の他の多くの特性と同様に、人の魅力を決定づけるマスター遺伝子は存在しない。その代わりに、それは弱い効果を伴う多数の遺伝的要素と関連している可能性が最も高い。興味深いことに、性特異性は我々の研究のほとんどすべての分析において観察されるパターンである。」と著者のQiongshi Lu博士は述べた。しかしこの研究者らは、自分達の調査結果は同年代および民族的背景を持つ同種の個人のグループに基づいていることを認めており、多様な集団や年齢から成るより大きなサンプル数の人々を含んだ解析を提案しいる。将来、この非常に価値のある人間の特徴について、さらに解明が進むだろう。BioQuick News:Genetics of Beauty—Genes Associated with Facial Attractiveness Vary Depending on Sex, According to New Study from University of Wisconsin-Madison
ウィスコンシン大学マディソン校の生物統計学および医学生物情報学科の助教授Qiongshi Lu博士とその同僚による新しい研究によると、遺伝子は人の顔の美しさを決定する役割を果たすが、その役割は性別によって異なるという。2019年4月4日にPLOS Geneticsに掲載されたこのオープンアクセス論文は「ゲノムワイド関連解析(GWAS)は顔の魅力の性特異的遺伝的構造を明らかにする(Genome-Wide Association Study Reveals Sex-Specific Genetic Architecture of Facial Attractiveness.)」と題されている。人は美しさに夢中になる傾向がある - 人の魅力は学業成績、キャリアの成功、そして所得階層の上位移動に関連している。しかし、その重要性にもかかわらず、科学者たちはかわいい顔を持つことの遺伝的根拠についてほとんど何も知らなかった。現在の研究では、研究者らは4,383人の個人からの遺伝情報を用いてゲノムワイド関連解析(GWAS)を行い、顔の美しさに関連するゲノムの部分を特定した。彼らは、ヨーロッパ人の祖先を持つ参加者からの魅力に基づいて年鑑の写真を採点し、得点を各人の遺伝情報と比較した。 研究者らは、顔の魅力に関連するいくつかの遺伝子を同定したが、それらの役割および他のヒトの特徴との関連性は性別によって異なる。女性では、美しさに関連する特定の遺伝的変異も体重に影響を与える遺伝子に関連しているように見えたが、男性では、顔の魅力の変異は血中コレステロールレベルに影響を及ぼす遺伝子に関連していた。 この研究は、顔の魅力の根底にある遺伝的要因への新しい洞察を提供し、美と他の人間の特性との間の複雑な関係を浮き彫りにしている。「人間の他の多くの特性と同様に、人の魅力を決定づけるマスター遺伝子は存在しない。その代わりに、それは弱い効果を伴う多数の遺伝的要素と関連している可能性が最も高い。興味深いことに、性特異性は我々の研究のほとんどすべての分析において観察されるパターンである。」と著者のQiongshi Lu博士は述べた。しかしこの研究者らは、自分達の調査結果は同年代および民族的背景を持つ同種の個人のグループに基づいていることを認めており、多様な集団や年齢から成るより大きなサンプル数の人々を含んだ解析を提案しいる。将来、この非常に価値のある人間の特徴について、さらに解明が進むだろう。BioQuick News:Genetics of Beauty—Genes Associated with Facial Attractiveness Vary Depending on Sex, According to New Study from University of Wisconsin-Madison
 初めて、クロロフィルを生産するにも関わらず光合成に従事しない微生物が発見された。 それは世界中のサンゴの70%で発見され、将来的にサンゴ礁を保護するための手がかりを提供する可能性があるため、この特殊な微生物は「corallicolid」と命名された。2019年4月3日にNatureのオンラインで報告されたこの論文は「クロロフィル生合成遺伝子を含む広範囲のサンゴ感染アピコンプレクサ(A Widespread Coral-Infecting Apicomplexan with Chlorophyll Biosynthesis Genes.)」と題されている。この研究について、ブリティッシュコロンビア大学(UBC)の植物学者で上級研究者であるPatrick Keeling博士は、次のように述べている。「この微生物は全く新しい生化学的疑問を投げかけている。それは寄生虫のように見え、そしてそれは間違いなく光合成ではない。しかし、それは依然としてクロロフィルを作り出す。」クロロフィルは、植物や藻類に含まれる緑色の色素で、光合成中に太陽光からエネルギーを吸収することができる。 「クロロフィルはエネルギーを捕捉するのに非常に優れているので、光合成なしでクロロフィルを持つことは実際には非常に危険だ。それは光合成なしでエネルギーをゆっくり放出するのは、細胞の中に爆弾を抱えて生きるようなものだ。」とKeeling博士は語った。
初めて、クロロフィルを生産するにも関わらず光合成に従事しない微生物が発見された。 それは世界中のサンゴの70%で発見され、将来的にサンゴ礁を保護するための手がかりを提供する可能性があるため、この特殊な微生物は「corallicolid」と命名された。2019年4月3日にNatureのオンラインで報告されたこの論文は「クロロフィル生合成遺伝子を含む広範囲のサンゴ感染アピコンプレクサ(A Widespread Coral-Infecting Apicomplexan with Chlorophyll Biosynthesis Genes.)」と題されている。この研究について、ブリティッシュコロンビア大学(UBC)の植物学者で上級研究者であるPatrick Keeling博士は、次のように述べている。「この微生物は全く新しい生化学的疑問を投げかけている。それは寄生虫のように見え、そしてそれは間違いなく光合成ではない。しかし、それは依然としてクロロフィルを作り出す。」クロロフィルは、植物や藻類に含まれる緑色の色素で、光合成中に太陽光からエネルギーを吸収することができる。 「クロロフィルはエネルギーを捕捉するのに非常に優れているので、光合成なしでクロロフィルを持つことは実際には非常に危険だ。それは光合成なしでエネルギーをゆっくり放出するのは、細胞の中に爆弾を抱えて生きるようなものだ。」とKeeling博士は語った。
 71歳のスコットランド人女性(Jo Cameronさん・写真)は、これまでに同定されていない遺伝子の変異によって痛みをほとんど感じず、ごくわずかな不安や恐怖しか経験したことがなく、この突然変異のために創傷治癒能力が増強されているかもしれないので、新しい治療法を導くのに有用な可能性がある、とロンドン大学ユニバーシティカレッジ(UCL)の共同研究者がthe British Journal of Anaesthesiaで報告した。このオープンアクセスの論文は、「高アナンダミド濃度と痛みを感じない患者で同定されたFAAH偽遺伝子の微小欠失(Microdeletion in a FAAH Pseudogene Identified In A Patient With High Anandamide Concentrations And Pain Insensitivity.)」と題されている。「この女性は、疼痛や不安の治療対象となるかもしれないと考えられている遺伝子の活性を低下させる特定の遺伝子型を持っていることが分かった。我々はこの新たに同定された遺伝子がどのように機能するのかを明らかにし、新しい治療標的をさらに進歩させることを望んでいる。」と、この研究の主要研究者の一人、James Cox博士(UCL Medicine)は述べた。65歳の時、この女性は股関節の治療を求めていたが、痛みがないにもかかわらず重度の関節変性を伴うことが判明した。 66歳の時、彼女は手の手術を受けたが、これは通常非常に痛みを伴うにも関わらず手術後も痛みは報告されなかった。彼女の疼痛感受性について、スコットランド北部のNHS病院の麻酔コンサルタントであるDevjit Srivastava博士と、この論文の共著者が診断した。女性は、歯科手術などの手術後に鎮痛剤を必要としたことがないことを研究者に伝えた。 彼女はUCLとオックスフォード大学の疼痛遺伝学者に紹介され、遺伝解析により2つの注目すべき突然変異が発見された。1つは偽遺伝子の微小欠失で、これまでは医学文献で簡単な注釈が付けられていただけであったが、研究者らは初めてこれを説明し、FAAH-OUTと名付けた。 彼女はまた、FAAH(脂肪酸アミド加水分解酵素)酵素を制御する隣接遺伝子にも突然変異があった。カナダのカルガリー大学の共同研究者らによるさらなる試験では、通常はFAAHによって分解される神経伝達物質の血中濃度の上昇、FAAH機能の喪失のさらなる証拠が明らかにされた。FAAH遺伝子は、痛みの感覚、気分、および記憶の中心となる内在性カンナビノイドシグナル伝達に関与しているため、痛みの研究者にはよく知られている。現在FAAH-OUTと呼ばれる偽遺伝子は、以前は機能的ではない「ジャンク」遺伝子であると考えられていた。 研究者らは、FAAHの発現を媒介している可能性があり、以前に信じられていた以上のことがあると見出した。
71歳のスコットランド人女性(Jo Cameronさん・写真)は、これまでに同定されていない遺伝子の変異によって痛みをほとんど感じず、ごくわずかな不安や恐怖しか経験したことがなく、この突然変異のために創傷治癒能力が増強されているかもしれないので、新しい治療法を導くのに有用な可能性がある、とロンドン大学ユニバーシティカレッジ(UCL)の共同研究者がthe British Journal of Anaesthesiaで報告した。このオープンアクセスの論文は、「高アナンダミド濃度と痛みを感じない患者で同定されたFAAH偽遺伝子の微小欠失(Microdeletion in a FAAH Pseudogene Identified In A Patient With High Anandamide Concentrations And Pain Insensitivity.)」と題されている。「この女性は、疼痛や不安の治療対象となるかもしれないと考えられている遺伝子の活性を低下させる特定の遺伝子型を持っていることが分かった。我々はこの新たに同定された遺伝子がどのように機能するのかを明らかにし、新しい治療標的をさらに進歩させることを望んでいる。」と、この研究の主要研究者の一人、James Cox博士(UCL Medicine)は述べた。65歳の時、この女性は股関節の治療を求めていたが、痛みがないにもかかわらず重度の関節変性を伴うことが判明した。 66歳の時、彼女は手の手術を受けたが、これは通常非常に痛みを伴うにも関わらず手術後も痛みは報告されなかった。彼女の疼痛感受性について、スコットランド北部のNHS病院の麻酔コンサルタントであるDevjit Srivastava博士と、この論文の共著者が診断した。女性は、歯科手術などの手術後に鎮痛剤を必要としたことがないことを研究者に伝えた。 彼女はUCLとオックスフォード大学の疼痛遺伝学者に紹介され、遺伝解析により2つの注目すべき突然変異が発見された。1つは偽遺伝子の微小欠失で、これまでは医学文献で簡単な注釈が付けられていただけであったが、研究者らは初めてこれを説明し、FAAH-OUTと名付けた。 彼女はまた、FAAH(脂肪酸アミド加水分解酵素)酵素を制御する隣接遺伝子にも突然変異があった。カナダのカルガリー大学の共同研究者らによるさらなる試験では、通常はFAAHによって分解される神経伝達物質の血中濃度の上昇、FAAH機能の喪失のさらなる証拠が明らかにされた。FAAH遺伝子は、痛みの感覚、気分、および記憶の中心となる内在性カンナビノイドシグナル伝達に関与しているため、痛みの研究者にはよく知られている。現在FAAH-OUTと呼ばれる偽遺伝子は、以前は機能的ではない「ジャンク」遺伝子であると考えられていた。 研究者らは、FAAHの発現を媒介している可能性があり、以前に信じられていた以上のことがあると見出した。
 黒死病と呼ばれ14世紀のヨーロッパを襲った壊滅的な伝染病ペストは、今はもう絶滅したバクテリアYersinia pestisによるものだと思われる。この記事は2011年8月29日付けのPNAS誌に発表された。カナダのマックマスター大学のポワナー・ヘンデリック博士と研究者グループは、イギリスのロンドンにあるイースト・スミスフィールドの集団埋葬地から掘り出された109人の白骨遺体から検出されたDNAを分析し、この結果にたどり着いた。また、セント・ニコラス・シャンブルから掘り出された10人の遺骨からもDNAを検出し、解析を行なった。イースト・スミスフィールドに埋葬されていた遺骨からはY. pestisの遺伝子が見つかり、著者達によって配列解析されたこの遺伝子は、古来の病原体の中でも最も歴史の長い遺伝子の集合体である。
黒死病と呼ばれ14世紀のヨーロッパを襲った壊滅的な伝染病ペストは、今はもう絶滅したバクテリアYersinia pestisによるものだと思われる。この記事は2011年8月29日付けのPNAS誌に発表された。カナダのマックマスター大学のポワナー・ヘンデリック博士と研究者グループは、イギリスのロンドンにあるイースト・スミスフィールドの集団埋葬地から掘り出された109人の白骨遺体から検出されたDNAを分析し、この結果にたどり着いた。また、セント・ニコラス・シャンブルから掘り出された10人の遺骨からもDNAを検出し、解析を行なった。イースト・スミスフィールドに埋葬されていた遺骨からはY. pestisの遺伝子が見つかり、著者達によって配列解析されたこの遺伝子は、古来の病原体の中でも最も歴史の長い遺伝子の集合体である。
 合成ペプチド(TNF由来のTIPペプチド)が腎炎で起こる破壊的な炎症を中断し、腎臓がその重要な機能をよりよく回復し維持することを可能にするとジョージア医科大学の研究者らは報告している。TIPペプチドを全身に投与しても腎臓に直接投与しても、血圧を上昇させることなく免疫細胞の腎臓への移動を抑制し、炎症と損傷を解消し、腎機能を改善した。
合成ペプチド(TNF由来のTIPペプチド)が腎炎で起こる破壊的な炎症を中断し、腎臓がその重要な機能をよりよく回復し維持することを可能にするとジョージア医科大学の研究者らは報告している。TIPペプチドを全身に投与しても腎臓に直接投与しても、血圧を上昇させることなく免疫細胞の腎臓への移動を抑制し、炎症と損傷を解消し、腎機能を改善した。
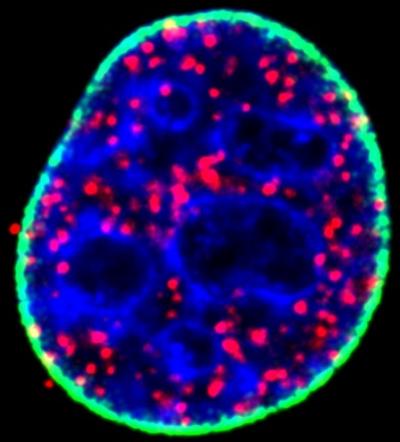 これまで突然変異したタンパク質p53が、さまざまな癌の発症において重要な因子であり、一方でその変異していない形態は、癌から保護することが知られてきた。 これらの対立する特質により、p53タンパク質およびそれをコードする遺伝子は生物学において最も研究されている対象の一つだが、その安定性および機能を支配する分子機構はまだ完全には理解されていない。ウィスコンシン大学マディソン校(UW-Madison)の癌研究者であるRichard A. Anderson博士とウィスコンシン大学医学部のVincent Cryns医師らの研究チームは、重要なタンパク質の予想外の調節因子の発見を報告し、それを標的とする薬物の開発へ扉を開いた。2019年3月18日にNature Cell Biologyに掲載されたこの論文は、「核ホスホイノシチドキナーゼ複合体がp53を調節する(A Nuclear Phosphoinositide Kinase Complex Regulates p53.)」と題されている。「ローマ神話の出入り口と扉の守護神ヤヌスの様に、p53には2つの面がある。p53遺伝子は癌において最も頻繁に変異する遺伝子であり、そして変異すると、それはその機能を腫瘍抑制因子から癌遺伝子の大部分を駆動する癌遺伝子に変える。」とAnderson博士は述べた。Anderson博士によると、通常p53タンパク質は「ゲノムの保護者」として働き、紫外線、化学物質、その他の方法で損傷を受けたDNAの修復を開始し、腫瘍の増殖を防ぐ。 しかし、変異するとタンパク質は悪事を働くようになり、未変異のタンパク質よりも安定して豊富になり、細胞の核に蓄積して癌を引き起こす。ウィスコンシン大学の研究チームで、Suyong Choi博士とMo Chen博士がこの安定性を推進する新しいメカニズムを発見した。 この原因はPIPK1-αと呼ばれる酵素であり、その脂質メッセンジャーはPIP2として知られており、p53の主な調節因子として振る舞うらしい。
これまで突然変異したタンパク質p53が、さまざまな癌の発症において重要な因子であり、一方でその変異していない形態は、癌から保護することが知られてきた。 これらの対立する特質により、p53タンパク質およびそれをコードする遺伝子は生物学において最も研究されている対象の一つだが、その安定性および機能を支配する分子機構はまだ完全には理解されていない。ウィスコンシン大学マディソン校(UW-Madison)の癌研究者であるRichard A. Anderson博士とウィスコンシン大学医学部のVincent Cryns医師らの研究チームは、重要なタンパク質の予想外の調節因子の発見を報告し、それを標的とする薬物の開発へ扉を開いた。2019年3月18日にNature Cell Biologyに掲載されたこの論文は、「核ホスホイノシチドキナーゼ複合体がp53を調節する(A Nuclear Phosphoinositide Kinase Complex Regulates p53.)」と題されている。「ローマ神話の出入り口と扉の守護神ヤヌスの様に、p53には2つの面がある。p53遺伝子は癌において最も頻繁に変異する遺伝子であり、そして変異すると、それはその機能を腫瘍抑制因子から癌遺伝子の大部分を駆動する癌遺伝子に変える。」とAnderson博士は述べた。Anderson博士によると、通常p53タンパク質は「ゲノムの保護者」として働き、紫外線、化学物質、その他の方法で損傷を受けたDNAの修復を開始し、腫瘍の増殖を防ぐ。 しかし、変異するとタンパク質は悪事を働くようになり、未変異のタンパク質よりも安定して豊富になり、細胞の核に蓄積して癌を引き起こす。ウィスコンシン大学の研究チームで、Suyong Choi博士とMo Chen博士がこの安定性を推進する新しいメカニズムを発見した。 この原因はPIPK1-αと呼ばれる酵素であり、その脂質メッセンジャーはPIP2として知られており、p53の主な調節因子として振る舞うらしい。
 イギリスのオックスフォードにあるルートヴィヒ癌研究所の科学者らは、2019年2月25日にNature Biotechnologyにオンラインで報告した研究で、DNAの化学修飾を検出するための新しく改良された方法を記載している。これらの修飾、または「エピジェネティック」マークは、遺伝子発現の制御を助け、それらのゲノム全体での異常な分布は癌の進行および治療抵抗性に関与している。
イギリスのオックスフォードにあるルートヴィヒ癌研究所の科学者らは、2019年2月25日にNature Biotechnologyにオンラインで報告した研究で、DNAの化学修飾を検出するための新しく改良された方法を記載している。これらの修飾、または「エピジェネティック」マークは、遺伝子発現の制御を助け、それらのゲノム全体での異常な分布は癌の進行および治療抵抗性に関与している。
 ホオジロザメは地球上で最も有名な海洋生物の1つであり、広く人々の注目を集め、ハリウッドの歴史の中で最も成功した映画の1つ「ジョーズ」を生み出した。このサメは、その巨大なサイズ(最大6メートルと3トン)、そしておよそ1200メートルの深さまで潜ることを含む顕著な特徴を有する。 ホオジロザメはまた、世界の海洋において比較的少数であることを考えると、重要な保全対象でもある。この象徴的な頂点捕食者と一般的なサメの生物学を理解するために、ホオジロザメの全ゲノムが詳細に解読された。 (NSU)ノバサウスイースタン大学のSave Our Seas Foundationサメ研究センター(フロリダ州マイアミ)とガイハーヴェイ研究所(フロリダ州マイアミ)、コーネル大学獣医学部(ニューヨーク州イサカ)の科学者が率いるチーム そして、モントレーベイ水族館(カリフォルニア州モントレー)は、ホオジロザメのゲノムを完成させ、そしてそれを巨大なジンベイザメおよびヒトを含む他の様々な脊椎動物由来のゲノムと比較した。この研究論文はPNASで2019年2月19日にオンラインで報告され、「White Shark Genomeは創傷治癒とゲノム安定性の維持に関連する古代の軟骨魚類の適応を明らかにする(White Shark Genome Reveals Ancient Elasmobranch Adaptations Associated with Wound Healing and the Maintenance of Genome Stability.)」と題されている。ホオジロザメのゲノムを解読すると、その巨大なサイズ(ヒトゲノムの1.5倍のサイズ)だけでなく、大型で長寿命のサメの進化的な成功の背後にある豊富な遺伝的変化も明らかになった。研究者らは、ゲノム安定性の維持に重要な役割を果たす多数の遺伝子における分子適応(ポジティブセレクションとも呼ばれる)を示す特異的なDNA配列変化の顕著な発生を発見した。 ゲノムの完全性 これらの適応的配列変化は、他の遺伝子の中でもとりわけ、DNA修復、DNA損傷応答、およびDNA損傷耐性に密接に関連する遺伝子で見出された。 これとは逆の現象である、ゲノムの不安定性は、蓄積したDNA損傷によって引き起こされ、人間を多数の癌や加齢に伴う病気にかかりやすくすることで知られている。
ホオジロザメは地球上で最も有名な海洋生物の1つであり、広く人々の注目を集め、ハリウッドの歴史の中で最も成功した映画の1つ「ジョーズ」を生み出した。このサメは、その巨大なサイズ(最大6メートルと3トン)、そしておよそ1200メートルの深さまで潜ることを含む顕著な特徴を有する。 ホオジロザメはまた、世界の海洋において比較的少数であることを考えると、重要な保全対象でもある。この象徴的な頂点捕食者と一般的なサメの生物学を理解するために、ホオジロザメの全ゲノムが詳細に解読された。 (NSU)ノバサウスイースタン大学のSave Our Seas Foundationサメ研究センター(フロリダ州マイアミ)とガイハーヴェイ研究所(フロリダ州マイアミ)、コーネル大学獣医学部(ニューヨーク州イサカ)の科学者が率いるチーム そして、モントレーベイ水族館(カリフォルニア州モントレー)は、ホオジロザメのゲノムを完成させ、そしてそれを巨大なジンベイザメおよびヒトを含む他の様々な脊椎動物由来のゲノムと比較した。この研究論文はPNASで2019年2月19日にオンラインで報告され、「White Shark Genomeは創傷治癒とゲノム安定性の維持に関連する古代の軟骨魚類の適応を明らかにする(White Shark Genome Reveals Ancient Elasmobranch Adaptations Associated with Wound Healing and the Maintenance of Genome Stability.)」と題されている。ホオジロザメのゲノムを解読すると、その巨大なサイズ(ヒトゲノムの1.5倍のサイズ)だけでなく、大型で長寿命のサメの進化的な成功の背後にある豊富な遺伝的変化も明らかになった。研究者らは、ゲノム安定性の維持に重要な役割を果たす多数の遺伝子における分子適応(ポジティブセレクションとも呼ばれる)を示す特異的なDNA配列変化の顕著な発生を発見した。 ゲノムの完全性 これらの適応的配列変化は、他の遺伝子の中でもとりわけ、DNA修復、DNA損傷応答、およびDNA損傷耐性に密接に関連する遺伝子で見出された。 これとは逆の現象である、ゲノムの不安定性は、蓄積したDNA損傷によって引き起こされ、人間を多数の癌や加齢に伴う病気にかかりやすくすることで知られている。
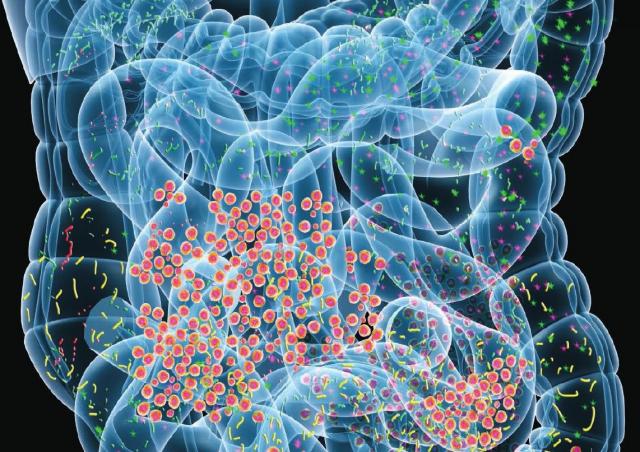 身体の免疫系による関節、皮膚、および腎臓への攻撃が特徴の病気である全身性エリテマトーデス(SLE:systemic lupus erythematosus)は、腸内のバクテリアの異常な混合と関連していることが新研究で判明した。これは、ニューヨーク大学Langone Health / ニューヨーク大学医学部の科学者らによる新研究によるものだ。 細菌性不均衡は炎症性腸疾患、関節炎、そしていくつかの癌を含む多くの免疫関連疾患と結びついているが、この研究は腸内の細菌性不均衡とSLEの潜在的な生命への脅威の関連についての初めての詳細な証拠である。2019年2月19日にリウマチ性疾患学会誌にオンラインで発表されたこの新研究は、SLEと診断された61人の女性が、同じ年齢および人種的背景を持たない17人の健常な女性の約5倍以上の腸内細菌を持っていたことを示した。狼瘡(Lupus)は男性より女性の方が多い。研究結果によると、皮膚の発疹や関節の痛みから透析を必要とする重度の腎臓機能障害に至るまでの疾患「フレア(flares)」において、腸内で増殖するR.gnavus菌を示す抗体が血液サンプルに大幅に増加するという。腎臓フレアを有する試験参加者は、R. gnavusに対する抗体が特に高レベルであった。このオープンアクセスの論文は、「狼瘡腎炎は疾患活動の拡大と腸の常在菌に対する免疫に関連している(Lupus Nephritis Is Linked to Disease-Activity Associated Expansions and Immunity to a Gut Commensal.)」と題されている。著者らは、遺伝的要因もあり、150万人ものアメリカ人に影響を与える狼瘡の具体的な原因は不明であると述べている。
身体の免疫系による関節、皮膚、および腎臓への攻撃が特徴の病気である全身性エリテマトーデス(SLE:systemic lupus erythematosus)は、腸内のバクテリアの異常な混合と関連していることが新研究で判明した。これは、ニューヨーク大学Langone Health / ニューヨーク大学医学部の科学者らによる新研究によるものだ。 細菌性不均衡は炎症性腸疾患、関節炎、そしていくつかの癌を含む多くの免疫関連疾患と結びついているが、この研究は腸内の細菌性不均衡とSLEの潜在的な生命への脅威の関連についての初めての詳細な証拠である。2019年2月19日にリウマチ性疾患学会誌にオンラインで発表されたこの新研究は、SLEと診断された61人の女性が、同じ年齢および人種的背景を持たない17人の健常な女性の約5倍以上の腸内細菌を持っていたことを示した。狼瘡(Lupus)は男性より女性の方が多い。研究結果によると、皮膚の発疹や関節の痛みから透析を必要とする重度の腎臓機能障害に至るまでの疾患「フレア(flares)」において、腸内で増殖するR.gnavus菌を示す抗体が血液サンプルに大幅に増加するという。腎臓フレアを有する試験参加者は、R. gnavusに対する抗体が特に高レベルであった。このオープンアクセスの論文は、「狼瘡腎炎は疾患活動の拡大と腸の常在菌に対する免疫に関連している(Lupus Nephritis Is Linked to Disease-Activity Associated Expansions and Immunity to a Gut Commensal.)」と題されている。著者らは、遺伝的要因もあり、150万人ものアメリカ人に影響を与える狼瘡の具体的な原因は不明であると述べている。
 カメラの進歩と同様、一般的なバイオインフォマティクスデータの可視化手法の重要な数学的更新により、単一細胞遺伝子発現のスナップショットが数倍の速さ且つ遥かに高い解像度で作成できるようになった。2019年2月11日にNature Methodsに掲載されたこのエール大学の数学者による革新は、100万点のシングルセルRNAシーケンス(scRNA-seq)データセットのレンダリング時間を3時間以上からわずか15分に短縮するものだ。
カメラの進歩と同様、一般的なバイオインフォマティクスデータの可視化手法の重要な数学的更新により、単一細胞遺伝子発現のスナップショットが数倍の速さ且つ遥かに高い解像度で作成できるようになった。2019年2月11日にNature Methodsに掲載されたこのエール大学の数学者による革新は、100万点のシングルセルRNAシーケンス(scRNA-seq)データセットのレンダリング時間を3時間以上からわずか15分に短縮するものだ。
 何十年もの間、科学者や医者は土壌中のバクテリアがある種の膵臓癌のための重要な治療薬である抗生物質化合物のストレプトゾトシンを製造することを知っていたが、バクテリアがどうやってそれを合成するのか不明だった。ハーバード大学の化学・化学生物学教授のEmily Balskus博士が率いる研究者チームはそのプロセスを解明し、この化合物が酵素経路を介して生産されることを初めて示し、そのプロセスを推進する新たな化学を明らかにした。
何十年もの間、科学者や医者は土壌中のバクテリアがある種の膵臓癌のための重要な治療薬である抗生物質化合物のストレプトゾトシンを製造することを知っていたが、バクテリアがどうやってそれを合成するのか不明だった。ハーバード大学の化学・化学生物学教授のEmily Balskus博士が率いる研究者チームはそのプロセスを解明し、この化合物が酵素経路を介して生産されることを初めて示し、そのプロセスを推進する新たな化学を明らかにした。
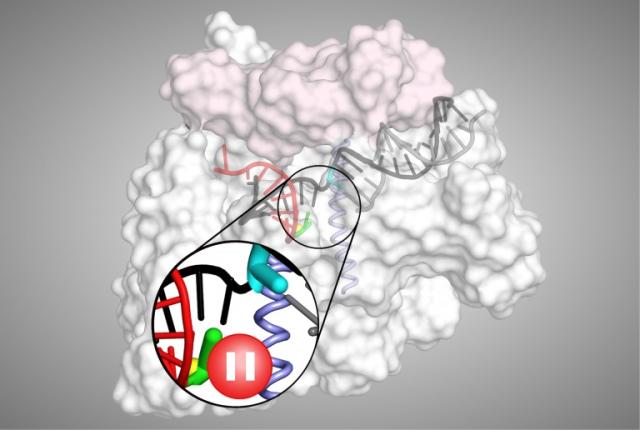 ウィスコンシン大学マディソン校の生化学および細菌学教授のRobert Landick博士と彼のチームが率いた研究は、すべての生物における遺伝子発現制御の根底にある現象、転写の一時停止の要素メカニズムを初めて明らかにした。この研究はまた、ディフィシル菌感染症や結核などの治療の重要な薬物標的である酵素RNAポリメラーゼについての新しい理解を提供している。
ウィスコンシン大学マディソン校の生化学および細菌学教授のRobert Landick博士と彼のチームが率いた研究は、すべての生物における遺伝子発現制御の根底にある現象、転写の一時停止の要素メカニズムを初めて明らかにした。この研究はまた、ディフィシル菌感染症や結核などの治療の重要な薬物標的である酵素RNAポリメラーゼについての新しい理解を提供している。
 アラバマ大学バーミンガム校(University of Alabama at Birmingham :UAB)の研究者らは、慢性閉塞性肺疾患(COPD)患者の肺における慢性炎症と組織破壊との間の根本的なつながりである、これまで報告されていない新しい病原体を発見した。 COPDは世界における死因の第4位だ。精製された活性化多形核白血球(PMN: polymorphonuclear leukocytes)から収集された小さな細胞内粒子が健康なマウスの肺に点滴注入されたとき、この病原体 - PMN由来 エクソソーム - はCOPD損傷を引き起こした。注目すべき点は、UABの研究者らはCOPDのヒト患者の肺液および肺疾患の気管支肺異形成症のICU乳児の肺液からエクソソームも収集した。 そのヒト由来のエクソソームを健康なマウスの肺に点滴注入すると、それらはまたCOPD肺損傷を引き起こした。損傷は主にヒトの肺由来のPMN由来のエクソソームからのものであった。 「この報告は、非感染性subcellular entityがヒトからマウスに移されたときに疾患表現型を再現する能力の最初のエビデンスのように思われる。これは非常に意味深い発見になると思われる。ここで発見したことの多くは、病気によっては他の組織にも当てはまるだろう。」とUAB医学部 肺・アレルギーおよび救急医療教授のJ. Edwin Blalock博士は述べた。免疫細胞炎症および組織破壊によって特徴付けられる他の疾患には、心臓発作、転移性癌および慢性腎臓病が含まれる。 活性化されたPMNエクソソームはまた、嚢胞性線維症などの過剰なPMN駆動炎症を有する他の疾患における肺損傷にも寄与し得る。この研究はCell誌で報告された。 この論文は2018年1月10日にオンラインで公開され、「活性化PMNエクソソーム:肺の中でマトリックスの破壊と病気を引き起こす病原体(Activated PMN Exosomes: Pathogenic Entities Causing Matrix Destruction and Disease in the Lung.)」と題されている。「これらの調査結果は、慢性肺疾患における先天性免疫反応の新たな役割を浮き彫りにし、COPDおよびおそらく嚢胞性線維症の新しい診断薬および治療薬の開発に使用できるだろう」と国立衛生研究所の一部である国立心臓肺血液研究所のJames Kiley博士は語った。
アラバマ大学バーミンガム校(University of Alabama at Birmingham :UAB)の研究者らは、慢性閉塞性肺疾患(COPD)患者の肺における慢性炎症と組織破壊との間の根本的なつながりである、これまで報告されていない新しい病原体を発見した。 COPDは世界における死因の第4位だ。精製された活性化多形核白血球(PMN: polymorphonuclear leukocytes)から収集された小さな細胞内粒子が健康なマウスの肺に点滴注入されたとき、この病原体 - PMN由来 エクソソーム - はCOPD損傷を引き起こした。注目すべき点は、UABの研究者らはCOPDのヒト患者の肺液および肺疾患の気管支肺異形成症のICU乳児の肺液からエクソソームも収集した。 そのヒト由来のエクソソームを健康なマウスの肺に点滴注入すると、それらはまたCOPD肺損傷を引き起こした。損傷は主にヒトの肺由来のPMN由来のエクソソームからのものであった。 「この報告は、非感染性subcellular entityがヒトからマウスに移されたときに疾患表現型を再現する能力の最初のエビデンスのように思われる。これは非常に意味深い発見になると思われる。ここで発見したことの多くは、病気によっては他の組織にも当てはまるだろう。」とUAB医学部 肺・アレルギーおよび救急医療教授のJ. Edwin Blalock博士は述べた。免疫細胞炎症および組織破壊によって特徴付けられる他の疾患には、心臓発作、転移性癌および慢性腎臓病が含まれる。 活性化されたPMNエクソソームはまた、嚢胞性線維症などの過剰なPMN駆動炎症を有する他の疾患における肺損傷にも寄与し得る。この研究はCell誌で報告された。 この論文は2018年1月10日にオンラインで公開され、「活性化PMNエクソソーム:肺の中でマトリックスの破壊と病気を引き起こす病原体(Activated PMN Exosomes: Pathogenic Entities Causing Matrix Destruction and Disease in the Lung.)」と題されている。「これらの調査結果は、慢性肺疾患における先天性免疫反応の新たな役割を浮き彫りにし、COPDおよびおそらく嚢胞性線維症の新しい診断薬および治療薬の開発に使用できるだろう」と国立衛生研究所の一部である国立心臓肺血液研究所のJames Kiley博士は語った。
 その小さな体、頑固な顔つき、そして離れ目。ブルドッグ、フレンチブルドッグ、ボストンテリアは様々な犬種の中で最も人気が高い。カリフォルニア大学(UC)デイビス校 獣医学部の研究者らは、これらの犬の外観の遺伝的根拠を見出し、それをヒトにおける希少遺伝性疾患と結びつけた。
その小さな体、頑固な顔つき、そして離れ目。ブルドッグ、フレンチブルドッグ、ボストンテリアは様々な犬種の中で最も人気が高い。カリフォルニア大学(UC)デイビス校 獣医学部の研究者らは、これらの犬の外観の遺伝的根拠を見出し、それをヒトにおける希少遺伝性疾患と結びつけた。
 前臨床モデルにおいても癌患者においても、免疫チェックポイント阻害療法について多くの成功例がある。 しかし、そのような免疫療法がどのようにしてその反応を引き出すのか、そしてチェックポイント阻害療法が癌を根絶するための免疫システムの再活性化に成功(または失敗)する要因については、多くの疑問が残っている。ボストンのBrigham and Women's Hospitalの研究者らが同じくボストンにあるBroad研究所の同僚と共同で行った新しい研究で、腫瘍の免疫細胞の重要なクラスであるT細胞の異なる集団に対する免疫チェックポイント阻害療法の効果を調べた。このチームの驚くべき成果は、過去に見過ごされてきたT細胞の集団を示しており、治療に対する反応を予測する分子因子の同定につながっている。この論文は2019年1月8日のImmunityにオンラインで発表され、「チェックポイント阻害免疫療法は、PD-1-CD8 +腫瘍浸潤T細胞の動的変化を誘導する(Checkpoint Blockade Immunotherapy Induces Dynamic Changes in PD-1−CD8+ Tumor-Infiltrating T Cells.)」と題されている。「我々の研究は、腫瘍内のT細胞には非常に多様性があるという観察を利用している。異なる細胞集団に対する治療の効果を見て、我々は驚いて困惑した。 エクスプレスチェックポイント阻害剤は、遺伝レベルで有意な変化を示した」と、共著者であるBrighamの准科学者およびハーバード大学医学大学院の神経科学准教授のAna Anderson博士(写真)は述べた。 「以前はほとんど無視されてきた細胞だ。我々の研究ではチェックポイント阻害療法が何をしているのか、そしてそれがどのようにその効果を媒介するのかという焦点を広げている。」Anderson博士らは、最新の技術を利用して、さまざまな癌に関与するT細胞に対しコンピューター手法と個々の細胞から何千もの遺伝子の出力を測定するための技術であるシングルセルRNAシーケンスを利用して治療法の効果を調べた。研究者らは反復的なアプローチを取り、興味深いリードの特定を可能にし、次に癌の前臨床モデルでさらなる試験を実施した。このアプローチにより記憶可能な免疫細胞集団の維持および機能に必要とされる転写因子Tcf7が見つかった。 この実験モデルを通して、チームはこの因子が免疫ベースの治療が成功するのに必要であることを発見した。Anderson博士は、現在までのところ、この分野はPD-1やCTLA-4などのチェックポイント受容体を備えた完全に成熟した末期T細胞に主に焦点を当ててきたと述べている。活性化の初期段階では、T細胞はまだこれらの受容体を発現していない。それでも、これらの新生細胞は治療に対する反応を示している。「我々は、チェックポイント阻害療法がどのように機能するのかを明らかにするために、これらの初期段階のT細胞を理解する必要がある」とAnderson博士は述べた。「私たちの研究は、さまざまな癌に関与するチェックポイント阻害免疫療法に反応する重要な免疫細胞集団を特定するのに役立ち、この療法の成功における重要な要因を示している。」「さらなる研究により、治療に対する患者の反応を予測し、免疫療法アプローチを用いてどの細胞を標的とすることが最も重要であるかを特定するためのバイオマーカーを定義できる可能性がある。」Anderson博士は、癌免疫療法に関心を持つPotenza TherapeuticsとTizona Therapeuticsの科学諮問委員会のメンバーである。共著者のVijay Kuchroo博士は、Potenza TherapeuticsとTizona Therapeuticsの科学諮問委員会のメンバーである。共著者のAviv Regev博士は、Thermo FisherおよびSyros Pharmaceuticals and Driver Groupの科学諮問委員会のメンバーである。この研究成果は特許出願中である。【BioQuick News:Scientists ID Transcription Factor (Tcf7) Required for Success of Immune Checkpoint Blockades in Cancer Therapy; Finding May Advance Understanding of How These Therapies Elicit Their Response】
前臨床モデルにおいても癌患者においても、免疫チェックポイント阻害療法について多くの成功例がある。 しかし、そのような免疫療法がどのようにしてその反応を引き出すのか、そしてチェックポイント阻害療法が癌を根絶するための免疫システムの再活性化に成功(または失敗)する要因については、多くの疑問が残っている。ボストンのBrigham and Women's Hospitalの研究者らが同じくボストンにあるBroad研究所の同僚と共同で行った新しい研究で、腫瘍の免疫細胞の重要なクラスであるT細胞の異なる集団に対する免疫チェックポイント阻害療法の効果を調べた。このチームの驚くべき成果は、過去に見過ごされてきたT細胞の集団を示しており、治療に対する反応を予測する分子因子の同定につながっている。この論文は2019年1月8日のImmunityにオンラインで発表され、「チェックポイント阻害免疫療法は、PD-1-CD8 +腫瘍浸潤T細胞の動的変化を誘導する(Checkpoint Blockade Immunotherapy Induces Dynamic Changes in PD-1−CD8+ Tumor-Infiltrating T Cells.)」と題されている。「我々の研究は、腫瘍内のT細胞には非常に多様性があるという観察を利用している。異なる細胞集団に対する治療の効果を見て、我々は驚いて困惑した。 エクスプレスチェックポイント阻害剤は、遺伝レベルで有意な変化を示した」と、共著者であるBrighamの准科学者およびハーバード大学医学大学院の神経科学准教授のAna Anderson博士(写真)は述べた。 「以前はほとんど無視されてきた細胞だ。我々の研究ではチェックポイント阻害療法が何をしているのか、そしてそれがどのようにその効果を媒介するのかという焦点を広げている。」Anderson博士らは、最新の技術を利用して、さまざまな癌に関与するT細胞に対しコンピューター手法と個々の細胞から何千もの遺伝子の出力を測定するための技術であるシングルセルRNAシーケンスを利用して治療法の効果を調べた。研究者らは反復的なアプローチを取り、興味深いリードの特定を可能にし、次に癌の前臨床モデルでさらなる試験を実施した。このアプローチにより記憶可能な免疫細胞集団の維持および機能に必要とされる転写因子Tcf7が見つかった。 この実験モデルを通して、チームはこの因子が免疫ベースの治療が成功するのに必要であることを発見した。Anderson博士は、現在までのところ、この分野はPD-1やCTLA-4などのチェックポイント受容体を備えた完全に成熟した末期T細胞に主に焦点を当ててきたと述べている。活性化の初期段階では、T細胞はまだこれらの受容体を発現していない。それでも、これらの新生細胞は治療に対する反応を示している。「我々は、チェックポイント阻害療法がどのように機能するのかを明らかにするために、これらの初期段階のT細胞を理解する必要がある」とAnderson博士は述べた。「私たちの研究は、さまざまな癌に関与するチェックポイント阻害免疫療法に反応する重要な免疫細胞集団を特定するのに役立ち、この療法の成功における重要な要因を示している。」「さらなる研究により、治療に対する患者の反応を予測し、免疫療法アプローチを用いてどの細胞を標的とすることが最も重要であるかを特定するためのバイオマーカーを定義できる可能性がある。」Anderson博士は、癌免疫療法に関心を持つPotenza TherapeuticsとTizona Therapeuticsの科学諮問委員会のメンバーである。共著者のVijay Kuchroo博士は、Potenza TherapeuticsとTizona Therapeuticsの科学諮問委員会のメンバーである。共著者のAviv Regev博士は、Thermo FisherおよびSyros Pharmaceuticals and Driver Groupの科学諮問委員会のメンバーである。この研究成果は特許出願中である。【BioQuick News:Scientists ID Transcription Factor (Tcf7) Required for Success of Immune Checkpoint Blockades in Cancer Therapy; Finding May Advance Understanding of How These Therapies Elicit Their Response】
 研究者らは、線虫のオスとメスの発育中の脳の違いを誘導し、思春期の開始、ヒトの性的成熟のタイミングを制御するのと同じ機能を持つであろう遺伝経路の引き金となる一群の遺伝子を同定した。コロンビア大学の科学者が率いるこの研究は、神経発達の性差における直接的な遺伝的影響についての新しい証拠を提供し、男性と女性の脳がどのように結びついているか、そしてそれらがどのように機能するかを理解しようとする試みである。この研究は、2019年1月1日にハワード・ヒューズ医学研究所、マックス・プランク研究所、およびウェルカム・トラストによって設立されたオープンアクセスジャーナルeLifeに掲載された。 この論文のタイトルは「性的二型神経系分化のタイミングメカニズム(Timing Mechanism of Sexually Dimorphic Nervous System Differentiation.)」と題されている。思春期はホルモンシグナルの生成でニューロンが活性化することにより特徴付けられる脳の実質的な変化であることを科学者たちは長い間知っていた。しかし、思春期になるホルモンを脳が放出し始める原因は捉えどころのないままであった。コロンビア生物学科の教授でハワード・ヒューズ医学研究所の研究者であるOliver Hobert博士は、次のように述べている。「驚くべきことに、この経路の各メンバーはワームとヒトの間で受け継がれていることが分かった。これは、脳における性的な脳の違いが遺伝的にどのようにコードされるかについての一般原則を明らかにしたことを示している。」この研究のために、研究者らはゲノム配列を決定した最初の多細胞生物である透明線虫C. elegansを利用した。 このワームの遺伝子構成はヒトのものと非常によく似ており、分子遺伝学および発生生物学における最も強力な研究モデルの1つである。
研究者らは、線虫のオスとメスの発育中の脳の違いを誘導し、思春期の開始、ヒトの性的成熟のタイミングを制御するのと同じ機能を持つであろう遺伝経路の引き金となる一群の遺伝子を同定した。コロンビア大学の科学者が率いるこの研究は、神経発達の性差における直接的な遺伝的影響についての新しい証拠を提供し、男性と女性の脳がどのように結びついているか、そしてそれらがどのように機能するかを理解しようとする試みである。この研究は、2019年1月1日にハワード・ヒューズ医学研究所、マックス・プランク研究所、およびウェルカム・トラストによって設立されたオープンアクセスジャーナルeLifeに掲載された。 この論文のタイトルは「性的二型神経系分化のタイミングメカニズム(Timing Mechanism of Sexually Dimorphic Nervous System Differentiation.)」と題されている。思春期はホルモンシグナルの生成でニューロンが活性化することにより特徴付けられる脳の実質的な変化であることを科学者たちは長い間知っていた。しかし、思春期になるホルモンを脳が放出し始める原因は捉えどころのないままであった。コロンビア生物学科の教授でハワード・ヒューズ医学研究所の研究者であるOliver Hobert博士は、次のように述べている。「驚くべきことに、この経路の各メンバーはワームとヒトの間で受け継がれていることが分かった。これは、脳における性的な脳の違いが遺伝的にどのようにコードされるかについての一般原則を明らかにしたことを示している。」この研究のために、研究者らはゲノム配列を決定した最初の多細胞生物である透明線虫C. elegansを利用した。 このワームの遺伝子構成はヒトのものと非常によく似ており、分子遺伝学および発生生物学における最も強力な研究モデルの1つである。
 成人の一定割合は白色脂肪組織だけでなく褐色脂肪組織も有している。この褐色脂肪組織は糖と脂肪を熱に変えるのを助ける。 褐色脂肪組織を持つ人は、冬に体温を調整するのが得意で、体重超過や糖尿病に苦しむ可能性が低いとされている。ETHチューリッヒのトランスレーショナル栄養生物学教授であるChristian Wolfrum博士が率いる国際的な研究チームは、スタチンクラスの医薬品が褐色脂肪組織の形成を減少させることを発見した。この論文は、2018年12月20日にCell Metabolismにオンライン掲載され、「タンパク質のプレニル化に影響を与えることによって、マウスおよび男性において脂肪細胞の褐変を防ぐメバロン酸経路の阻害(Inhibition of Mevalonate Pathway Prevents Adipocyte Browning in Mice and Men by Affecting Protein Prenylation.)」と題されている。スタチンは血液中のコレステロール値を下げ心臓発作の危険性を減らす目的で処方されている世界で最も一般的に処方されている薬の一つである。Wolfrum博士と彼の同僚は長年にわたり褐色脂肪組織を研究してきた。 彼らは、私たちの肌下脂肪層を形成する「悪い」白い脂肪細胞が、どのように「良い」褐色の脂肪細胞になるかという課題を調べた。 細胞培養実験を行った結果、彼らはコレステロールの生産に関与する生化学的経路がこの形質転換において中心的な役割を果たすことを発見した。 彼らはまた、変換を制御する重要な分子が代謝産物のゲラニルゲラニルピロリン酸であることを発見した。以前の研究は、コレステロールの生化学的経路もスタチンの機能の中心であることを示した。 それらの効果の1つは、ゲラニルゲラニルピロリン酸の産生を減少させることである。 スタチンが褐色脂肪組織の形成にも影響を与えるかどうかを研究者が知りたがったのはこのためだ。研究者たちがマウスや人間に関する研究で示しているように、実際にそのようなっている。
成人の一定割合は白色脂肪組織だけでなく褐色脂肪組織も有している。この褐色脂肪組織は糖と脂肪を熱に変えるのを助ける。 褐色脂肪組織を持つ人は、冬に体温を調整するのが得意で、体重超過や糖尿病に苦しむ可能性が低いとされている。ETHチューリッヒのトランスレーショナル栄養生物学教授であるChristian Wolfrum博士が率いる国際的な研究チームは、スタチンクラスの医薬品が褐色脂肪組織の形成を減少させることを発見した。この論文は、2018年12月20日にCell Metabolismにオンライン掲載され、「タンパク質のプレニル化に影響を与えることによって、マウスおよび男性において脂肪細胞の褐変を防ぐメバロン酸経路の阻害(Inhibition of Mevalonate Pathway Prevents Adipocyte Browning in Mice and Men by Affecting Protein Prenylation.)」と題されている。スタチンは血液中のコレステロール値を下げ心臓発作の危険性を減らす目的で処方されている世界で最も一般的に処方されている薬の一つである。Wolfrum博士と彼の同僚は長年にわたり褐色脂肪組織を研究してきた。 彼らは、私たちの肌下脂肪層を形成する「悪い」白い脂肪細胞が、どのように「良い」褐色の脂肪細胞になるかという課題を調べた。 細胞培養実験を行った結果、彼らはコレステロールの生産に関与する生化学的経路がこの形質転換において中心的な役割を果たすことを発見した。 彼らはまた、変換を制御する重要な分子が代謝産物のゲラニルゲラニルピロリン酸であることを発見した。以前の研究は、コレステロールの生化学的経路もスタチンの機能の中心であることを示した。 それらの効果の1つは、ゲラニルゲラニルピロリン酸の産生を減少させることである。 スタチンが褐色脂肪組織の形成にも影響を与えるかどうかを研究者が知りたがったのはこのためだ。研究者たちがマウスや人間に関する研究で示しているように、実際にそのようなっている。
 今年で10周年となるPrecision Medicine World Conference(PMWC)が、2019年1月20日から23日まで、約2,500人が参加してサンタクララコンベンションセンター(カリフォルニア州シリコンバレー)で開催される。この興味深い複数の関連分野の著名な専門家との集まりは、UCSF、スタンフォードヘルスケア/スタンフォード大学医学部、デューク大学、デュークヘルスとジョンズホプキンス大学によって共催される。
今年で10周年となるPrecision Medicine World Conference(PMWC)が、2019年1月20日から23日まで、約2,500人が参加してサンタクララコンベンションセンター(カリフォルニア州シリコンバレー)で開催される。この興味深い複数の関連分野の著名な専門家との集まりは、UCSF、スタンフォードヘルスケア/スタンフォード大学医学部、デューク大学、デュークヘルスとジョンズホプキンス大学によって共催される。
 学際的なアプローチにより、テキサス州のベイラー医科大学を含むいくつかの機関から成る国際研究チームは、人乳中のオリゴ糖とマイクロバイオームとの間の複雑な相互作用が新生児ロタウイルス感染に影響を及ぼすことを明らかにした。Nature Communications誌にオンラインで報告されたこの研究は、新生児におけるロタウイルス感染症についての新しい理解を提供し、生弱毒化ロタウイルスワクチンの性能を改善することができる母性成分の同定に役立つ。2018年11月27日に掲載されたこのオープンアクセスの論文は、「ヒト乳オリゴ糖、乳マイクロバイオームおよび乳児腸マイクロバイオームは新生児ロタウイルス感染を調節する(Human Milk Oligosaccharides, Milk Microbiome and Infant Gut Microbiome Modulate Neonatal Rotavirus Infection.)」と題されている。「ロタウイルス感染症は生後28日未満の子供を除き、主に5歳未満の子供に下痢と嘔吐を引き起こすが、通常は症状はない。しかし、新生児の感染症は深刻な胃腸障害に関連することがある。症状の有無にかかわらず、どの要因が新生児の違いを示すかははっきりと分かっていない。」とベイラー医科大学分子ウイルス学・微生物学の助教授で筆頭著者であるSasirekha Ramani博士(写真)は語った。「我々は何年も前にこの調査をロタウイルスの特定の株が新生児の無症候性感染症と臨床症状の両方に関連していることを決定するために開始した。」Ramani博士とその同僚は、ウイルスの観点から最初の答えを探し始めた。彼女らは、新生児のウイルス量やウイルスのゲノムなどの因子が新生児の症状の存在と関連しているかどうかを調査したが、それらの因子間に関連性は見いだされなかった。その後、新生児の観点から問いを投げかけた。 このウイルスが新生児に感染する理由と臨床症状に違いがある理由を説明できる他の要因はあるか?研究室では、研究者らは、母親の母乳成分がロタウイルス研究用に確立されたモデルであるMA104細胞の感染を、彼らがインドの新生児保育所で確認したロタウイルスの特定の株で抑制できるかどうか調べた。 意外なことに、母乳中に存在する特定の糖が新生児ロタウイルス株と培養中の細胞との感染を増強することを発見した。
学際的なアプローチにより、テキサス州のベイラー医科大学を含むいくつかの機関から成る国際研究チームは、人乳中のオリゴ糖とマイクロバイオームとの間の複雑な相互作用が新生児ロタウイルス感染に影響を及ぼすことを明らかにした。Nature Communications誌にオンラインで報告されたこの研究は、新生児におけるロタウイルス感染症についての新しい理解を提供し、生弱毒化ロタウイルスワクチンの性能を改善することができる母性成分の同定に役立つ。2018年11月27日に掲載されたこのオープンアクセスの論文は、「ヒト乳オリゴ糖、乳マイクロバイオームおよび乳児腸マイクロバイオームは新生児ロタウイルス感染を調節する(Human Milk Oligosaccharides, Milk Microbiome and Infant Gut Microbiome Modulate Neonatal Rotavirus Infection.)」と題されている。「ロタウイルス感染症は生後28日未満の子供を除き、主に5歳未満の子供に下痢と嘔吐を引き起こすが、通常は症状はない。しかし、新生児の感染症は深刻な胃腸障害に関連することがある。症状の有無にかかわらず、どの要因が新生児の違いを示すかははっきりと分かっていない。」とベイラー医科大学分子ウイルス学・微生物学の助教授で筆頭著者であるSasirekha Ramani博士(写真)は語った。「我々は何年も前にこの調査をロタウイルスの特定の株が新生児の無症候性感染症と臨床症状の両方に関連していることを決定するために開始した。」Ramani博士とその同僚は、ウイルスの観点から最初の答えを探し始めた。彼女らは、新生児のウイルス量やウイルスのゲノムなどの因子が新生児の症状の存在と関連しているかどうかを調査したが、それらの因子間に関連性は見いだされなかった。その後、新生児の観点から問いを投げかけた。 このウイルスが新生児に感染する理由と臨床症状に違いがある理由を説明できる他の要因はあるか?研究室では、研究者らは、母親の母乳成分がロタウイルス研究用に確立されたモデルであるMA104細胞の感染を、彼らがインドの新生児保育所で確認したロタウイルスの特定の株で抑制できるかどうか調べた。 意外なことに、母乳中に存在する特定の糖が新生児ロタウイルス株と培養中の細胞との感染を増強することを発見した。
 なぜ私たちは年を取るのか? 何世紀にも渡り研究されているが(そしてアンチエイジングは巨大な産業でもあるが)、年齢とともに細胞や臓器が劣化する要因はまだほとんど解っていない。一つ知られているファクターは温度である。多くの動物種は、より高い温度よりも低い温度でより長く生きる。
なぜ私たちは年を取るのか? 何世紀にも渡り研究されているが(そしてアンチエイジングは巨大な産業でもあるが)、年齢とともに細胞や臓器が劣化する要因はまだほとんど解っていない。一つ知られているファクターは温度である。多くの動物種は、より高い温度よりも低い温度でより長く生きる。
 スクリプス研究所の科学者は、原理上、癌および慢性ウイルス感染を治療するための標的にすることができる重要な免疫系調節タンパク質を発見した。2018年11月12日にNature Chemical Biologyに掲載されたこの研究では、脳と神経の宿主を特徴とする希少な遺伝病を引き起こすタンパク質ABHD12 (abhydrolase domain containing protein 12)の機能について特定している。
スクリプス研究所の科学者は、原理上、癌および慢性ウイルス感染を治療するための標的にすることができる重要な免疫系調節タンパク質を発見した。2018年11月12日にNature Chemical Biologyに掲載されたこの研究では、脳と神経の宿主を特徴とする希少な遺伝病を引き起こすタンパク質ABHD12 (abhydrolase domain containing protein 12)の機能について特定している。
 急性骨髄性白血病(AML)の患者に合わせた治療のために、白血病細胞の薬物感受性および耐性の迅速スクリーニングに進歩がみられている。 白血病幹細胞の薬物応答に関する研究は、治療が成功しなかった理由、または最初は有望な治療結果がなぜ持続しなかった理由を明らかにするかもしれない。 AMLは、ある種の血液形成細胞の重大な障害である。この病気では、白血球に通常発達する骨髄中の特定の初期前駆細胞が適切に成熟しない。 それらは芽球と呼ばれる原始細胞として凍結され、さらに分化し成熟することはできない。これらが蓄積し、低血球数を引き起こして感染症と戦う能力を低下させ、低血小板数は生命を脅かす出血のリスクを引き起こす。未成熟の癌性血液細胞の前駆細胞である白血病幹細胞は、AMLを増殖させ、また治療後の再発にも関与する。がんの研究者は、このデータが標準的な療法への抵抗の手がかりといくつかの患者が再発する理由に対する手掛かりとなる可能性があるため、この細胞集団で遺伝子がどのように発現するかに興味があった。サンディエゴの第60回米国血液学会(2018年12月1-4日)で発表されたこの研究では、AMLと診断された個々の患者から採取した幹細胞および芽細胞の薬物応答パターンを調べた。 この情報は、多くのサンプルをすばやく評価してテストする最先端の方法であるハイスループットスクリーニングによって収集された。
急性骨髄性白血病(AML)の患者に合わせた治療のために、白血病細胞の薬物感受性および耐性の迅速スクリーニングに進歩がみられている。 白血病幹細胞の薬物応答に関する研究は、治療が成功しなかった理由、または最初は有望な治療結果がなぜ持続しなかった理由を明らかにするかもしれない。 AMLは、ある種の血液形成細胞の重大な障害である。この病気では、白血球に通常発達する骨髄中の特定の初期前駆細胞が適切に成熟しない。 それらは芽球と呼ばれる原始細胞として凍結され、さらに分化し成熟することはできない。これらが蓄積し、低血球数を引き起こして感染症と戦う能力を低下させ、低血小板数は生命を脅かす出血のリスクを引き起こす。未成熟の癌性血液細胞の前駆細胞である白血病幹細胞は、AMLを増殖させ、また治療後の再発にも関与する。がんの研究者は、このデータが標準的な療法への抵抗の手がかりといくつかの患者が再発する理由に対する手掛かりとなる可能性があるため、この細胞集団で遺伝子がどのように発現するかに興味があった。サンディエゴの第60回米国血液学会(2018年12月1-4日)で発表されたこの研究では、AMLと診断された個々の患者から採取した幹細胞および芽細胞の薬物応答パターンを調べた。 この情報は、多くのサンプルをすばやく評価してテストする最先端の方法であるハイスループットスクリーニングによって収集された。
 ゲノムにおける相互作用は、何十億年も前の先進的な生命の発生の原動力の1つになった可能性がある。この発見は「ジャンピング遺伝子」として知られるレトロトランスポゾンへの好奇心がきっかけになった。ヒトゲノムのほぼ半分はレトロトランスポゾンで構成されているが、バクテリアにはほとんど存在しない。イリノイ大学アーバナシャンペーン校(UIUC)の物理学教授でありNASAアストロバイオロジー研究所のディレクターでもあるNigel Goldenfeld博士と、元UIUC(現在はカリフォルニア大)の物理学教授であるThomas Kuhlman博士らは、これがなぜなのか疑問に思っていた。「本当に単純に、自分のゲノムからレトロトランスポゾンを取り出し、それをバクテリアに入れて何が起こるか見てみたいと考えた。それは本当に興味深いことになった。」とKuhlman博士は語った。彼らの成果は2018年11月19日にPNASでオンライン公開され、数十億年前に高度な生命がどのように誕生したかの謎に迫っている。また、他の惑星の生命の可能性を判断するのにも役立つ。このオープンアクセスのPNASの論文のタイトルは、「祖先真核細胞の出現のためのレトロエレメント侵入仮説のテスト(Testing the Retroelement Invasion Hypothesis for the Emergence of the Ancestral Eukaryotic Cell.)」と題されている。
ゲノムにおける相互作用は、何十億年も前の先進的な生命の発生の原動力の1つになった可能性がある。この発見は「ジャンピング遺伝子」として知られるレトロトランスポゾンへの好奇心がきっかけになった。ヒトゲノムのほぼ半分はレトロトランスポゾンで構成されているが、バクテリアにはほとんど存在しない。イリノイ大学アーバナシャンペーン校(UIUC)の物理学教授でありNASAアストロバイオロジー研究所のディレクターでもあるNigel Goldenfeld博士と、元UIUC(現在はカリフォルニア大)の物理学教授であるThomas Kuhlman博士らは、これがなぜなのか疑問に思っていた。「本当に単純に、自分のゲノムからレトロトランスポゾンを取り出し、それをバクテリアに入れて何が起こるか見てみたいと考えた。それは本当に興味深いことになった。」とKuhlman博士は語った。彼らの成果は2018年11月19日にPNASでオンライン公開され、数十億年前に高度な生命がどのように誕生したかの謎に迫っている。また、他の惑星の生命の可能性を判断するのにも役立つ。このオープンアクセスのPNASの論文のタイトルは、「祖先真核細胞の出現のためのレトロエレメント侵入仮説のテスト(Testing the Retroelement Invasion Hypothesis for the Emergence of the Ancestral Eukaryotic Cell.)」と題されている。
 2018年の内分泌学学会年次大会(11月19-21日 イギリス・グラスゴー)で、若年マウスのストレスに起因する脳の発育の変化を予防することがアムステルダム大学の研究チームによって発表された。この研究成果は、栄養豊富な食事が、早期ストレスに曝された若いマウスの脳の発達に保護的効果をもたらし、後の学習および記憶障害を軽減することを示唆している。ヒトや動物において初期ストレスのような逆境への曝露は、脳機能に長期間影響を及ぼし、後の人生で認知障害を引き起こすことが報告されている。 出生直後の期間は脳の発達にとって重要であり、栄養素の需要は、エネルギーのためにも、発達する脳のための不可欠な構成要素である。したがって、この期間中の必須栄養素の欠損は、学習プロセスを含む脳機能の長期的な異常をもたらす可能性がある。身体のストレスと代謝過程は密接に関連しており、良質な栄養は早期のストレスに関連する認知障害を予防することができるが、これまで精力的に調査されて来なかった。
2018年の内分泌学学会年次大会(11月19-21日 イギリス・グラスゴー)で、若年マウスのストレスに起因する脳の発育の変化を予防することがアムステルダム大学の研究チームによって発表された。この研究成果は、栄養豊富な食事が、早期ストレスに曝された若いマウスの脳の発達に保護的効果をもたらし、後の学習および記憶障害を軽減することを示唆している。ヒトや動物において初期ストレスのような逆境への曝露は、脳機能に長期間影響を及ぼし、後の人生で認知障害を引き起こすことが報告されている。 出生直後の期間は脳の発達にとって重要であり、栄養素の需要は、エネルギーのためにも、発達する脳のための不可欠な構成要素である。したがって、この期間中の必須栄養素の欠損は、学習プロセスを含む脳機能の長期的な異常をもたらす可能性がある。身体のストレスと代謝過程は密接に関連しており、良質な栄養は早期のストレスに関連する認知障害を予防することができるが、これまで精力的に調査されて来なかった。
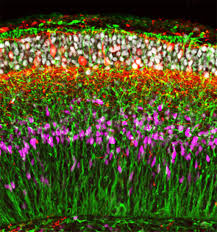 イェール大学医学部とイタリアのピサ大学の生物学科のチームは、動物モデルで脊髄損傷の修復に特に効果的である特定の幹細胞集団(神経上皮幹細胞)を同定した。この実験では、これらの細胞が損傷組織内に組み込まれ、移植後に数センチメートルのプロセスを延長し、治療を受けた動物に運動機能回復をもたらすことを実証した。さらに、ラボの試験で示されているように、回復は傷害の程度に比例した。
イェール大学医学部とイタリアのピサ大学の生物学科のチームは、動物モデルで脊髄損傷の修復に特に効果的である特定の幹細胞集団(神経上皮幹細胞)を同定した。この実験では、これらの細胞が損傷組織内に組み込まれ、移植後に数センチメートルのプロセスを延長し、治療を受けた動物に運動機能回復をもたらすことを実証した。さらに、ラボの試験で示されているように、回復は傷害の程度に比例した。
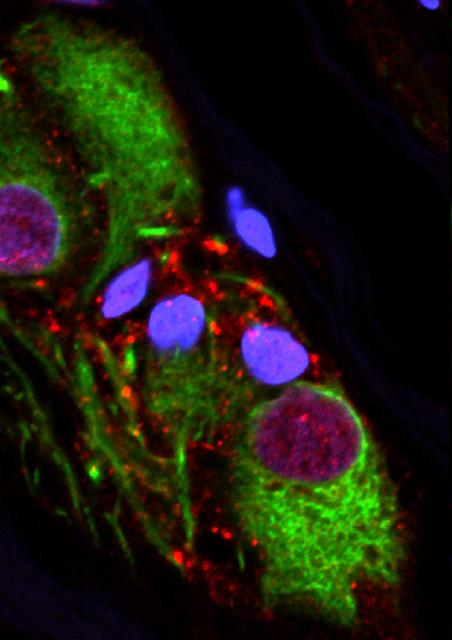 虫垂の切除は、パーキンソン病の発症リスクを19〜25%低下させる可能性があることが2018年10月31日発行のScience Translational Medicineに掲載された。このオープンアクセスの論文は、「虫垂がパーキンソン病を発症するリスクに影響する(The Vermiform Appendix Impacts the Risk of Developing Parkinson’s Disease.)」と題されている。この発見はまた、パーキンソン病の発生における腸および免疫系の役割を明確にし、パーキンソン病の発症および進行と密接に関連している異常に折り畳まれたα-シヌクレインタンパク質の主要リザーバーとして機能することを明らかにした。「我々の結果は、パーキンソン病の原因部位としての虫垂を指し、この病気の発症における胃腸管の役割を活用する新しい治療戦略を考案するための道筋を提供している。大部分が不必要であるという評判があるにもかかわらず、虫垂は実際に我々の免疫系の主要部分であり、私たちの腸内細菌の構成を調節し、今度はパーキンソン病における役割も我々の研究で示された。」とViviane Labrie 研究所(VARI)の助教授であり論文のシニア著者であるVan Andel博士は語った。パーキンソン病のリスクの低下は、パーキンソン病の発症の数年前に、虫垂およびその中に含まれるα-シヌクレインが、早期に取り除かれたときにのみ明らかであり、虫垂が疾患の開始に関与する可能性があることを示唆している。 しかしながら、疾患プロセスが開始した後の虫垂の除去は、疾患の進行に影響を及ぼさなかった。 一般の集団では、虫垂切除術を受けた人々は、パーキンソン病を発症する可能性が19%低くなった。 この効果は農村部に住む人々に特に顕著で、虫垂切除術により疾患リスクが25%低下した。 パーキンソン病は、しばしば農村集団においてより一般的であり、農薬への曝露の増加に関連している傾向がある。
虫垂の切除は、パーキンソン病の発症リスクを19〜25%低下させる可能性があることが2018年10月31日発行のScience Translational Medicineに掲載された。このオープンアクセスの論文は、「虫垂がパーキンソン病を発症するリスクに影響する(The Vermiform Appendix Impacts the Risk of Developing Parkinson’s Disease.)」と題されている。この発見はまた、パーキンソン病の発生における腸および免疫系の役割を明確にし、パーキンソン病の発症および進行と密接に関連している異常に折り畳まれたα-シヌクレインタンパク質の主要リザーバーとして機能することを明らかにした。「我々の結果は、パーキンソン病の原因部位としての虫垂を指し、この病気の発症における胃腸管の役割を活用する新しい治療戦略を考案するための道筋を提供している。大部分が不必要であるという評判があるにもかかわらず、虫垂は実際に我々の免疫系の主要部分であり、私たちの腸内細菌の構成を調節し、今度はパーキンソン病における役割も我々の研究で示された。」とViviane Labrie 研究所(VARI)の助教授であり論文のシニア著者であるVan Andel博士は語った。パーキンソン病のリスクの低下は、パーキンソン病の発症の数年前に、虫垂およびその中に含まれるα-シヌクレインが、早期に取り除かれたときにのみ明らかであり、虫垂が疾患の開始に関与する可能性があることを示唆している。 しかしながら、疾患プロセスが開始した後の虫垂の除去は、疾患の進行に影響を及ぼさなかった。 一般の集団では、虫垂切除術を受けた人々は、パーキンソン病を発症する可能性が19%低くなった。 この効果は農村部に住む人々に特に顕著で、虫垂切除術により疾患リスクが25%低下した。 パーキンソン病は、しばしば農村集団においてより一般的であり、農薬への曝露の増加に関連している傾向がある。
 2018年10月16-20日にカリフォルニア州サンディエゴで開催されたアメリカ人類遺伝学会年次総会(ASHG2018)で、ペルー・アンデス山脈の古代人は、高所への環境と農業の導入に他の世界の人々とは異なる方法で適応したことが発表された。ASHGは今年の会議で記録的な出席者8,500人を報告している。
2018年10月16-20日にカリフォルニア州サンディエゴで開催されたアメリカ人類遺伝学会年次総会(ASHG2018)で、ペルー・アンデス山脈の古代人は、高所への環境と農業の導入に他の世界の人々とは異なる方法で適応したことが発表された。ASHGは今年の会議で記録的な出席者8,500人を報告している。
 遺伝子解析の新しいアプローチは、環境因子とpharmacogene(薬物に反応するヒト遺伝子)の関連性を見出した。これは、集団遺伝学と医薬の境界で新しい研究のための発想を呼び起こすものである。米国人類遺伝学会(ASHG)2018年次会合で発表されたこの内容について、「人間は数世紀に渡って医薬品を開発し、使用してきたが、それらの遺伝子は独自に機能しており、それ以前から他の環境要因と相互作用していた」とコロラド大学のChris Gignoux博士(写真)は語った。この要旨は「薬理ゲノム変異の世界的景観(The Global Landscape of Pharmacogenomic Variation.)」と題されている。物理的環境の変化と同様に、薬物は体内の微小環境に影響を及ぼし、その細胞と遺伝子の働きを変える。 このことは、薬理ゲノムとの関連性を有する遺伝子が、遺伝学と環境とのより広い相関を研究する上でも有用であり得ることを示唆している。さまざまな環境要因を探るために、Gignoux博士はスタンフォード大学のElena Sorokin博士と協力し、NASA、世界自然保護基金などのデータを使用して、20以上の気候、地理、生態学的変数のジオコード化されたリソースを作成した。米国の共同研究者らは、ゲノミックスと疫学(PAGE: Population Architecture using Genomics and Epidemiology)研究を用い、99の世界人口から51,698人の臨床的および疫学的に関連するバリエーションのサンプルを調査する大きなイニシアチブである。新しい分析手法は、Enviro-WAS(environment-wide association study)と呼ばれ、遺伝子型と20の環境変数との間の関連性を同定するために19,690の薬理ゲノム関連変異体を調べた。
遺伝子解析の新しいアプローチは、環境因子とpharmacogene(薬物に反応するヒト遺伝子)の関連性を見出した。これは、集団遺伝学と医薬の境界で新しい研究のための発想を呼び起こすものである。米国人類遺伝学会(ASHG)2018年次会合で発表されたこの内容について、「人間は数世紀に渡って医薬品を開発し、使用してきたが、それらの遺伝子は独自に機能しており、それ以前から他の環境要因と相互作用していた」とコロラド大学のChris Gignoux博士(写真)は語った。この要旨は「薬理ゲノム変異の世界的景観(The Global Landscape of Pharmacogenomic Variation.)」と題されている。物理的環境の変化と同様に、薬物は体内の微小環境に影響を及ぼし、その細胞と遺伝子の働きを変える。 このことは、薬理ゲノムとの関連性を有する遺伝子が、遺伝学と環境とのより広い相関を研究する上でも有用であり得ることを示唆している。さまざまな環境要因を探るために、Gignoux博士はスタンフォード大学のElena Sorokin博士と協力し、NASA、世界自然保護基金などのデータを使用して、20以上の気候、地理、生態学的変数のジオコード化されたリソースを作成した。米国の共同研究者らは、ゲノミックスと疫学(PAGE: Population Architecture using Genomics and Epidemiology)研究を用い、99の世界人口から51,698人の臨床的および疫学的に関連するバリエーションのサンプルを調査する大きなイニシアチブである。新しい分析手法は、Enviro-WAS(environment-wide association study)と呼ばれ、遺伝子型と20の環境変数との間の関連性を同定するために19,690の薬理ゲノム関連変異体を調べた。
 一般的に使用されている抗精神病薬は、治療が最も困難なトリプルネガティブ乳癌に対しても有効であるという新たな研究が発表された。英国のブラッドフォード大学が率いるこの研究では、ピモジド(pimozide)がトリプルネガティブ乳癌の他、最も一般的なタイプの肺がんをも治療できる可能性があることが示された。
一般的に使用されている抗精神病薬は、治療が最も困難なトリプルネガティブ乳癌に対しても有効であるという新たな研究が発表された。英国のブラッドフォード大学が率いるこの研究では、ピモジド(pimozide)がトリプルネガティブ乳癌の他、最も一般的なタイプの肺がんをも治療できる可能性があることが示された。
 英国のエクセター大学の科学者たちは、身体の特定の部位に薬物を運ぶことによって疾患の治療に革命を起こす可能性のある、精子細胞を模倣した小型の磁気スイミング装置を作製した。長さが1ミリメートルのこの小型デバイスは、磁気ヘッドとフレキシブルテールで構成されており、磁場によって活性化されると特定の位置に「泳ぐ」ことができる。
英国のエクセター大学の科学者たちは、身体の特定の部位に薬物を運ぶことによって疾患の治療に革命を起こす可能性のある、精子細胞を模倣した小型の磁気スイミング装置を作製した。長さが1ミリメートルのこの小型デバイスは、磁気ヘッドとフレキシブルテールで構成されており、磁場によって活性化されると特定の位置に「泳ぐ」ことができる。
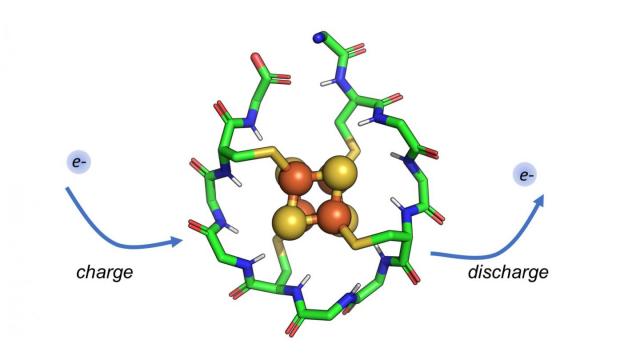 地球上で生命はどのように起こったのか?ニュージャージー州のラトガース大学の研究者は、単純なタンパク質触媒の最初で唯一の証拠の中に、細胞に不可欠な、生命が始まったときに存在していたかもしれない生命のビルディングブロックを発見した。この原始のペプチドまたは小さなタンパク質の研究が、米国化学会誌に掲載された。
地球上で生命はどのように起こったのか?ニュージャージー州のラトガース大学の研究者は、単純なタンパク質触媒の最初で唯一の証拠の中に、細胞に不可欠な、生命が始まったときに存在していたかもしれない生命のビルディングブロックを発見した。この原始のペプチドまたは小さなタンパク質の研究が、米国化学会誌に掲載された。
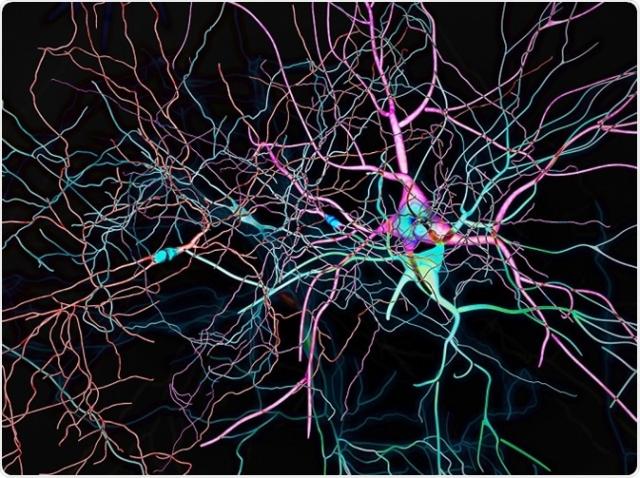 2018年8月29日にサイエンスのオンラインで公開された新研究で、非小細胞肺癌(NSCLC)での遺伝子変異は、細胞の主要な増殖シグナルの認識を妨げて、腫瘍形成を促進する可能性があると報告された。この論文は、「癌突然変異と標的薬物は、Ras-Erk経路によるダイナミックシグナルエンコーディングを混乱させる可能性がある(Cancer Mutations and Targeted Drugs Can Disrupt Dynamic Signal Encoding by the Ras-Erk Pathway.)」と題されている。カリフォルニア大学サンフランシスコ校(UCSF)の研究者が率いるこの研究は、多くのヒト癌の根底にある欠陥メカニズムを理解し、欠陥メカニズムを最終標的とする重要な意味を持つ可能性がある。健常細胞は、いつ、どのように増殖、分裂、および移動するかについて外部の手がかりを解釈するために、Ras / Erk増殖シグナル伝達経路(Ras / MAPK経路)に依存するが、これらのメッセージが伝達される際の欠陥は、 制御不能に陥り、身体の他の部分へ浸潤する原因となりうる。このような突然変異は、大多数のヒト癌で発見され、Ras / Erkの治療法を開発は、癌研究の至高の目標である。何十年もの研究により、科学者は、突然変異により経路の1つ以上のコンポーネントが成長前の状態から抜け出せなくなった場合に、Ras / Erkによる癌が生じると考えている。研究者らは、これらの壊れたスイッチを元に戻す標的治療法を開発するために努力してきたが、これまでのところほとんどが臨床試験に失敗している。現在、光パルスを用いてRas / Erkシグナル伝達を制御し、ゲノム動態を迅速に読み取ることが可能なUCSFで開発されたハイスループット技術を用い、この広範囲に研究された経路について驚くべき発見をした。オプトジェネティックス(Optogenetics:光感受性タンパク質が光パルスに応答するように細胞内で遺伝子操作されるアプローチ)は、神経科学における革新的な実験技術であり、研究者はニューロンのネットワーク内の電気活動パターンを精緻に制御し研究することができる。同じアプローチを使用することによって個々の細胞内の化学伝達パターンを探索する新しいUCSFの研究は、いくつかのRas / Erk突然変異が、細胞増殖シグナルの強度よりむしろタイミングを変えることによって癌を引き起こすことを明らかにした。 シグナルタイミングのこのぼやけが、欠陥Ras / Erkシグナル伝達を遮断するように設計された一部の標的薬物が逆説的に経路を活性化し、潜在的に新しい腫瘍形成のリスクを高める理由も示された。「この新しい技術は疾患細胞に接続する診断装置のようなもので、多くの光に基づく刺激で細胞を刺激して調べ、それがどのように反応するか見ることができる。」「このアプローチを使用することで、細胞回路によって通常はフィルタリングされたシグナルに応答して細胞増殖につながるシグナル、すなわち振る舞いを処理する方法において、ある欠陥を有する癌細胞を同定することができた。」と論文著者の1人であるUCSF合成生物学者のWendell Lim博士は語った。UCSFの医学腫瘍専門医および癌生物学者であるTrever Bivona博士、プリンストンの分子生物学者Jared Toettcher博士(元Lim研究室のポスドク研究員)は、この新研究の共著者である。 この研究の筆頭著者は、ペンシルバニア大学のLukasz Bugaj博士であり、以前はLim博士のポスドク研究者であった。
2018年8月29日にサイエンスのオンラインで公開された新研究で、非小細胞肺癌(NSCLC)での遺伝子変異は、細胞の主要な増殖シグナルの認識を妨げて、腫瘍形成を促進する可能性があると報告された。この論文は、「癌突然変異と標的薬物は、Ras-Erk経路によるダイナミックシグナルエンコーディングを混乱させる可能性がある(Cancer Mutations and Targeted Drugs Can Disrupt Dynamic Signal Encoding by the Ras-Erk Pathway.)」と題されている。カリフォルニア大学サンフランシスコ校(UCSF)の研究者が率いるこの研究は、多くのヒト癌の根底にある欠陥メカニズムを理解し、欠陥メカニズムを最終標的とする重要な意味を持つ可能性がある。健常細胞は、いつ、どのように増殖、分裂、および移動するかについて外部の手がかりを解釈するために、Ras / Erk増殖シグナル伝達経路(Ras / MAPK経路)に依存するが、これらのメッセージが伝達される際の欠陥は、 制御不能に陥り、身体の他の部分へ浸潤する原因となりうる。このような突然変異は、大多数のヒト癌で発見され、Ras / Erkの治療法を開発は、癌研究の至高の目標である。何十年もの研究により、科学者は、突然変異により経路の1つ以上のコンポーネントが成長前の状態から抜け出せなくなった場合に、Ras / Erkによる癌が生じると考えている。研究者らは、これらの壊れたスイッチを元に戻す標的治療法を開発するために努力してきたが、これまでのところほとんどが臨床試験に失敗している。現在、光パルスを用いてRas / Erkシグナル伝達を制御し、ゲノム動態を迅速に読み取ることが可能なUCSFで開発されたハイスループット技術を用い、この広範囲に研究された経路について驚くべき発見をした。オプトジェネティックス(Optogenetics:光感受性タンパク質が光パルスに応答するように細胞内で遺伝子操作されるアプローチ)は、神経科学における革新的な実験技術であり、研究者はニューロンのネットワーク内の電気活動パターンを精緻に制御し研究することができる。同じアプローチを使用することによって個々の細胞内の化学伝達パターンを探索する新しいUCSFの研究は、いくつかのRas / Erk突然変異が、細胞増殖シグナルの強度よりむしろタイミングを変えることによって癌を引き起こすことを明らかにした。 シグナルタイミングのこのぼやけが、欠陥Ras / Erkシグナル伝達を遮断するように設計された一部の標的薬物が逆説的に経路を活性化し、潜在的に新しい腫瘍形成のリスクを高める理由も示された。「この新しい技術は疾患細胞に接続する診断装置のようなもので、多くの光に基づく刺激で細胞を刺激して調べ、それがどのように反応するか見ることができる。」「このアプローチを使用することで、細胞回路によって通常はフィルタリングされたシグナルに応答して細胞増殖につながるシグナル、すなわち振る舞いを処理する方法において、ある欠陥を有する癌細胞を同定することができた。」と論文著者の1人であるUCSF合成生物学者のWendell Lim博士は語った。UCSFの医学腫瘍専門医および癌生物学者であるTrever Bivona博士、プリンストンの分子生物学者Jared Toettcher博士(元Lim研究室のポスドク研究員)は、この新研究の共著者である。 この研究の筆頭著者は、ペンシルバニア大学のLukasz Bugaj博士であり、以前はLim博士のポスドク研究者であった。
 科学者は、ケシゲノムのDNA配列を決定し、生薬の製造に使用される薬学的化合物を生産するために植物がどのように進化したかを明らかにした。この発見は、科学者が薬草植物の収量および耐病性を向上させ、鎮痛および緩和ケアのための最も効果的な薬剤の信頼できる安価な供給を確保する道を開くかもしれない。ヨーク大学の研究者たちは、英国のウェルカム・サンガー・インスティテュート、および国際的な協力により、咳抑制薬ノスカピンおよび鎮痛薬モルヒネおよびコデインの生産につながる遺伝的経路の起源を明らかにした。この研究は2018年8月30日にScienceでオンラインで報告された。 この論文は、「ケシのゲノムとモルフィナン生産(The Opium Poppy Genome and Morphinan Production.)」と題されている。共同執筆者であるヨーク大学の生物学科の新農産物センターのIan Graham教授は「生化学者は植物がどのように進化して地球上で最も豊富な化学物質リソースになったか長年関心があった。高品質のゲノムアセンブリを使用して、我々は、これがケシにおいてどのように起こったかを解明した。同時に、この研究は、途上国において痛みの緩和と緩和ケアのために利用可能な最も有効な鎮痛剤の信頼できる安価な供給が確保されるために分子植物育種ツールの開発の基盤を提供するだろう。」と語った。ノスカピン、コデイン、およびモルヒネなどの合成化合物を製造するための合成生物学ベースのアプローチが開発されており、植物由来の遺伝子を工業用発酵槽で生産可能にするために酵母などの微生物系に改変されている。しかし、ケシは、これらの製薬化合物の最も安価で唯一の商業的供給源であり続けている。
科学者は、ケシゲノムのDNA配列を決定し、生薬の製造に使用される薬学的化合物を生産するために植物がどのように進化したかを明らかにした。この発見は、科学者が薬草植物の収量および耐病性を向上させ、鎮痛および緩和ケアのための最も効果的な薬剤の信頼できる安価な供給を確保する道を開くかもしれない。ヨーク大学の研究者たちは、英国のウェルカム・サンガー・インスティテュート、および国際的な協力により、咳抑制薬ノスカピンおよび鎮痛薬モルヒネおよびコデインの生産につながる遺伝的経路の起源を明らかにした。この研究は2018年8月30日にScienceでオンラインで報告された。 この論文は、「ケシのゲノムとモルフィナン生産(The Opium Poppy Genome and Morphinan Production.)」と題されている。共同執筆者であるヨーク大学の生物学科の新農産物センターのIan Graham教授は「生化学者は植物がどのように進化して地球上で最も豊富な化学物質リソースになったか長年関心があった。高品質のゲノムアセンブリを使用して、我々は、これがケシにおいてどのように起こったかを解明した。同時に、この研究は、途上国において痛みの緩和と緩和ケアのために利用可能な最も有効な鎮痛剤の信頼できる安価な供給が確保されるために分子植物育種ツールの開発の基盤を提供するだろう。」と語った。ノスカピン、コデイン、およびモルヒネなどの合成化合物を製造するための合成生物学ベースのアプローチが開発されており、植物由来の遺伝子を工業用発酵槽で生産可能にするために酵母などの微生物系に改変されている。しかし、ケシは、これらの製薬化合物の最も安価で唯一の商業的供給源であり続けている。
 遺伝子FKBP5は、ストレス応答の重要な調節因子であり、我々がどのように環境刺激に応答するかに影響する。以前の研究では、この遺伝子の特定の変異体が、外傷後ストレス障害、うつ病、自殺リスクおよび攻撃的行動などの神経精神障害の発症において役割を果たすことが示されている。しかし、2013年にノースカロライナ大学(UNC)医学部の研究者らが、FKBP5の遺伝子変異と外傷後慢性疼痛との関連を初めて示した。特に、rs3800373として知られている第6染色体の変異型または軽症/リスクアレルを持つ人々は、この亜種を持たない人と比較して外傷(性的暴行または自動車衝突など)に曝された後により多くの痛みを経験する可能性があることが判明した。現在、Journal of Neuroscienceに掲載された同じ研究グループによる新しい研究では、自動車衝突の外傷を経験した1,500人以上の欧州アメリカ人およびアフリカ系アメリカ人の子孫のコホートにおいてこの関連が確認されている。 外傷修復研究所の麻酔科の助教授Sarah Linnstaedt博士(写真)がこの研究の筆頭著者である。この論文は「FKBP5の3'UTR中の機能性riboSNitchはMicroRNA-320a結合効率を変え、慢性外傷後疼痛の脆弱性を介在する(A Functional riboSNitch in the 3′UTR of FKBP5 Alters MicroRNA-320a Binding Efficiency and Mediates Vulnerability to Chronic Posttraumatic Pain.)」と題されている。
遺伝子FKBP5は、ストレス応答の重要な調節因子であり、我々がどのように環境刺激に応答するかに影響する。以前の研究では、この遺伝子の特定の変異体が、外傷後ストレス障害、うつ病、自殺リスクおよび攻撃的行動などの神経精神障害の発症において役割を果たすことが示されている。しかし、2013年にノースカロライナ大学(UNC)医学部の研究者らが、FKBP5の遺伝子変異と外傷後慢性疼痛との関連を初めて示した。特に、rs3800373として知られている第6染色体の変異型または軽症/リスクアレルを持つ人々は、この亜種を持たない人と比較して外傷(性的暴行または自動車衝突など)に曝された後により多くの痛みを経験する可能性があることが判明した。現在、Journal of Neuroscienceに掲載された同じ研究グループによる新しい研究では、自動車衝突の外傷を経験した1,500人以上の欧州アメリカ人およびアフリカ系アメリカ人の子孫のコホートにおいてこの関連が確認されている。 外傷修復研究所の麻酔科の助教授Sarah Linnstaedt博士(写真)がこの研究の筆頭著者である。この論文は「FKBP5の3'UTR中の機能性riboSNitchはMicroRNA-320a結合効率を変え、慢性外傷後疼痛の脆弱性を介在する(A Functional riboSNitch in the 3′UTR of FKBP5 Alters MicroRNA-320a Binding Efficiency and Mediates Vulnerability to Chronic Posttraumatic Pain.)」と題されている。
 テキサス大学(UT)の科学者によって、初めて大型哺乳動物(犬)のデュシェンヌ型筋ジストロフィー(DMD)の進行を停止させるためにCRISPR遺伝子編集が使用され、救命の可能性が示された。2018年8月30日にサイエンスでオンラインで公開されたこの研究では、筋機能に重要なタンパク質であるジストロフィンの産生を阻害する突然変異によって引き起こされ、小児の最も一般的な致死的遺伝病であるDMDを有する犬の筋繊維に前例のない改善があったとしている。この論文は、「遺伝子編集はデュシェンヌ型筋ジストロフィーのイヌモデルにおけるジストロフィン発現を回復させる(Gene Editing Restores Dystrophin Expression in a Canine Model Of Duchenne Muscular Dystrophy.)」と題されている。研究では、筋肉や心臓組織のジストロフィンを正常レベルの92%まで回復させるために、シングルカット遺伝子編集技術を使用した。科学者は、患者を有意に助けるのに15%の閾値が必要であると推定している。「DMDを患う子供たちは、心臓が鼓動する力が失われたり、横隔膜が息をするには弱すぎたりするため、しばしば死亡する。このレベルのジストロフィン発現なら、うまくいけばそれが起こらないようにするだろう。」とUTサウスウエスタンのハモン再生医科学センターのEric Olson博士は語った。5,000人の少年のうちの1人に影響を及ぼすDMDは、筋肉および心不全に至り、30代前半で早死を引き起こす。患者は、筋肉が退化して車椅子に乗せられることになり、最終的には横隔膜が弱くなるにつれて呼吸器が着けられる。効果的な治療は存在しないが、科学者はジストロフィン遺伝子の欠損がその状態を引き起こすことを何十年も前に分かっていた。サイエンスに発表されたこの研究は、ジストロフィー筋肉におけるシングルカット遺伝子編集のコンセプトを実証し、臨床試験への大きな一歩を象徴している。
テキサス大学(UT)の科学者によって、初めて大型哺乳動物(犬)のデュシェンヌ型筋ジストロフィー(DMD)の進行を停止させるためにCRISPR遺伝子編集が使用され、救命の可能性が示された。2018年8月30日にサイエンスでオンラインで公開されたこの研究では、筋機能に重要なタンパク質であるジストロフィンの産生を阻害する突然変異によって引き起こされ、小児の最も一般的な致死的遺伝病であるDMDを有する犬の筋繊維に前例のない改善があったとしている。この論文は、「遺伝子編集はデュシェンヌ型筋ジストロフィーのイヌモデルにおけるジストロフィン発現を回復させる(Gene Editing Restores Dystrophin Expression in a Canine Model Of Duchenne Muscular Dystrophy.)」と題されている。研究では、筋肉や心臓組織のジストロフィンを正常レベルの92%まで回復させるために、シングルカット遺伝子編集技術を使用した。科学者は、患者を有意に助けるのに15%の閾値が必要であると推定している。「DMDを患う子供たちは、心臓が鼓動する力が失われたり、横隔膜が息をするには弱すぎたりするため、しばしば死亡する。このレベルのジストロフィン発現なら、うまくいけばそれが起こらないようにするだろう。」とUTサウスウエスタンのハモン再生医科学センターのEric Olson博士は語った。5,000人の少年のうちの1人に影響を及ぼすDMDは、筋肉および心不全に至り、30代前半で早死を引き起こす。患者は、筋肉が退化して車椅子に乗せられることになり、最終的には横隔膜が弱くなるにつれて呼吸器が着けられる。効果的な治療は存在しないが、科学者はジストロフィン遺伝子の欠損がその状態を引き起こすことを何十年も前に分かっていた。サイエンスに発表されたこの研究は、ジストロフィー筋肉におけるシングルカット遺伝子編集のコンセプトを実証し、臨床試験への大きな一歩を象徴している。
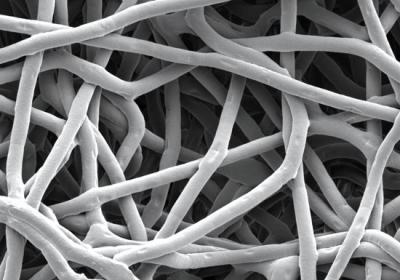 スコットランドのエジンバラ大学の再生医学研究センター(MRC)の科学者によって3Dヒト肝臓組織に形質転換された幹細胞は、肝臓疾患のマウスに移植された際に肝機能の有望なサポートをした。科学者は、ヒト肝臓組織インプラントを開発するための初期段階の進歩に加えて、実験室でのヒト肝臓疾患および試験薬の研究のためのより良いプラットフォームを提供することによって、実験動物の必要性を低減できるとも述べている。この研究はArchives of Toxicologyに掲載された。科学者はヒト胚性幹細胞を採取して人工多能性幹細胞(iPSCs)を誘導し、慎重にそれらを刺激して肝細胞の特性を発達させた。研究者らは、これらの細胞を1年以上にわたりディッシュの中の小さな塊として成長させた。この研究を主導したエジンバラ大学の再生医療センターMRCのDavid Hay博士は、「研究室で幹細胞由来の肝臓組織を1年以上生存させたのは、これが初めてだ。 長い間細胞を生きて安定した肝細胞として維持することは非常に難しいが、人にこの技術を応用することを望むなら、非常に重要なステップである。」と述べた。科学者は3Dの足場を開発するため、ヒトで既に承認された適切なポリマーを特定するために材料化学者および技術者と協力した。
スコットランドのエジンバラ大学の再生医学研究センター(MRC)の科学者によって3Dヒト肝臓組織に形質転換された幹細胞は、肝臓疾患のマウスに移植された際に肝機能の有望なサポートをした。科学者は、ヒト肝臓組織インプラントを開発するための初期段階の進歩に加えて、実験室でのヒト肝臓疾患および試験薬の研究のためのより良いプラットフォームを提供することによって、実験動物の必要性を低減できるとも述べている。この研究はArchives of Toxicologyに掲載された。科学者はヒト胚性幹細胞を採取して人工多能性幹細胞(iPSCs)を誘導し、慎重にそれらを刺激して肝細胞の特性を発達させた。研究者らは、これらの細胞を1年以上にわたりディッシュの中の小さな塊として成長させた。この研究を主導したエジンバラ大学の再生医療センターMRCのDavid Hay博士は、「研究室で幹細胞由来の肝臓組織を1年以上生存させたのは、これが初めてだ。 長い間細胞を生きて安定した肝細胞として維持することは非常に難しいが、人にこの技術を応用することを望むなら、非常に重要なステップである。」と述べた。科学者は3Dの足場を開発するため、ヒトで既に承認された適切なポリマーを特定するために材料化学者および技術者と協力した。
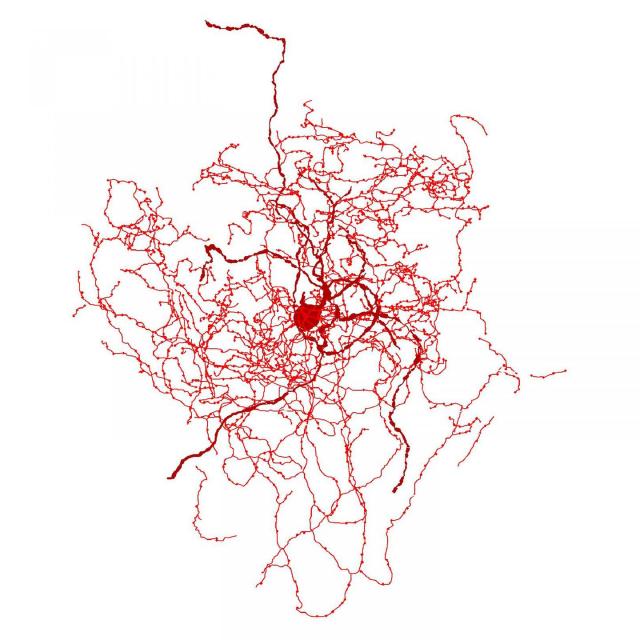 人間の脳に関する最も興味深い疑問は「私たちの脳を他の動物の脳と区別するのは何か?」であり、これは神経科学者にとって答えるのが最も難しい質問の1つである。「人間の脳を特別なものにするのは何か本当のところ分からない」とワシントン州シアトルにあるアレン脳科学研究所のEd Lein博士は述べている。「細胞と回路のレベルで違いを学ぶことはスタート地点としては適しており、今や我々はそれを行う新しいツールを持っている」2018年8月27日にNature Neuroscienceでオンラインで公開されたこの新研究で、Lein博士とその同僚は、この難しい疑問に対する可能性のある答えを発表した。この論文は、「特殊化されたヒト皮質ガバレクチン細胞型のトランスクリプトームおよび形態生理学的証拠(Transcriptomic and Morphophysiological Evidence for a Specialized Human Cortical Gabaergic Cell Type.)」と題されている。Lein博士とハンガリーのセゲド大学の神経科学者であるGábor Tamás博士の共同研究チームは、マウスや他のよく研究された実験動物では見られなかった新しいタイプのヒト脳細胞を発見した。Tamás博士とセゲド大学の博士課程学生であるEszter Boldogは、これらの新しい細胞を "ローズヒップニューロン"と呼んだ。なぜなら、細胞の中心の周りの各脳細胞の軸索形態が花弁をはずした後のバラのように見えるからだ。
人間の脳に関する最も興味深い疑問は「私たちの脳を他の動物の脳と区別するのは何か?」であり、これは神経科学者にとって答えるのが最も難しい質問の1つである。「人間の脳を特別なものにするのは何か本当のところ分からない」とワシントン州シアトルにあるアレン脳科学研究所のEd Lein博士は述べている。「細胞と回路のレベルで違いを学ぶことはスタート地点としては適しており、今や我々はそれを行う新しいツールを持っている」2018年8月27日にNature Neuroscienceでオンラインで公開されたこの新研究で、Lein博士とその同僚は、この難しい疑問に対する可能性のある答えを発表した。この論文は、「特殊化されたヒト皮質ガバレクチン細胞型のトランスクリプトームおよび形態生理学的証拠(Transcriptomic and Morphophysiological Evidence for a Specialized Human Cortical Gabaergic Cell Type.)」と題されている。Lein博士とハンガリーのセゲド大学の神経科学者であるGábor Tamás博士の共同研究チームは、マウスや他のよく研究された実験動物では見られなかった新しいタイプのヒト脳細胞を発見した。Tamás博士とセゲド大学の博士課程学生であるEszter Boldogは、これらの新しい細胞を "ローズヒップニューロン"と呼んだ。なぜなら、細胞の中心の周りの各脳細胞の軸索形態が花弁をはずした後のバラのように見えるからだ。
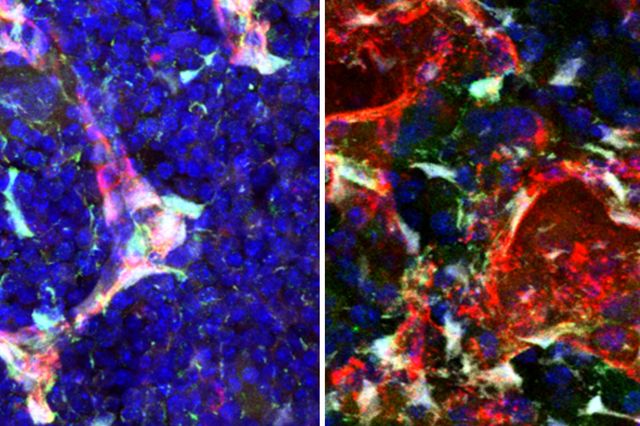 カリフォルニア州のUCLA ジョンソン総合がんセンターは、健常時および傷害後の微小環境によって造血幹細胞がどのように維持されているか重要な違いを発見した。人体は、健常時や、例えば癌の放射線治療のようなストレスやけがの時に単一成長因子を産生する細胞種を切り替えているように思われる。この研究結果は、放射線治療で造血幹細胞が実質的に枯渇していそうな時や、骨髄移植を受けている人の治療に影響を及ぼす可能性がある。この研究は、UCLAのデーヴィッドゲフェン医学部 血液学・腫瘍学の教授であるJohn Chute博士が率いたもので、Cell Stem Cellで発表された。この論文は、「プレオトロフィン制御造血幹細胞の維持および再生の骨髄源(Distinct Bone Marrow Sources of Pleiotrophin Control Hematopoietic Stem Cell Maintenance and Regeneration)」と題されている。血液形成または造血幹細胞は、白血球、赤血球および血小板などの様々な種類の成熟血液要素に分化することができる。それらは、様々なタイプの周囲の細胞が取り囲む骨髄中の「血管性ニッチ」に生存し、部分的には成長因子と呼ばれる化合物を分泌する。このUCLAの研究は、プレオトロフィン(PTN)と呼ばれる成長因子に焦点を当てている。
カリフォルニア州のUCLA ジョンソン総合がんセンターは、健常時および傷害後の微小環境によって造血幹細胞がどのように維持されているか重要な違いを発見した。人体は、健常時や、例えば癌の放射線治療のようなストレスやけがの時に単一成長因子を産生する細胞種を切り替えているように思われる。この研究結果は、放射線治療で造血幹細胞が実質的に枯渇していそうな時や、骨髄移植を受けている人の治療に影響を及ぼす可能性がある。この研究は、UCLAのデーヴィッドゲフェン医学部 血液学・腫瘍学の教授であるJohn Chute博士が率いたもので、Cell Stem Cellで発表された。この論文は、「プレオトロフィン制御造血幹細胞の維持および再生の骨髄源(Distinct Bone Marrow Sources of Pleiotrophin Control Hematopoietic Stem Cell Maintenance and Regeneration)」と題されている。血液形成または造血幹細胞は、白血球、赤血球および血小板などの様々な種類の成熟血液要素に分化することができる。それらは、様々なタイプの周囲の細胞が取り囲む骨髄中の「血管性ニッチ」に生存し、部分的には成長因子と呼ばれる化合物を分泌する。このUCLAの研究は、プレオトロフィン(PTN)と呼ばれる成長因子に焦点を当てている。
 メープルツリーはメープルシロップと美しい紅葉でよく知られている。 しかし、その葉の美しさは肌にとっても役立つものになる可能性があることが判明した。科学者らは、葉からの抽出物がしわを防止し得ることを報告している。この研究成果は第256回アメリカ化学会(ACS)の全国会議および博覧会で発表された。世界最大級の学会であるACSは、2018年8月19日〜8月23日にボストンでこの会議を開催した。ACSミーティングでは、幅広い科学分野で10,000件以上のプレゼンテーションが行われた。このメープルリーフの研究者は、以前に、サトウキビとレッドメープルの樹木から得た樹液とシロップの化学的および健康的利点を研究していた。プロジェクトの主任研究者であるロードアイランド大学のNavindra P. Seeram博士によれば、歴史の記録から木の他の部分も有用であることが示唆されたと言う。「ネイティブアメリカンは、伝統薬にレッドメープルの葉を使っていた。葉を無視する理由はない。」と彼は言う。皮膚の弾力性は、エラスチンなどのタンパク質によって維持される。 しわは、酵素エラスターゼが老化過程の一部として皮膚のエラスチンを分解するときに形成される。ACSの会議でこの研究を発表し、Seeram博士の研究室の研究員であるHang Ma博士は、「我々はレッドメープルの葉の抽出物がエラスターゼの活性を阻害するかどうかを知りたがっていた。」と語った。ロードアイランド大学の研究者らは、グルシトール含有ガロタンニン(GCGs)として知られている葉のフェノール化合物をゼロにし、各化合物が試験管内でエラスターゼ活性を阻害する能力を調べた。科学者はまた、GCGがエラスターゼとどのように相互作用してその活性をブロックするか、分子の構造がブロッキング能力にどのように影響するかを調べるためのコンピューター解析を行った。 複数のガロイル基(一種のフェノール基)を含むGCGは、単一のガロイル基を有するものよりも効果的であった。 しかし、これらの化合物は、エラスターゼを妨げる以上の効果がある。以前の研究では、Seeram博士のグループは、これらの同じGCGが炎症から皮膚を保護し、望ましくないそばかすまたは年齢の斑点などの暗い点を明るくする可能性があることを示した。Seeram博士とMa博士はさらなる試験を計画している。
メープルツリーはメープルシロップと美しい紅葉でよく知られている。 しかし、その葉の美しさは肌にとっても役立つものになる可能性があることが判明した。科学者らは、葉からの抽出物がしわを防止し得ることを報告している。この研究成果は第256回アメリカ化学会(ACS)の全国会議および博覧会で発表された。世界最大級の学会であるACSは、2018年8月19日〜8月23日にボストンでこの会議を開催した。ACSミーティングでは、幅広い科学分野で10,000件以上のプレゼンテーションが行われた。このメープルリーフの研究者は、以前に、サトウキビとレッドメープルの樹木から得た樹液とシロップの化学的および健康的利点を研究していた。プロジェクトの主任研究者であるロードアイランド大学のNavindra P. Seeram博士によれば、歴史の記録から木の他の部分も有用であることが示唆されたと言う。「ネイティブアメリカンは、伝統薬にレッドメープルの葉を使っていた。葉を無視する理由はない。」と彼は言う。皮膚の弾力性は、エラスチンなどのタンパク質によって維持される。 しわは、酵素エラスターゼが老化過程の一部として皮膚のエラスチンを分解するときに形成される。ACSの会議でこの研究を発表し、Seeram博士の研究室の研究員であるHang Ma博士は、「我々はレッドメープルの葉の抽出物がエラスターゼの活性を阻害するかどうかを知りたがっていた。」と語った。ロードアイランド大学の研究者らは、グルシトール含有ガロタンニン(GCGs)として知られている葉のフェノール化合物をゼロにし、各化合物が試験管内でエラスターゼ活性を阻害する能力を調べた。科学者はまた、GCGがエラスターゼとどのように相互作用してその活性をブロックするか、分子の構造がブロッキング能力にどのように影響するかを調べるためのコンピューター解析を行った。 複数のガロイル基(一種のフェノール基)を含むGCGは、単一のガロイル基を有するものよりも効果的であった。 しかし、これらの化合物は、エラスターゼを妨げる以上の効果がある。以前の研究では、Seeram博士のグループは、これらの同じGCGが炎症から皮膚を保護し、望ましくないそばかすまたは年齢の斑点などの暗い点を明るくする可能性があることを示した。Seeram博士とMa博士はさらなる試験を計画している。
 自動車事故は、高齢の患者に、癒されない重度の筋肉傷害を残す。 ドナーからの筋肉幹細胞による治療は、損傷した組織を回復させるかもしれないが、医師にはそれらを効果的に送達することが困難だ。新しい方法がこの状況を変えるのに役立つかもしれない。 ジョージア工科大学(Georgia Tech)の研究者は、筋肉がうまく再生しない患者の筋衛星細胞(MuSC)を筋肉組織に直接送達するために、ハイドロゲルである分子マトリックスを設計した。
自動車事故は、高齢の患者に、癒されない重度の筋肉傷害を残す。 ドナーからの筋肉幹細胞による治療は、損傷した組織を回復させるかもしれないが、医師にはそれらを効果的に送達することが困難だ。新しい方法がこの状況を変えるのに役立つかもしれない。 ジョージア工科大学(Georgia Tech)の研究者は、筋肉がうまく再生しない患者の筋衛星細胞(MuSC)を筋肉組織に直接送達するために、ハイドロゲルである分子マトリックスを設計した。
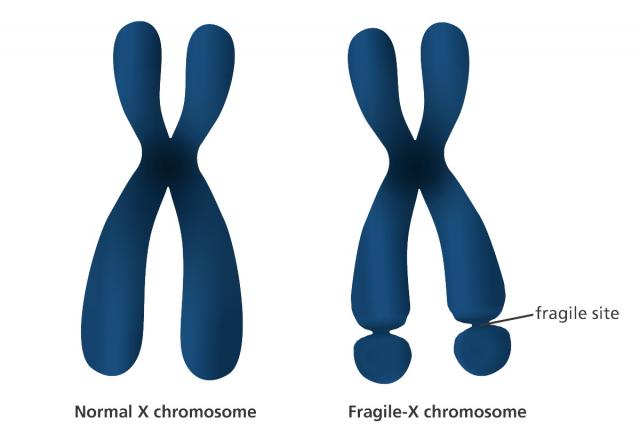 研究者は遺伝子編集ツールを用いて、ヒト幹細胞における脆弱X症候群で抑制されたFMR1遺伝子の再活性化に成功した。このニュースは、2018年8月16日にDiogo PintoによりFragile X News Todayの記事で報告された。 このオープンアクセスの科学論文は「脆弱なX症候群の胚性幹細胞におけるFMR1転写の標的化された再活性化(Targeted Reactivation of FMR1 Transcription In Fragile X Syndrome Embryonic Stem Cells)」と題されており、2018年8月15日に分子神経科学のフロンティアでオンライン公開された。脆弱X症候群(FXS)は、3つの余分なヌクレオチド(DNAのビルディングブロック)をその配列に付加することによって生じるFMR1遺伝子の突然変異によって引き起こされる。 これは、CGGリピートと呼ばれ、健常者では5から55まで変化する。リピートが繰り返されるほど、疾患を発症するリスクが高くなる。 この突然変異は、FMR1遺伝子によって産生されるタンパク質である脆弱X精神遅滞タンパク質(FMRP)の喪失をもたらす。これまでに試験された治療法は、FMRPタンパク質の損失を補うことを試み、通常はタンパク質機能の1つのみを標的とする。しかしながら、それらはこの疾患を治療するには不十分であることが証明されている。研究者らは、神経細胞および他の細胞型においてFMRPによって果たされる異なる機能は、1つの調節不能な分子経路のみを標的とする任意の治療では矯正するのが困難であり、今日までのヒト臨床試験での成功の欠如に関する潜在的な理由の1つと考えている 。
研究者は遺伝子編集ツールを用いて、ヒト幹細胞における脆弱X症候群で抑制されたFMR1遺伝子の再活性化に成功した。このニュースは、2018年8月16日にDiogo PintoによりFragile X News Todayの記事で報告された。 このオープンアクセスの科学論文は「脆弱なX症候群の胚性幹細胞におけるFMR1転写の標的化された再活性化(Targeted Reactivation of FMR1 Transcription In Fragile X Syndrome Embryonic Stem Cells)」と題されており、2018年8月15日に分子神経科学のフロンティアでオンライン公開された。脆弱X症候群(FXS)は、3つの余分なヌクレオチド(DNAのビルディングブロック)をその配列に付加することによって生じるFMR1遺伝子の突然変異によって引き起こされる。 これは、CGGリピートと呼ばれ、健常者では5から55まで変化する。リピートが繰り返されるほど、疾患を発症するリスクが高くなる。 この突然変異は、FMR1遺伝子によって産生されるタンパク質である脆弱X精神遅滞タンパク質(FMRP)の喪失をもたらす。これまでに試験された治療法は、FMRPタンパク質の損失を補うことを試み、通常はタンパク質機能の1つのみを標的とする。しかしながら、それらはこの疾患を治療するには不十分であることが証明されている。研究者らは、神経細胞および他の細胞型においてFMRPによって果たされる異なる機能は、1つの調節不能な分子経路のみを標的とする任意の治療では矯正するのが困難であり、今日までのヒト臨床試験での成功の欠如に関する潜在的な理由の1つと考えている 。
 睡眠についての理解は、慢性的な睡眠不足が蔓延している現代社会において、ますます重要になってきている。 睡眠不足と健康への悪影響の相関関係を示すエビデンスとして、睡眠の核心機能は謎のままである。しかし、2018年7月12日にオープン・アクセス・ジャーナルPLOS Biologyに掲載された新しい研究では、ニューヨークのコロンビア大学のVanessa Hill博士、Mimi Shirasu-Hiza博士および同僚らは、短睡眠ショウジョウバエ変異体が急性酸化ストレスに対する感受性の共通の欠陥を共有し、睡眠が抗酸化プロセスをサポートすることを見出した。地味な存在のショウジョウバエだが、睡眠と酸化ストレスの古くからの双方向の関係を理解することは、睡眠障害や神経変性疾患など現代人の病気についての洞察を得ることができる。この論文は、「ショウジョウバエの睡眠と酸化ストレスとの間の双方向の関係(A Bidirectional Relationship Between Sleep and Oxidative Stress in Drosophila.)」と題されている。 睡眠中の動物は脆弱で不動であり、環境に反応しにくく、捕食者から逃げることができない。睡眠行動の対価にも関わらず、ほとんどの動物は睡眠をとるため、睡眠はヒトからショウジョウバエまで本質的かつ進化的に保存された機能を示唆している。 研究者らは、健康の中枢機能のために睡眠が必要な場合、通常よりも睡眠時間が有意に少ない動物はすべて、その中枢機能に欠陥を共有するはずだと推論した。この研究のために、彼らは短睡眠ショウジョウバエ突然変異体の多様なグループを使用した。 彼らは、これらの短睡眠突然変異体が実際に共通の欠陥を共有していることを発見した。それらはすべて急性酸化ストレスに敏感である。 過剰のフリーラジカルに起因する酸化ストレスは、細胞に損傷を与え臓器機能障害を引き起こす可能性がある。 有毒なフリーラジカルまたは活性酸素種は、正常な代謝および環境ダメージから細胞内に蓄積する。睡眠の機能が酸化ストレスに対する防御ならば、睡眠の増加は酸化ストレスに対する耐性を増加させるはずである。 Hill博士と同僚は、これが真実であることを示すために薬理学的方法と遺伝的方法の両方を使用した。最終的に、著者は睡眠に抗酸化作用があると、酸化ストレスが睡眠そのものを制御する可能性があると提唱した。 この仮説と一致して、彼らは、抗酸化遺伝子を過剰発現させ、脳における酸化ストレスを減少させることによって、睡眠の量も減少することを見出した。これらの結果は、睡眠と酸化ストレスとの双方向性の関係性を指している。つまり、睡眠機能は酸化ストレスや酸化ストレスから体を守り、睡眠を誘発する。この研究は、睡眠障害がアルツハイマー病、パーキンソン病、ハンチントン病などの酸化ストレスに関連する多くの疾患と相関関係にあるため、ヒトの健康に関係している。睡眠喪失は、個体を酸化的ストレスやその後の疾患に対してより敏感にする可能性がある。 逆に、抗酸化物質応答の病理学的な崩壊はまた、睡眠喪失および関連する病状につながる可能性がある。■原著へのリンクは英語版をご覧ください:Antioxidant Benefits of Sleep Suggested in Fly Study
睡眠についての理解は、慢性的な睡眠不足が蔓延している現代社会において、ますます重要になってきている。 睡眠不足と健康への悪影響の相関関係を示すエビデンスとして、睡眠の核心機能は謎のままである。しかし、2018年7月12日にオープン・アクセス・ジャーナルPLOS Biologyに掲載された新しい研究では、ニューヨークのコロンビア大学のVanessa Hill博士、Mimi Shirasu-Hiza博士および同僚らは、短睡眠ショウジョウバエ変異体が急性酸化ストレスに対する感受性の共通の欠陥を共有し、睡眠が抗酸化プロセスをサポートすることを見出した。地味な存在のショウジョウバエだが、睡眠と酸化ストレスの古くからの双方向の関係を理解することは、睡眠障害や神経変性疾患など現代人の病気についての洞察を得ることができる。この論文は、「ショウジョウバエの睡眠と酸化ストレスとの間の双方向の関係(A Bidirectional Relationship Between Sleep and Oxidative Stress in Drosophila.)」と題されている。 睡眠中の動物は脆弱で不動であり、環境に反応しにくく、捕食者から逃げることができない。睡眠行動の対価にも関わらず、ほとんどの動物は睡眠をとるため、睡眠はヒトからショウジョウバエまで本質的かつ進化的に保存された機能を示唆している。 研究者らは、健康の中枢機能のために睡眠が必要な場合、通常よりも睡眠時間が有意に少ない動物はすべて、その中枢機能に欠陥を共有するはずだと推論した。この研究のために、彼らは短睡眠ショウジョウバエ突然変異体の多様なグループを使用した。 彼らは、これらの短睡眠突然変異体が実際に共通の欠陥を共有していることを発見した。それらはすべて急性酸化ストレスに敏感である。 過剰のフリーラジカルに起因する酸化ストレスは、細胞に損傷を与え臓器機能障害を引き起こす可能性がある。 有毒なフリーラジカルまたは活性酸素種は、正常な代謝および環境ダメージから細胞内に蓄積する。睡眠の機能が酸化ストレスに対する防御ならば、睡眠の増加は酸化ストレスに対する耐性を増加させるはずである。 Hill博士と同僚は、これが真実であることを示すために薬理学的方法と遺伝的方法の両方を使用した。最終的に、著者は睡眠に抗酸化作用があると、酸化ストレスが睡眠そのものを制御する可能性があると提唱した。 この仮説と一致して、彼らは、抗酸化遺伝子を過剰発現させ、脳における酸化ストレスを減少させることによって、睡眠の量も減少することを見出した。これらの結果は、睡眠と酸化ストレスとの双方向性の関係性を指している。つまり、睡眠機能は酸化ストレスや酸化ストレスから体を守り、睡眠を誘発する。この研究は、睡眠障害がアルツハイマー病、パーキンソン病、ハンチントン病などの酸化ストレスに関連する多くの疾患と相関関係にあるため、ヒトの健康に関係している。睡眠喪失は、個体を酸化的ストレスやその後の疾患に対してより敏感にする可能性がある。 逆に、抗酸化物質応答の病理学的な崩壊はまた、睡眠喪失および関連する病状につながる可能性がある。■原著へのリンクは英語版をご覧ください:Antioxidant Benefits of Sleep Suggested in Fly Study
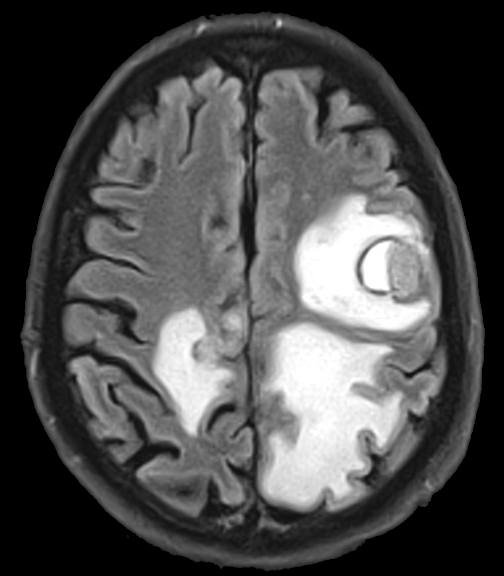 米国コホートの結果からメラノーマ脳転移(MBM: melanoma brain metastases)を有する皮膚メラノーマ患者のうち、チェックポイント阻害剤を用いた第一選択治療では、全生存期間の中央値が1.4倍増加していた。これらの結果は、Cancer Immunology Researchの2018年7月12日にオンラインで公開された。
米国コホートの結果からメラノーマ脳転移(MBM: melanoma brain metastases)を有する皮膚メラノーマ患者のうち、チェックポイント阻害剤を用いた第一選択治療では、全生存期間の中央値が1.4倍増加していた。これらの結果は、Cancer Immunology Researchの2018年7月12日にオンラインで公開された。
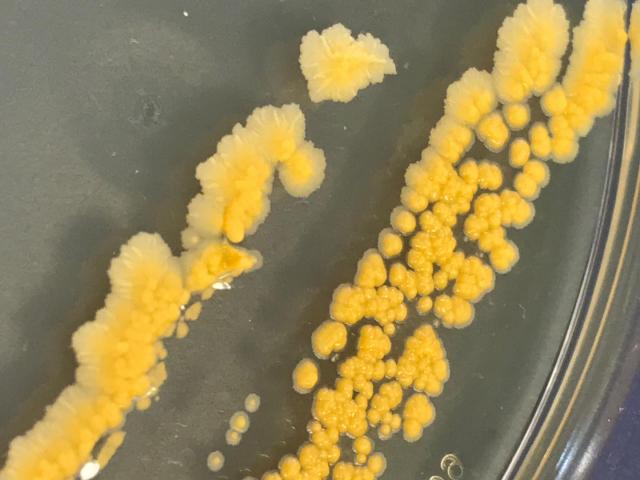 この新しい技術は、ヒト組織を保管し輸送する作業を根本的に改善することがでるだろう。英国のWarwick Medical School 化学部の研究者らは、ある極地生物に見られる天然の不凍タンパク質の合成を人工的に再現し、広範囲の細菌を凍結保存(または「凍結」)する方法を確立した。科学者らは、タンパク質の模倣体を加えることによって氷結晶の成長が遅くなり、それらが細菌細胞を破壊するのを止めることを見出した。 この革新的な方法は、食品産業、臓器輸送、医薬品、ならびに実験室における研究など、様々な用途の可能性を秘めている。細菌は、食品技術(例えば、ヨーグルトおよびプロバイオティクス)、医薬品製造(例えば、インスリン)、および酵素生産(例えば、洗剤)を含む広範なプロセスで使用され、研究室では感染や生活プロセスの基本を研究するために日常的に使用されている。世界中のほぼすべての実験室で使用されている細菌を保存する伝統的なアプローチは、凍結中の低温誘発損傷を減少させるため細菌にグリセロールを添加する方法である。しかし、すべての細菌が解凍後に回復するわけではなく、その成長および有用性を可能にするために、グリセロールを細菌から除去する必要がある。Matthew I. Gibson教授が率いるWarwickのチームは、地球上で最も寒い地域に生存する極地生物にヒントを得て、凍結保存のための新しい方法を開発した。極地生物の中で特に関心を寄せているのは、
この新しい技術は、ヒト組織を保管し輸送する作業を根本的に改善することがでるだろう。英国のWarwick Medical School 化学部の研究者らは、ある極地生物に見られる天然の不凍タンパク質の合成を人工的に再現し、広範囲の細菌を凍結保存(または「凍結」)する方法を確立した。科学者らは、タンパク質の模倣体を加えることによって氷結晶の成長が遅くなり、それらが細菌細胞を破壊するのを止めることを見出した。 この革新的な方法は、食品産業、臓器輸送、医薬品、ならびに実験室における研究など、様々な用途の可能性を秘めている。細菌は、食品技術(例えば、ヨーグルトおよびプロバイオティクス)、医薬品製造(例えば、インスリン)、および酵素生産(例えば、洗剤)を含む広範なプロセスで使用され、研究室では感染や生活プロセスの基本を研究するために日常的に使用されている。世界中のほぼすべての実験室で使用されている細菌を保存する伝統的なアプローチは、凍結中の低温誘発損傷を減少させるため細菌にグリセロールを添加する方法である。しかし、すべての細菌が解凍後に回復するわけではなく、その成長および有用性を可能にするために、グリセロールを細菌から除去する必要がある。Matthew I. Gibson教授が率いるWarwickのチームは、地球上で最も寒い地域に生存する極地生物にヒントを得て、凍結保存のための新しい方法を開発した。極地生物の中で特に関心を寄せているのは、
 テキサス大学(UTサウスウェスタン)の研究者らは、DNA感知酵素が小さなバイオリアクターとして作用し、先天性免疫を刺激する分子を作り出す液滴を形成すると報告している。2018年7月5日にScience誌でオンライン公開された。この研究は、感染、自己免疫疾患、および癌に対する新規治療法につながる可能性がある。
テキサス大学(UTサウスウェスタン)の研究者らは、DNA感知酵素が小さなバイオリアクターとして作用し、先天性免疫を刺激する分子を作り出す液滴を形成すると報告している。2018年7月5日にScience誌でオンライン公開された。この研究は、感染、自己免疫疾患、および癌に対する新規治療法につながる可能性がある。
 東南アジア人の祖先に関する2つの競合する学説は、8,000年前の骨格から抽出された古代人のDNAを革新的手法で分析することによって否定された。東南アジアは世界で最も遺伝的に多様な地域の一つだが、100年以上に渡り科学者たちは、この地域の集団の起源についてどの理論が正しいかについて意見が割れていた。1つの理論は、44,000年前から東南アジアに住んでいた先住民のホアビン狩猟採集民が、東アジアの初期の農家からの提供なしに、独立して農業慣行を採択したと主張している。 "2層モデル"と呼ばれるもう一つの理論は、現在の中国にあたる地域の米農家が移住し、ホアビン狩猟採集民を置き換えたという見解を支持している。2018年7月6日のScience誌に掲載された新研究に協力した世界各地の学者は、どちらの理論も完全に正確ではないことを見出した。彼らの研究は、現在の東南アジア人が少なくとも4つの古代人集団を祖先に持つことを発見した。この論文は「東南アジアの先史時代の人類学(The prehistoric peopling of Southeast Asia.)」と題されたもので、8,000年前のマレーシア、タイ、フィリピン、ベトナム、インドネシア、ラオス、日本からのヒト骨格遺体からDNAが抽出された(これまで成功したDNAシーケンシングは4,000年前のサンプルだけであった)。これらのサンプルには、集団間の遺伝的連鎖が疑われているホアビン狩猟採集民と日本の縄文人のDNAも含まれていた。合計26の古代人のヒトゲノム配列を研究し、東南アジアに住む現代人のDNAサンプルと比較した。東南アジアの暑さと湿気はDNA保存にとって最も困難な環境の一つであり、この先駆的研究は科学者に大きな課題を提起する印象的なものと言える。
東南アジア人の祖先に関する2つの競合する学説は、8,000年前の骨格から抽出された古代人のDNAを革新的手法で分析することによって否定された。東南アジアは世界で最も遺伝的に多様な地域の一つだが、100年以上に渡り科学者たちは、この地域の集団の起源についてどの理論が正しいかについて意見が割れていた。1つの理論は、44,000年前から東南アジアに住んでいた先住民のホアビン狩猟採集民が、東アジアの初期の農家からの提供なしに、独立して農業慣行を採択したと主張している。 "2層モデル"と呼ばれるもう一つの理論は、現在の中国にあたる地域の米農家が移住し、ホアビン狩猟採集民を置き換えたという見解を支持している。2018年7月6日のScience誌に掲載された新研究に協力した世界各地の学者は、どちらの理論も完全に正確ではないことを見出した。彼らの研究は、現在の東南アジア人が少なくとも4つの古代人集団を祖先に持つことを発見した。この論文は「東南アジアの先史時代の人類学(The prehistoric peopling of Southeast Asia.)」と題されたもので、8,000年前のマレーシア、タイ、フィリピン、ベトナム、インドネシア、ラオス、日本からのヒト骨格遺体からDNAが抽出された(これまで成功したDNAシーケンシングは4,000年前のサンプルだけであった)。これらのサンプルには、集団間の遺伝的連鎖が疑われているホアビン狩猟採集民と日本の縄文人のDNAも含まれていた。合計26の古代人のヒトゲノム配列を研究し、東南アジアに住む現代人のDNAサンプルと比較した。東南アジアの暑さと湿気はDNA保存にとって最も困難な環境の一つであり、この先駆的研究は科学者に大きな課題を提起する印象的なものと言える。
 クモの空気力学的能力は、何百年もの間科学者を虜にしてきた。 チャールズ・ダーウィン自身、どのように何百もの生き物たちが穏やかな日にビーグル号に 来て、そして風が吹かない日に素早く船から飛び立つのかをじっと考えていた。科学者らは、これら無翅の節足動物のクモの飛行行動が、風に乗るシルクの尾を放つことによって数千マイルも移動することができる「気球飛行」に起因していると考えていた。 しかし、無風、曇り空、そして雨が降っているときでさえ気球飛行が観察されたという事実は、ある疑問を生じさせる。"クモはどのように空力抵抗が低い状態で飛ぶのか?" ブリストル大学(英国)の生物学者は、その答えを見つけたと確信している。「多くのクモは、扇状に広がった複数本のシルクを使って気球を膨らましている。これは斥力的な静電気力が必要であることを示唆している」と感覚生物物理学の主任研究員 Erica Morley博士は説明する。「現在の理論は、風だけでクモの気球パターンを予測することはできない。何日も大量に飛んだり、他の日にはクモが全く気球を使わなくなるのは何故か? 他の外的な力や気球の空気抵抗を引き起こす可能性があるかどうか、そしてこの刺激を検出するためにどのような知覚システムが使用されるのか探し当てたいと考えていた。」
クモの空気力学的能力は、何百年もの間科学者を虜にしてきた。 チャールズ・ダーウィン自身、どのように何百もの生き物たちが穏やかな日にビーグル号に 来て、そして風が吹かない日に素早く船から飛び立つのかをじっと考えていた。科学者らは、これら無翅の節足動物のクモの飛行行動が、風に乗るシルクの尾を放つことによって数千マイルも移動することができる「気球飛行」に起因していると考えていた。 しかし、無風、曇り空、そして雨が降っているときでさえ気球飛行が観察されたという事実は、ある疑問を生じさせる。"クモはどのように空力抵抗が低い状態で飛ぶのか?" ブリストル大学(英国)の生物学者は、その答えを見つけたと確信している。「多くのクモは、扇状に広がった複数本のシルクを使って気球を膨らましている。これは斥力的な静電気力が必要であることを示唆している」と感覚生物物理学の主任研究員 Erica Morley博士は説明する。「現在の理論は、風だけでクモの気球パターンを予測することはできない。何日も大量に飛んだり、他の日にはクモが全く気球を使わなくなるのは何故か? 他の外的な力や気球の空気抵抗を引き起こす可能性があるかどうか、そしてこの刺激を検出するためにどのような知覚システムが使用されるのか探し当てたいと考えていた。」
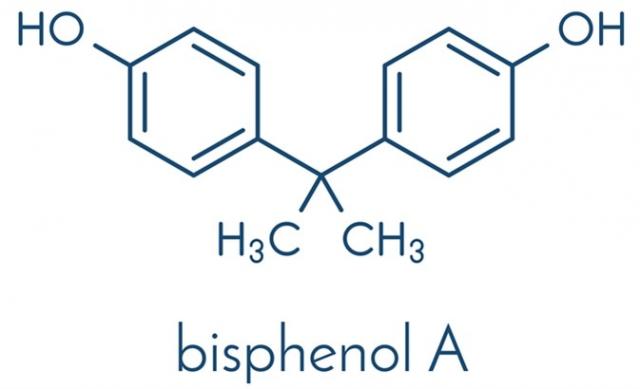 炎症性腸疾患(IBD)の前臨床モデルにおける最近の研究で、ポリカーボネートプラスチックおよびエポキシ樹脂中に見出されるビスフェノールAまたはBPAの食物曝露が死亡率を増加させ、その症状を悪化させる可能性があることを示している。Experimental Biology and Medicine誌で2018年6月6日にオンラインで公開された研究は、テキサスA&M大学の栄養食品科学研究科のClint Allred博士が主導した。この論文は、「芳香族アミノ酸から誘導された微生物代謝産物を変え、大腸炎の間の病気の活動を悪化させるビスフェノールA変種(Bisphenol-A Alters Microbiota Metabolites Derived From Aromatic Amino Acids And Worsens Disease Activity During Colitis.)」と題されている。全文はオンライン< https://tinyurl.com/IBDresearchBPA >で見ることができる。「これはBPAが過敏性腸疾患に関連している腸内微生物のアミノ酸代謝に悪影響を与えることを示す最初の研究である」と栄養食品科学部の大学院生であるJennifer DeLucaは述べた。この研究に参加したのはKimberly Allred博士(栄養食品科学部門)とRami Menon(Texas A&M化学工学科の化学エンジニア)であった。 IBDは、潰瘍性大腸炎およびクローン病を含む複雑な疾患の集合である。 消化管の慢性炎症があり、IBDに関連する症状としては、重度の下痢、腹痛、疲労および体重減少が挙げられる。 より深刻な例は、生涯にわたる治療または場合によっては外科手術を必要とする可能性がある。「IBDの原因はまだ明らかにされていないが、食生活、喫煙、感染、腸内微生物の変化、毒素や汚染物質などの環境暴露は発達と再発の危険因子だ」とClint Allred博士は述べている。「今回の調査では、BPAがIBDに与える影響に焦点を当てたいと考えていた。」BPAは、水ボトルなどの食品および飲料を貯蔵する容器の製造によく使用されるポリカーボネートプラスチックに含まれている。これはまた、食品缶、ボトルトップ、給水ラインなどの金属製品の内部をコーティングするために使用されるエポキシ樹脂にも見られる。 さらに、いくつかの歯科用シーラントおよび複合材料にもBPAが含まれている。
炎症性腸疾患(IBD)の前臨床モデルにおける最近の研究で、ポリカーボネートプラスチックおよびエポキシ樹脂中に見出されるビスフェノールAまたはBPAの食物曝露が死亡率を増加させ、その症状を悪化させる可能性があることを示している。Experimental Biology and Medicine誌で2018年6月6日にオンラインで公開された研究は、テキサスA&M大学の栄養食品科学研究科のClint Allred博士が主導した。この論文は、「芳香族アミノ酸から誘導された微生物代謝産物を変え、大腸炎の間の病気の活動を悪化させるビスフェノールA変種(Bisphenol-A Alters Microbiota Metabolites Derived From Aromatic Amino Acids And Worsens Disease Activity During Colitis.)」と題されている。全文はオンライン< https://tinyurl.com/IBDresearchBPA >で見ることができる。「これはBPAが過敏性腸疾患に関連している腸内微生物のアミノ酸代謝に悪影響を与えることを示す最初の研究である」と栄養食品科学部の大学院生であるJennifer DeLucaは述べた。この研究に参加したのはKimberly Allred博士(栄養食品科学部門)とRami Menon(Texas A&M化学工学科の化学エンジニア)であった。 IBDは、潰瘍性大腸炎およびクローン病を含む複雑な疾患の集合である。 消化管の慢性炎症があり、IBDに関連する症状としては、重度の下痢、腹痛、疲労および体重減少が挙げられる。 より深刻な例は、生涯にわたる治療または場合によっては外科手術を必要とする可能性がある。「IBDの原因はまだ明らかにされていないが、食生活、喫煙、感染、腸内微生物の変化、毒素や汚染物質などの環境暴露は発達と再発の危険因子だ」とClint Allred博士は述べている。「今回の調査では、BPAがIBDに与える影響に焦点を当てたいと考えていた。」BPAは、水ボトルなどの食品および飲料を貯蔵する容器の製造によく使用されるポリカーボネートプラスチックに含まれている。これはまた、食品缶、ボトルトップ、給水ラインなどの金属製品の内部をコーティングするために使用されるエポキシ樹脂にも見られる。 さらに、いくつかの歯科用シーラントおよび複合材料にもBPAが含まれている。
 国際的な研究者チームが音波を用い、血液サンプルから循環腫瘍細胞を臨床使用に迅速かつ効率的に分離する、穏やかで非接触の方法を開発した。循環腫瘍細胞(CTC)は、血流に漏れ出して流れる腫瘍の一部である。腫瘍の種類、身体的特徴、遺伝的変異など、豊富な情報が含まれている。
国際的な研究者チームが音波を用い、血液サンプルから循環腫瘍細胞を臨床使用に迅速かつ効率的に分離する、穏やかで非接触の方法を開発した。循環腫瘍細胞(CTC)は、血流に漏れ出して流れる腫瘍の一部である。腫瘍の種類、身体的特徴、遺伝的変異など、豊富な情報が含まれている。
 オーストラリア連邦科学産業研究機構(CSIRO)は、感染と病気に対する身体の免疫応答を調節する上で重要な役割を果たす遺伝子を同定した。 この発見は、インフルエンザ、関節炎、さらには癌のための新しい治療法の開発につながる可能性がある。 C6orf106または「C6」と呼ばれるこの遺伝子は、感染症、癌および糖尿病に関与するタンパク質の産生を制御している。
オーストラリア連邦科学産業研究機構(CSIRO)は、感染と病気に対する身体の免疫応答を調節する上で重要な役割を果たす遺伝子を同定した。 この発見は、インフルエンザ、関節炎、さらには癌のための新しい治療法の開発につながる可能性がある。 C6orf106または「C6」と呼ばれるこの遺伝子は、感染症、癌および糖尿病に関与するタンパク質の産生を制御している。
 人体の多くの重要なタンパク質は、正しく働くために、鉄 - 硫黄クラスター、鉄と硫黄原子でできた小さな構造を必要とする。アメリカ国立がん研究所(NCI)、アメリカ国立衛生研究所(NIH)、およびケンタッキー大学の研究者は、鉄硫黄クラスターの形成の中断が特定の細胞に脂肪小滴の蓄積をもたらす可能性があることを発見した。これらの発見は、Journal of Biological Chemistryの2018年5月25日号に掲載されており、非アルコール性脂肪肝疾患や腎明細胞癌のような状態の生化学的原因に関する手がかりを提供する。この記事は、「哺乳動物細胞における代謝再プログラミングおよび脂質液滴の形成における鉄-硫黄クラスターの急性喪失(Acute loss of Iron–Sulfur Clusters Results in Metabolic Reprogramming and Generation of Lipid Droplets in Mammalian Cells.)」と題されている。「鉄-硫黄クラスターは繊細で、細胞内の損傷を受けやすい」と新しい研究を率いたポスドクのDaniel Crooks博士は語った。「この理由から、私たちの体内の細胞は常に新しい鉄-硫黄クラスターを構築している」 Crooks博士は、NIH傘下機関の国立小児保健発達研究所(Eunice Kennedy Shriver National Institute of Child Health and Human Development:NICHD)のTracey Rouault博士のラボで、鉄-硫黄クラスターを形成する酵素の研究を開始した。
人体の多くの重要なタンパク質は、正しく働くために、鉄 - 硫黄クラスター、鉄と硫黄原子でできた小さな構造を必要とする。アメリカ国立がん研究所(NCI)、アメリカ国立衛生研究所(NIH)、およびケンタッキー大学の研究者は、鉄硫黄クラスターの形成の中断が特定の細胞に脂肪小滴の蓄積をもたらす可能性があることを発見した。これらの発見は、Journal of Biological Chemistryの2018年5月25日号に掲載されており、非アルコール性脂肪肝疾患や腎明細胞癌のような状態の生化学的原因に関する手がかりを提供する。この記事は、「哺乳動物細胞における代謝再プログラミングおよび脂質液滴の形成における鉄-硫黄クラスターの急性喪失(Acute loss of Iron–Sulfur Clusters Results in Metabolic Reprogramming and Generation of Lipid Droplets in Mammalian Cells.)」と題されている。「鉄-硫黄クラスターは繊細で、細胞内の損傷を受けやすい」と新しい研究を率いたポスドクのDaniel Crooks博士は語った。「この理由から、私たちの体内の細胞は常に新しい鉄-硫黄クラスターを構築している」 Crooks博士は、NIH傘下機関の国立小児保健発達研究所(Eunice Kennedy Shriver National Institute of Child Health and Human Development:NICHD)のTracey Rouault博士のラボで、鉄-硫黄クラスターを形成する酵素の研究を開始した。
 「ヒト独特」と考えられていた筋肉が、いくつかの類人猿の種で発見されており、ヒトの軟組織の起源と進化に関する長年の理論に議論が起こっている。 この発見は、特定の筋肉が、二足歩行、道具の使用、声によるコミュニケーション、表情など、ヒトの特質に対する特別な適応を提供する唯一の目的のために進化したというヒト中心の見解に疑問を投げかけている。Frontiers in Ecology and Evolutionで2018年4月26日に発表されたこの研究は、ヒトの進化をより良く理解するためには、類人猿の解剖学の徹底的な知識が必要であることを強調している。この論文は、「ボノボの最初の詳細な解剖学的研究は、特定の変異を明らかにし、ヒトの進化、二足歩行、および道具の使用に関するストーリーを明らかにする。(First Detailed Anatomical Study of Bonobos Reveals Intra-Specific Variations and Exposes Just-So Stories of Human Evolution, Bipedalism, and Tool Use.)」と題されている。 「この研究は、ヒトの進化と〝自然の階段〟におけるヒトの位置付けについてのドグマと矛盾している」とワシントンDCのハワード大学 解剖学科のRui Diogo博士は言う。
「ヒト独特」と考えられていた筋肉が、いくつかの類人猿の種で発見されており、ヒトの軟組織の起源と進化に関する長年の理論に議論が起こっている。 この発見は、特定の筋肉が、二足歩行、道具の使用、声によるコミュニケーション、表情など、ヒトの特質に対する特別な適応を提供する唯一の目的のために進化したというヒト中心の見解に疑問を投げかけている。Frontiers in Ecology and Evolutionで2018年4月26日に発表されたこの研究は、ヒトの進化をより良く理解するためには、類人猿の解剖学の徹底的な知識が必要であることを強調している。この論文は、「ボノボの最初の詳細な解剖学的研究は、特定の変異を明らかにし、ヒトの進化、二足歩行、および道具の使用に関するストーリーを明らかにする。(First Detailed Anatomical Study of Bonobos Reveals Intra-Specific Variations and Exposes Just-So Stories of Human Evolution, Bipedalism, and Tool Use.)」と題されている。 「この研究は、ヒトの進化と〝自然の階段〟におけるヒトの位置付けについてのドグマと矛盾している」とワシントンDCのハワード大学 解剖学科のRui Diogo博士は言う。
 アメリカ国立衛生研究所(NIH)は、2018年5月6日(日)に、すべてのバックグラウンドの人々の個別化予防・治療・ケアを目指し、「All of Us 研究プログラム」(https://www.joinallofus.org/en)の全国登録を開始した。健康状態にかかわらず、18歳以上の人々が登録することができる。公開日には、全国の7つの都市でのコミュニティイベントとオンラインイベントが行われた。プログラムの全国立ち上げの準備期間における1年間のベータテストを通じ、All of Usにすでに2万5千人以上のボランティアが登録している。全体的な目的は、100万人以上のボランティアと研究で過小評価されているオーバーサンプリングコミュニティを登録することです。Alex Azar 保健福祉部長官は、「All of Usは、病気や医療の研究方法に革命を起こす可能性のある野心的なプロジェクトだ」と述べた。「NIHの前例のない努力は、パーソナライズされた、非常に効果的なヘルスケアの新しい時代のための科学的基礎を築くだろう。 私たちは、全てのバックグラウンドの人々と協力して、この国の健康のために大きな一歩を踏み出すことを楽しみにしている。」プレシジョンメディシンは、人々のライフスタイル、環境、遺伝子を含む生物学的構成の違いを考慮した、疾患の治療と予防への新たなアプローチである。眼鏡や補聴器では、私たちは長い間、個人のニーズに合わせたカスタマイズされたソリューションを提供されてきた。 もっと最近では、特定のタイプの癌の治療は、患者のDNAを標的とした治療で可能になった。 それでも、個人、その家族、地域社会、医療界に良い選択肢を与えられずに多くの未解決の課題が残っている。
アメリカ国立衛生研究所(NIH)は、2018年5月6日(日)に、すべてのバックグラウンドの人々の個別化予防・治療・ケアを目指し、「All of Us 研究プログラム」(https://www.joinallofus.org/en)の全国登録を開始した。健康状態にかかわらず、18歳以上の人々が登録することができる。公開日には、全国の7つの都市でのコミュニティイベントとオンラインイベントが行われた。プログラムの全国立ち上げの準備期間における1年間のベータテストを通じ、All of Usにすでに2万5千人以上のボランティアが登録している。全体的な目的は、100万人以上のボランティアと研究で過小評価されているオーバーサンプリングコミュニティを登録することです。Alex Azar 保健福祉部長官は、「All of Usは、病気や医療の研究方法に革命を起こす可能性のある野心的なプロジェクトだ」と述べた。「NIHの前例のない努力は、パーソナライズされた、非常に効果的なヘルスケアの新しい時代のための科学的基礎を築くだろう。 私たちは、全てのバックグラウンドの人々と協力して、この国の健康のために大きな一歩を踏み出すことを楽しみにしている。」プレシジョンメディシンは、人々のライフスタイル、環境、遺伝子を含む生物学的構成の違いを考慮した、疾患の治療と予防への新たなアプローチである。眼鏡や補聴器では、私たちは長い間、個人のニーズに合わせたカスタマイズされたソリューションを提供されてきた。 もっと最近では、特定のタイプの癌の治療は、患者のDNAを標的とした治療で可能になった。 それでも、個人、その家族、地域社会、医療界に良い選択肢を与えられずに多くの未解決の課題が残っている。
 スタンフォード大学の研究者は、新研究でラットの傷ついた肺の呼吸能力を回復させるのに有効なタンパク質模倣物を生物工学により作った。この合成産物は、ヒトの急性肺傷害に対して、より良い、より安価な治療につながる可能性がある。 ラットで使用した際、それはいくつかの生理的尺度で高価な動物由来の製品と同等またはそれ以上の性能を示したと研究は述べている。この研究論文は、5月1日にScientific Reportsにオンラインで掲載された。このオープンアクセス論文は、「肺サーファクタントタンパク質のヘリックス性、両親媒性ペプトイド模倣物による急性肺傷害の有効なインビボ治療(Effective in vivo treatment of acute lung injury with helical, amphipathic peptoid mimics of pulmonary surfactant proteins.)」と題されている。テニスコートぐらいの表面積を持つ風船を膨らませるために必要な力を想像してください。 さらに、その風船にはポケットがあり、湿った内面を持ち、繊細な素材で作られていると想像してください。その風船とはあなたの肺のことです。すべての呼吸は奇跡的なことなのです。石鹸の様な膜または界面活性剤の薄いコーティングが肺の内面の張力を低下させ、吸入するのに必要な力を大きく減少させる。この界面活性剤なくして、呼吸することはできない。スタンフォード大学の生物工学准教授であるAnnelise Barron 博士(写真)は、「肺の界面活性剤には素晴らしい生物学的特性がある。」と述べた。
スタンフォード大学の研究者は、新研究でラットの傷ついた肺の呼吸能力を回復させるのに有効なタンパク質模倣物を生物工学により作った。この合成産物は、ヒトの急性肺傷害に対して、より良い、より安価な治療につながる可能性がある。 ラットで使用した際、それはいくつかの生理的尺度で高価な動物由来の製品と同等またはそれ以上の性能を示したと研究は述べている。この研究論文は、5月1日にScientific Reportsにオンラインで掲載された。このオープンアクセス論文は、「肺サーファクタントタンパク質のヘリックス性、両親媒性ペプトイド模倣物による急性肺傷害の有効なインビボ治療(Effective in vivo treatment of acute lung injury with helical, amphipathic peptoid mimics of pulmonary surfactant proteins.)」と題されている。テニスコートぐらいの表面積を持つ風船を膨らませるために必要な力を想像してください。 さらに、その風船にはポケットがあり、湿った内面を持ち、繊細な素材で作られていると想像してください。その風船とはあなたの肺のことです。すべての呼吸は奇跡的なことなのです。石鹸の様な膜または界面活性剤の薄いコーティングが肺の内面の張力を低下させ、吸入するのに必要な力を大きく減少させる。この界面活性剤なくして、呼吸することはできない。スタンフォード大学の生物工学准教授であるAnnelise Barron 博士(写真)は、「肺の界面活性剤には素晴らしい生物学的特性がある。」と述べた。
 新しい研究によると、特定の種類のダークチョコレートを食べると健康上の恩恵があるかもしれない。 サンディエゴで行われたExperimental Biology 2018年次会議(2月21-25日)で発表された2つの研究結果は、高濃度のカカオ(カカオ70%、有機砂糖30%)を含むダークチョコレートを摂取すると、ストレスレベル、炎症、気分、記憶、および免疫にポジティブな効果が見られた。カカオがフラボノイドを多く含むことはよく知られているが、認知、内分泌、および心臓血管の健康をどの様にサポートするのかを特定するため、ヒト被験者で効果が研究されたのはこれが初めてである。米国ロマリンダ大学の連合医療専門学校、精神免疫学および食品科学の研究部長 Lee S. Berk 公衆衛生学博士は、両研究の主任研究員を務めた。 「数年前から、ダークチョコレートの糖度の観点からの神経学的機能への影響を見てきた。砂糖が多いほど私たちはより幸せだ。」とBerk博士は述べた。 「短期間または長期間にわたり、通常サイズのチョコレートバーと同程度の少量のカカオの影響を見てきたのはこれが初めてのことである。これらの研究は、カカオの濃度が高いほど認知、記憶、気分、免疫、および他の有益な効果への影響がよりポジティブなものであることを示している」カカオのフラボノイドは、脳や心臓血管の健康に有益な既知のメカニズムを有する極めて強力な抗酸化剤および抗炎症剤である。下記の結果は「ダークチョコレート(70%カカオ)がヒトの遺伝子発現に及ぼす影響:カカオは細胞の免疫応答、神経シグナル伝達および知覚を調節する」(4月23日月曜日10: 00〜12:00、サンディエゴ・コンベンションセンター・展示ホールA〜D)で発表された。
新しい研究によると、特定の種類のダークチョコレートを食べると健康上の恩恵があるかもしれない。 サンディエゴで行われたExperimental Biology 2018年次会議(2月21-25日)で発表された2つの研究結果は、高濃度のカカオ(カカオ70%、有機砂糖30%)を含むダークチョコレートを摂取すると、ストレスレベル、炎症、気分、記憶、および免疫にポジティブな効果が見られた。カカオがフラボノイドを多く含むことはよく知られているが、認知、内分泌、および心臓血管の健康をどの様にサポートするのかを特定するため、ヒト被験者で効果が研究されたのはこれが初めてである。米国ロマリンダ大学の連合医療専門学校、精神免疫学および食品科学の研究部長 Lee S. Berk 公衆衛生学博士は、両研究の主任研究員を務めた。 「数年前から、ダークチョコレートの糖度の観点からの神経学的機能への影響を見てきた。砂糖が多いほど私たちはより幸せだ。」とBerk博士は述べた。 「短期間または長期間にわたり、通常サイズのチョコレートバーと同程度の少量のカカオの影響を見てきたのはこれが初めてのことである。これらの研究は、カカオの濃度が高いほど認知、記憶、気分、免疫、および他の有益な効果への影響がよりポジティブなものであることを示している」カカオのフラボノイドは、脳や心臓血管の健康に有益な既知のメカニズムを有する極めて強力な抗酸化剤および抗炎症剤である。下記の結果は「ダークチョコレート(70%カカオ)がヒトの遺伝子発現に及ぼす影響:カカオは細胞の免疫応答、神経シグナル伝達および知覚を調節する」(4月23日月曜日10: 00〜12:00、サンディエゴ・コンベンションセンター・展示ホールA〜D)で発表された。
 それはDNAだが、私たちの知っているそれではない。オーストラリアの研究者は世界で初めて細胞内に“iモチーフ”と呼ばれる新しいDNA構造を同定した。DNAのねじれた“結び目”、iモチーフはこれまで生きている細胞の中で直接見られたことはなかった。ガルバン医学研究所の新しい発見は、Nature Chemistryの2018年4月23日にオンラインで公開された。
それはDNAだが、私たちの知っているそれではない。オーストラリアの研究者は世界で初めて細胞内に“iモチーフ”と呼ばれる新しいDNA構造を同定した。DNAのねじれた“結び目”、iモチーフはこれまで生きている細胞の中で直接見られたことはなかった。ガルバン医学研究所の新しい発見は、Nature Chemistryの2018年4月23日にオンラインで公開された。
 免疫革命と呼ばれる中、ペンシルベニア大学のアブラムソンがんセンター(UPenn)のディレクターであるRobert H. Vonderheide MD,PhD(写真)が、癌免疫療法の分野で革新的な進歩を続けている。Vonderheide博士は画期的な免疫療法の成功について、多くの患者が初期の成功の後に反応しなくなるか、または再発するかのいずれかであるため、甘くないと説明している。
免疫革命と呼ばれる中、ペンシルベニア大学のアブラムソンがんセンター(UPenn)のディレクターであるRobert H. Vonderheide MD,PhD(写真)が、癌免疫療法の分野で革新的な進歩を続けている。Vonderheide博士は画期的な免疫療法の成功について、多くの患者が初期の成功の後に反応しなくなるか、または再発するかのいずれかであるため、甘くないと説明している。
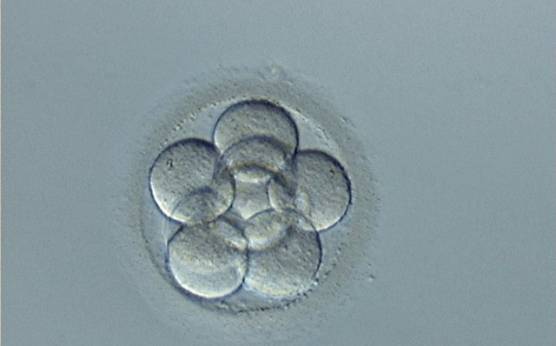 科学誌Cellの2018年3月22日号に掲載された論文によると、非常に初期の段階のヒト胚でヒト発生の謎を解明するのに一歩近づく、ヒト胚の遺伝子発現を活性化させる重要なファクターを中国の科学者が明らかにした。この論文は、「ヒト初期胚のクロマチン・アクセシビリティの状況と進化との関連(Chromatin Accessibility Landscape in Human Early Embryos and Its Association with Evolution.)」と題されている。ヒトの生命は受精卵から始まる。 しかし、受精後の最初の2日間は、ヒト胚で遺伝子発現はほとんどなかった。 これまでゲノムがどのように活性化し、初期胚で遺伝子発現を開始するのか、科学者は知らなかった。「遺伝子発現を活性化するものは何か?このパズルは世界中の科学者を悩ませています。私たちはこれを最初に見つけました」と、この論文の上級著者であるLiu Jiang博士は述べている。 ヒトが成長する間、適切な時と場所で異なる遺伝子が発現されなければならない。DNAに保存されている遺伝コードは、遺伝子発現によって「解釈」され、これにより個体の特徴が生じる。中国科学アカデミー(CAS)の北京研究所のLiu博士主導のチーム、Shandong大学・繁殖医学センターのChen Zijiang博士、Guangzhou医科大学のLiu Jianqiao博士のグループは、転写因子であるOct-4が接合体のゲノム発現を活性化するのに重要な役割を果たすことを見出した。
科学誌Cellの2018年3月22日号に掲載された論文によると、非常に初期の段階のヒト胚でヒト発生の謎を解明するのに一歩近づく、ヒト胚の遺伝子発現を活性化させる重要なファクターを中国の科学者が明らかにした。この論文は、「ヒト初期胚のクロマチン・アクセシビリティの状況と進化との関連(Chromatin Accessibility Landscape in Human Early Embryos and Its Association with Evolution.)」と題されている。ヒトの生命は受精卵から始まる。 しかし、受精後の最初の2日間は、ヒト胚で遺伝子発現はほとんどなかった。 これまでゲノムがどのように活性化し、初期胚で遺伝子発現を開始するのか、科学者は知らなかった。「遺伝子発現を活性化するものは何か?このパズルは世界中の科学者を悩ませています。私たちはこれを最初に見つけました」と、この論文の上級著者であるLiu Jiang博士は述べている。 ヒトが成長する間、適切な時と場所で異なる遺伝子が発現されなければならない。DNAに保存されている遺伝コードは、遺伝子発現によって「解釈」され、これにより個体の特徴が生じる。中国科学アカデミー(CAS)の北京研究所のLiu博士主導のチーム、Shandong大学・繁殖医学センターのChen Zijiang博士、Guangzhou医科大学のLiu Jianqiao博士のグループは、転写因子であるOct-4が接合体のゲノム発現を活性化するのに重要な役割を果たすことを見出した。
 2018年1月16日付JAMA Internal Medicineオンライン版に掲載された新Kaiser Permanente研究は、長期的な全国研究で6か月以上母乳育児すると、妊娠可能期間を通じて母体の2型糖尿病発病リスクが半分近くまで低下することを突き止めたと述べている。このオープン・アクセス論文は、「Lactation Duration and Progression to Diabetes in Women Across the Childbearing Years: The 30-Year CARDIA Study (授乳期間と妊娠可能期間を通じての糖尿病発症の関係:30年間のCARDIA研究)」と題されている。 論文の筆頭著者であり、Kaiser Permanente Division of ResearchのSenior Research Scientistを務めるErica P. Gunderson, PhD, MS, MPHは、「母乳育児期間と糖尿病発症リスク低下の間には、考えられる他のリスク・ファクターをすべて計算に入れても強い関連性が認められた」と述べている。出産の度に6か月以上母乳育児していた女性は、母乳育児をまったくしなかった女性に比べると、2型糖尿病を発症するリスクが47%も低下していた。また、母乳育児の期間が6か月以下の女性の場合、糖尿病リスク低下率は25%だった。
2018年1月16日付JAMA Internal Medicineオンライン版に掲載された新Kaiser Permanente研究は、長期的な全国研究で6か月以上母乳育児すると、妊娠可能期間を通じて母体の2型糖尿病発病リスクが半分近くまで低下することを突き止めたと述べている。このオープン・アクセス論文は、「Lactation Duration and Progression to Diabetes in Women Across the Childbearing Years: The 30-Year CARDIA Study (授乳期間と妊娠可能期間を通じての糖尿病発症の関係:30年間のCARDIA研究)」と題されている。 論文の筆頭著者であり、Kaiser Permanente Division of ResearchのSenior Research Scientistを務めるErica P. Gunderson, PhD, MS, MPHは、「母乳育児期間と糖尿病発症リスク低下の間には、考えられる他のリスク・ファクターをすべて計算に入れても強い関連性が認められた」と述べている。出産の度に6か月以上母乳育児していた女性は、母乳育児をまったくしなかった女性に比べると、2型糖尿病を発症するリスクが47%も低下していた。また、母乳育児の期間が6か月以下の女性の場合、糖尿病リスク低下率は25%だった。
 ほとんどの女性は妊娠中につわりを経験するが、妊娠中の女性の約2%が、ときには症状が深刻で入院が必要な程の、より重度の悪心および嘔吐の症状を経験する。妊娠中の重度妊婦とも呼ばれるこの状態は、ケイト・ミドルトン/ケンブリッジ公爵夫人が妊娠中に耐えたものと同じである。 UCLAの研究者によって主導され、2018年3月23日にNature Communicationsのオンライン版に公開されたこの新しい研究では、前回の研究では原因が特定されていない、催吐性重篤度に関連する2つの遺伝子が同定された。GDF15およびIGFBP7として知られているこの遺伝子は、胎盤の発達に関与しており、早期妊娠および食欲調節において重要な役割を果たす。このオープンアクセスの論文は「胎盤と食欲遺伝子GDF15とIGFBP7は、妊娠悪阻に関連している。(Placenta and Appetite Genes GDF15 And IGFBP7 Are Associated with Hyperemesis Gravidarum.)」と題されている。
ほとんどの女性は妊娠中につわりを経験するが、妊娠中の女性の約2%が、ときには症状が深刻で入院が必要な程の、より重度の悪心および嘔吐の症状を経験する。妊娠中の重度妊婦とも呼ばれるこの状態は、ケイト・ミドルトン/ケンブリッジ公爵夫人が妊娠中に耐えたものと同じである。 UCLAの研究者によって主導され、2018年3月23日にNature Communicationsのオンライン版に公開されたこの新しい研究では、前回の研究では原因が特定されていない、催吐性重篤度に関連する2つの遺伝子が同定された。GDF15およびIGFBP7として知られているこの遺伝子は、胎盤の発達に関与しており、早期妊娠および食欲調節において重要な役割を果たす。このオープンアクセスの論文は「胎盤と食欲遺伝子GDF15とIGFBP7は、妊娠悪阻に関連している。(Placenta and Appetite Genes GDF15 And IGFBP7 Are Associated with Hyperemesis Gravidarum.)」と題されている。
 大きな出っ歯、シワだらけで毛が無い身体。こんなハダカデバネズミは「かわいい齧歯類」コンテストでとても勝てそうにない。しかし、ハダカデバネズミの寿命は齧歯類としては最長の30年という長寿であり、加齢性の疾患に驚くほどの耐性があるため、加齢とがんという謎を解くカギを与えてくれている。それこそが、University of Rochester のVera Gorbunova, PhD、Andrei Seluanov, PhDら生物学教授とポスドク研究員のYang Zhao, PhDのハダカデバネズミ研究の動機であり、2018年2月5日付PNASオンライン版に掲載された研究論文の筆頭著者、Dr. Zhaoは、「この齧歯類で、細胞老化と呼ばれる抗がんメカニズムが見られるだろうか? 見られるとすれば、そのメカニズムはマウスのような寿命の短い動物とどのように異なるのだろうか、ということを調べた」と述べている。
大きな出っ歯、シワだらけで毛が無い身体。こんなハダカデバネズミは「かわいい齧歯類」コンテストでとても勝てそうにない。しかし、ハダカデバネズミの寿命は齧歯類としては最長の30年という長寿であり、加齢性の疾患に驚くほどの耐性があるため、加齢とがんという謎を解くカギを与えてくれている。それこそが、University of Rochester のVera Gorbunova, PhD、Andrei Seluanov, PhDら生物学教授とポスドク研究員のYang Zhao, PhDのハダカデバネズミ研究の動機であり、2018年2月5日付PNASオンライン版に掲載された研究論文の筆頭著者、Dr. Zhaoは、「この齧歯類で、細胞老化と呼ばれる抗がんメカニズムが見られるだろうか? 見られるとすれば、そのメカニズムはマウスのような寿命の短い動物とどのように異なるのだろうか、ということを調べた」と述べている。
 トカゲには特別な超能力がある。鳥類は羽根を再生できるし、ほ乳類は皮膚を再生できる。しかし、トカゲはしっぽのような構造全体を再生できるのだ。このような違いはあっても、動物はすべてトカゲのような共通の祖先から進化してきたものだ。アメリカ全体に広がっているトカゲのグループ、アノールは、ダーウィン・フィンチのように、様々な島や、大陸本土の様々な棲息地の条件に適応している。現在では、その種は400を超える。Arizona State University (ASU) の研究者は、パナマのSmithsonian Tropical Research Institute (STRI) を通じてパナマで採集した3種のトカゲと、アメリカ南東部で採集した1種のトカゲの系統樹を再構成し、トカゲのゲノムのDNAコード全体を他の動物と比較した。その結果、松果体その他の内分泌腺のある間脳で、色覚、ホルモン、オスがメスを誘うために上下に揺らす喉袋などに関わる遺伝子の変化が起きており、それが種の境界を形成している可能性があることを突き止めた。四肢の発達を調節する遺伝子も特に急速に進化している。責任著者でASU School of Life Sciencesの教授を務めるDr. Kenro Kusumiは、「リクガメのような爬虫類は何百万年もの間、ほとんど変わっていないが、アノール・トカゲは急速に進化しており、様々な形や行動の違いを生み出している。今はゲノム全体をシーケンシングすることも低コストかつ容易になっており、今回の研究で急激な進化の分子遺伝学的証拠がつかめており、この進化こそが動物の棲む環境が異なればその身体にも著しい違いが生まれる理由かも知れない」と述べている。この研究は2018年2月1日付Genome Biology and Evolutionのオープンアクセス論文として掲載されており、「Comparative Genomics Reveals Accelerated Evolution in Conserved Pathways during the Diversification of Anole Lizards (比較遺伝学研究によりアノール・トカゲの多様化の過程で保存経路の急速な進化が明らかに)」と題されている。Dr. Kusumi研究グループは、University of Arizona College of Medicine-Phoenixの同僚と共同で研究を続けており、爬虫類のゲノムが爬虫類の再生能力や様々な体形に発達する能力に及ぼす影響に特に関心を抱いている。
トカゲには特別な超能力がある。鳥類は羽根を再生できるし、ほ乳類は皮膚を再生できる。しかし、トカゲはしっぽのような構造全体を再生できるのだ。このような違いはあっても、動物はすべてトカゲのような共通の祖先から進化してきたものだ。アメリカ全体に広がっているトカゲのグループ、アノールは、ダーウィン・フィンチのように、様々な島や、大陸本土の様々な棲息地の条件に適応している。現在では、その種は400を超える。Arizona State University (ASU) の研究者は、パナマのSmithsonian Tropical Research Institute (STRI) を通じてパナマで採集した3種のトカゲと、アメリカ南東部で採集した1種のトカゲの系統樹を再構成し、トカゲのゲノムのDNAコード全体を他の動物と比較した。その結果、松果体その他の内分泌腺のある間脳で、色覚、ホルモン、オスがメスを誘うために上下に揺らす喉袋などに関わる遺伝子の変化が起きており、それが種の境界を形成している可能性があることを突き止めた。四肢の発達を調節する遺伝子も特に急速に進化している。責任著者でASU School of Life Sciencesの教授を務めるDr. Kenro Kusumiは、「リクガメのような爬虫類は何百万年もの間、ほとんど変わっていないが、アノール・トカゲは急速に進化しており、様々な形や行動の違いを生み出している。今はゲノム全体をシーケンシングすることも低コストかつ容易になっており、今回の研究で急激な進化の分子遺伝学的証拠がつかめており、この進化こそが動物の棲む環境が異なればその身体にも著しい違いが生まれる理由かも知れない」と述べている。この研究は2018年2月1日付Genome Biology and Evolutionのオープンアクセス論文として掲載されており、「Comparative Genomics Reveals Accelerated Evolution in Conserved Pathways during the Diversification of Anole Lizards (比較遺伝学研究によりアノール・トカゲの多様化の過程で保存経路の急速な進化が明らかに)」と題されている。Dr. Kusumi研究グループは、University of Arizona College of Medicine-Phoenixの同僚と共同で研究を続けており、爬虫類のゲノムが爬虫類の再生能力や様々な体形に発達する能力に及ぼす影響に特に関心を抱いている。
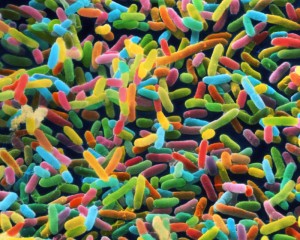 遺伝環境論争は、ヒトが腸内に持っている通常有益な細菌群、マイクロバイオーム(微生物叢)の構成にまで広がっている。研究に次ぐ研究でマイクロバイオームが私達の健康のほぼ全ての面に関わっていることが突き止められており、また、人それぞれに異なっているマイクロバイオームの構成が体重増加やその人の気分にまで関わっている可能性も示されている。一部のマイクロバイオーム研究者は、このような個人差は遺伝子の違いから始まっているのではないかとしているが、イスラエルのWeizmann Institute of Scienceで行われた大規模な研究はこの遺伝子説に反証しており、さらにマイクロバイオームと健康の間には私達が考えている以上に重要な関係を示す証拠を提出している。事実、その研究でも作業仮説としてマイクロバイオームの個人差に遺伝子が大きく関わっているのではないかと予想していた。その仮説に従えば、遺伝子がマイクロバイオームの棲息する環境を決定し、さらに個々の環境がそこで繁殖する細菌種を決定するはずだった。ところが、実際には宿主の遺伝はマイクロバイオームの構成にごくわずかしか関わっておらず、大人口で考えた場合、わずか2%程度の違いにしかならないことを突き止め、Weizmannの研究チームにとってはむしろ意外だった。
遺伝環境論争は、ヒトが腸内に持っている通常有益な細菌群、マイクロバイオーム(微生物叢)の構成にまで広がっている。研究に次ぐ研究でマイクロバイオームが私達の健康のほぼ全ての面に関わっていることが突き止められており、また、人それぞれに異なっているマイクロバイオームの構成が体重増加やその人の気分にまで関わっている可能性も示されている。一部のマイクロバイオーム研究者は、このような個人差は遺伝子の違いから始まっているのではないかとしているが、イスラエルのWeizmann Institute of Scienceで行われた大規模な研究はこの遺伝子説に反証しており、さらにマイクロバイオームと健康の間には私達が考えている以上に重要な関係を示す証拠を提出している。事実、その研究でも作業仮説としてマイクロバイオームの個人差に遺伝子が大きく関わっているのではないかと予想していた。その仮説に従えば、遺伝子がマイクロバイオームの棲息する環境を決定し、さらに個々の環境がそこで繁殖する細菌種を決定するはずだった。ところが、実際には宿主の遺伝はマイクロバイオームの構成にごくわずかしか関わっておらず、大人口で考えた場合、わずか2%程度の違いにしかならないことを突き止め、Weizmannの研究チームにとってはむしろ意外だった。
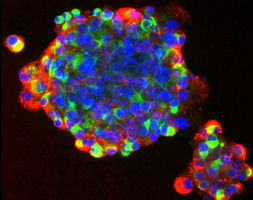 肺再生研究を飛躍的に進める画期的な結果が、このたび、シンガポール科学技術研究庁(Agency for Science, Technology and Research (A*STAR))遺伝子研究所(GIS)と分子生物学研究所(IMB)との共同研究で得られた。彼らの研究は、肺に存在する特殊な幹細胞である末梢気道胚細胞(DASCs)が、損傷を受けた胚組織を新しい肺胞に取り換える機能を有する事を実証し、肺の再生研究に大きな基礎を築いた。この研究は2011年10月28日付けのセル誌に掲載された。肺は、インフルエンザや慢性閉塞成敗疾患(COPD)などの慢性呼吸器疾患を含む様々な肺疾患により損傷を受ける。
肺再生研究を飛躍的に進める画期的な結果が、このたび、シンガポール科学技術研究庁(Agency for Science, Technology and Research (A*STAR))遺伝子研究所(GIS)と分子生物学研究所(IMB)との共同研究で得られた。彼らの研究は、肺に存在する特殊な幹細胞である末梢気道胚細胞(DASCs)が、損傷を受けた胚組織を新しい肺胞に取り換える機能を有する事を実証し、肺の再生研究に大きな基礎を築いた。この研究は2011年10月28日付けのセル誌に掲載された。肺は、インフルエンザや慢性閉塞成敗疾患(COPD)などの慢性呼吸器疾患を含む様々な肺疾患により損傷を受ける。
 報いられない愛に苦しまない種はない。しかし、アメリカのテキサス州在来種の個体全てがメスで無性生殖をすることで知られたカダヤシ属の淡水魚、アマゾン・モーリーは何千年も栄えてきた種である。最近、この魚のゲノムシーケンス解析が完了しており、その性の生物学的基礎情報から学ぶことは多いのではないかと研究者は期待している。テキサス州・メキシコ国境線に沿った淡水の河川はこの進化異常の種の棲息地になっており、この魚は自然の法則に反して受精なしで胚の発育と発達が起き、母親とまったく同一のクローンの娘だけができる単為生殖という自然の形式によって繁栄してきた。Texas A&M University Hagler Institute for Advanced Study (HIAS) のFaculty Fellow、Dr. Manfred Schartlは、この魚の生殖がどのようにして通常の雌雄両性生殖から逸れたのか、またどのようにしてアマゾン・モーリーが種としてその過程を無事に通過したのかをより深く理解するため、世界で初めてアマゾン・モーリーと、この独特な魚をつくり出した元の親種のゲノムのシーケンス解析を完了した。National Institutes of Healthの研究資金を受けて行われたこの研究の結果は、2018年2月12日付Nature Ecology & Evolutionオンライン版に掲載された。このオープンアクセス論文は、「Clonal Polymorphism and High Heterozygosity in the Celibate Genome of the Amazon Molly (アマゾン・モーリーの独身型ゲノムにおけるクローン多形性と高異型接合性)」と題されている。
報いられない愛に苦しまない種はない。しかし、アメリカのテキサス州在来種の個体全てがメスで無性生殖をすることで知られたカダヤシ属の淡水魚、アマゾン・モーリーは何千年も栄えてきた種である。最近、この魚のゲノムシーケンス解析が完了しており、その性の生物学的基礎情報から学ぶことは多いのではないかと研究者は期待している。テキサス州・メキシコ国境線に沿った淡水の河川はこの進化異常の種の棲息地になっており、この魚は自然の法則に反して受精なしで胚の発育と発達が起き、母親とまったく同一のクローンの娘だけができる単為生殖という自然の形式によって繁栄してきた。Texas A&M University Hagler Institute for Advanced Study (HIAS) のFaculty Fellow、Dr. Manfred Schartlは、この魚の生殖がどのようにして通常の雌雄両性生殖から逸れたのか、またどのようにしてアマゾン・モーリーが種としてその過程を無事に通過したのかをより深く理解するため、世界で初めてアマゾン・モーリーと、この独特な魚をつくり出した元の親種のゲノムのシーケンス解析を完了した。National Institutes of Healthの研究資金を受けて行われたこの研究の結果は、2018年2月12日付Nature Ecology & Evolutionオンライン版に掲載された。このオープンアクセス論文は、「Clonal Polymorphism and High Heterozygosity in the Celibate Genome of the Amazon Molly (アマゾン・モーリーの独身型ゲノムにおけるクローン多形性と高異型接合性)」と題されている。
 マサチューセッツ州Woods HoleのMarine Biological Laboratory (MBL) 他の研究機関の共同グループの研究によると、ヤツメウナギの脊髄損傷自然治癒にかかわっている遺伝子の多くが哺乳動物の末梢神経系の修復でも大きく関わっている。このことから、長期的に見れば、人間の脊髄損傷治療法向上のために同じ遺伝子を利用できるようになる可能性がある。 2018年1月15日付Scientific Reportsオンライン版に掲載された研究の著者の一人であり、MBL, Eugene Bell Center for Regenerative Biology and Tissue EngineeringのDirectorを務めるJennifer Morgan, PhDは、「研究で、哺乳動物の末梢神経系の再生の原動力となる転写因子の中心部と大きくダブることが突き止められた」と述べている。
マサチューセッツ州Woods HoleのMarine Biological Laboratory (MBL) 他の研究機関の共同グループの研究によると、ヤツメウナギの脊髄損傷自然治癒にかかわっている遺伝子の多くが哺乳動物の末梢神経系の修復でも大きく関わっている。このことから、長期的に見れば、人間の脊髄損傷治療法向上のために同じ遺伝子を利用できるようになる可能性がある。 2018年1月15日付Scientific Reportsオンライン版に掲載された研究の著者の一人であり、MBL, Eugene Bell Center for Regenerative Biology and Tissue EngineeringのDirectorを務めるJennifer Morgan, PhDは、「研究で、哺乳動物の末梢神経系の再生の原動力となる転写因子の中心部と大きくダブることが突き止められた」と述べている。
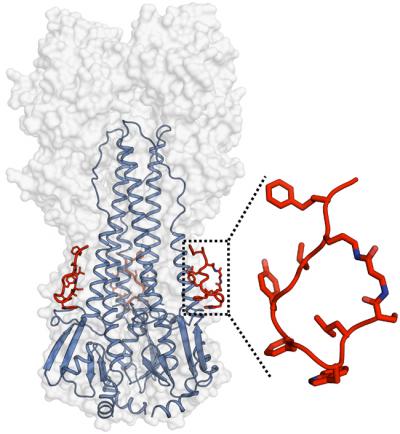 Scripps Research Institute (TSRI) とJanssen Research & Development (Janssen) の研究チームは、広いスペクトルのインフルエンザ・ウイルス株を中和する人工ペプチド分子を開発した。ペプチドはアミノ酸の短い鎖であり、タンパク質と似ているがもっと小さくて単純な構造である。この人工ペプチド分子はインフルエンザを標的とする医薬になる可能性を秘めている。毎年、世界中で50万人がインフルエンザで亡くなっており、アメリカ経済にとって病気欠勤日と生産性の損失で年間何十億ドルもの負担になっている。新しく開発されたペプチドは、アジア地域で何百人もの人に感染し、死者さえ出した鳥インフルエンザ株のH5N1や、2009年から2010年にかけて世界的に蔓延した豚インフルエンザのH1N1などを含め、世界的にもっとも一般的なグループ1のインフルエンザA型ウイルスの伝染力をブロックするものである。同チームは、最近発見された、事実上すべてのインフルエンザA型株を中和できる「スーパー抗体」という酵素がウイルスを捕捉する結合部位を取り入れたペプチドを設計した。抗体は大きなタンパク質であり、つくるのにはコストもかかり、人体への注入も注射か輸液で行わなければならない。しかし、「研究で開発されたペプチドは、将来的には錠剤タイプの医薬として利用できる可能性がある」。TSRIのHansen Professor of Structural Biologyで、共同主任研究員を務めるDr. Ian Wilsonは、「私達の新しい研究成果が示すように、広いスペクトラムでウイルスを中和する大きな分子の抗体と基本的に同じことを小さな分子でやらせるというのは将来性のある楽しみな戦略だ」と述べている。この新しいペプチドに関する研究論文は、2017年9月27日付Science誌オンライン版にFirst Release論文として掲載されており、「Potent Peptidic Fusion Inhibitors of Influenza Virus (インフルエンザ・ウイルスの融合阻害剤に有望なペプチド開発)」と題されている。このペプチド開発の基礎になった2つのインフルエンザ・スーパー抗体、FI6v3とCR9114はそれぞれ2011年、2012年に発見されており、それ以来、TSRIのDr. Wilson研究室は、Janssenその他の世界各国の構造生物学研究室と提携し、広いスペクトラムのウイルスを中和する抗体がどのようにインフルエンザ・ウイルスと結合するかを原子スケールでマップ化している。ワシントン大学のデイビッド・ベイカー博士が率いる研究チームは、最近これらの抗体構造データを用いて抗体よりも小さくインフルエンザウイルスに同様に結合し、広範なインフルエンザウイルスを中和する新しいタンパク質を設計した。Janssenの科学者と共同でTSRIが新たに取り組んだのは、インフルエンザウイルスの標的領域を標的とするより小さな非タンパク質様分子の開発でした。研究チームは、分子設計と合成、ウイルス結合試験、および原子レベルの構造評価を数回実施した後、潜在的なインフルエンザ阻止分子としてよく機能する環状の「環状」構造を持つ4つのペプチドセットを開発しました。このペプチドは、実験室実験でこれらのウイルスによる感染を中和する強力な能力と同様に、広範な群1群のインフルエンザAウイルスに対して高い結合親和性を示した。対象とする第1群のインフルエンザA型ウイルスにはH1、H2、H5およびH6サブタイプが含まれる。このペプチドはまた天然タンパク質に見出されないアミノ酸構築ブロックを組み込みこれはそれらの環状構造と同様に、そうでなければ血流からペプチド薬物を迅速に除去することができる酵素に対して比較的耐性であった。 P7と命名された4つのペプチドの中で最も最適化されたものは、マウスまたはヒト血漿に曝露されたとき、またはマウスに注入されたときに数時間生存した。「これらのペプチドは、薬物のような安定性を有し、動物モデルにおける抗ウイルス効果のさらなる試験のための良い候補となり、」研究の共同筆頭著者である博士ラメシュワー・U・カダム、ウィルソン研究所の上級ポスドク研究員は語ります。Janssenの主任科学者Jarek Juraszekと一緒にいます。ペプチドは模倣するように設計された抗体と同様に、インフルエンザウイルスの主要エンベロープタンパク質赤血球凝集素の下部にある疎水性ステム溝と呼ばれる部位に結合する。この部位の分子構造は、ウィルスが宿主細胞に浸透して感染を開始させる形状シフトプロセスにおいて重要な役割を果たすので、インフルエンザ株の中ではあまり変化しない傾向がある。 Kadam博士の構造評価によりペプチドがこの形状変化を防止し、それによって宿主細胞の浸透を妨げることが見出された。「感染の第1段階を標的とする治療は、感染の後期段階を標的とする既存の抗インフルエンザ薬を補完するだろう」とカダム博士は述べた。これらのペプチドは、それらが基づく抗体として包括的にそれらのウイルス標的に結合しない。例えば、グループ2のインフルエンザA型ウイルスでは、標的部位の重要な部分を遮断する赤血球凝集素上の糖分子を追い払う、または回避するより嵩張る抗体の能力が欠けていた。しかしKadamはさらなる研究により1型および2型インフルエンザAおよびインフルエンザB型株でさえも活性を有するペプチドが得られる可能性があると述べた。「抗体についての構造情報を利用して、ほとんど同じ分子の結合親和性とインフルエンザウィルスに対する中和の幅を持つ分子を作ることができたのは画期的なことです」とカダム博士は述べています。ウィルソン博士は、このような小分子でもこのような結果を得ることができるとの懐疑的な意見がありましたが、この研究は可能であることを証明しています。紙の他の共著者はBoerriesブランデンブルク、クリストフ・バイック、ヴィム・シェペンズ、バート・ケストレイン、バート・ストープス、ロブ・ブリーケン、ジャン・バーモンド、ウーター・グーシャー、チャン・タング、ロナルド・ボーゲルズ、ロバート・フリーセン、ジャアップ・ガウズミットと共同シニア研究者マリア・バンましたDongen【BioQuick News:Scientists Develop Broad-Spectrum Peptide Inhibitors of Influenza Virus】
Scripps Research Institute (TSRI) とJanssen Research & Development (Janssen) の研究チームは、広いスペクトルのインフルエンザ・ウイルス株を中和する人工ペプチド分子を開発した。ペプチドはアミノ酸の短い鎖であり、タンパク質と似ているがもっと小さくて単純な構造である。この人工ペプチド分子はインフルエンザを標的とする医薬になる可能性を秘めている。毎年、世界中で50万人がインフルエンザで亡くなっており、アメリカ経済にとって病気欠勤日と生産性の損失で年間何十億ドルもの負担になっている。新しく開発されたペプチドは、アジア地域で何百人もの人に感染し、死者さえ出した鳥インフルエンザ株のH5N1や、2009年から2010年にかけて世界的に蔓延した豚インフルエンザのH1N1などを含め、世界的にもっとも一般的なグループ1のインフルエンザA型ウイルスの伝染力をブロックするものである。同チームは、最近発見された、事実上すべてのインフルエンザA型株を中和できる「スーパー抗体」という酵素がウイルスを捕捉する結合部位を取り入れたペプチドを設計した。抗体は大きなタンパク質であり、つくるのにはコストもかかり、人体への注入も注射か輸液で行わなければならない。しかし、「研究で開発されたペプチドは、将来的には錠剤タイプの医薬として利用できる可能性がある」。TSRIのHansen Professor of Structural Biologyで、共同主任研究員を務めるDr. Ian Wilsonは、「私達の新しい研究成果が示すように、広いスペクトラムでウイルスを中和する大きな分子の抗体と基本的に同じことを小さな分子でやらせるというのは将来性のある楽しみな戦略だ」と述べている。この新しいペプチドに関する研究論文は、2017年9月27日付Science誌オンライン版にFirst Release論文として掲載されており、「Potent Peptidic Fusion Inhibitors of Influenza Virus (インフルエンザ・ウイルスの融合阻害剤に有望なペプチド開発)」と題されている。このペプチド開発の基礎になった2つのインフルエンザ・スーパー抗体、FI6v3とCR9114はそれぞれ2011年、2012年に発見されており、それ以来、TSRIのDr. Wilson研究室は、Janssenその他の世界各国の構造生物学研究室と提携し、広いスペクトラムのウイルスを中和する抗体がどのようにインフルエンザ・ウイルスと結合するかを原子スケールでマップ化している。ワシントン大学のデイビッド・ベイカー博士が率いる研究チームは、最近これらの抗体構造データを用いて抗体よりも小さくインフルエンザウイルスに同様に結合し、広範なインフルエンザウイルスを中和する新しいタンパク質を設計した。Janssenの科学者と共同でTSRIが新たに取り組んだのは、インフルエンザウイルスの標的領域を標的とするより小さな非タンパク質様分子の開発でした。研究チームは、分子設計と合成、ウイルス結合試験、および原子レベルの構造評価を数回実施した後、潜在的なインフルエンザ阻止分子としてよく機能する環状の「環状」構造を持つ4つのペプチドセットを開発しました。このペプチドは、実験室実験でこれらのウイルスによる感染を中和する強力な能力と同様に、広範な群1群のインフルエンザAウイルスに対して高い結合親和性を示した。対象とする第1群のインフルエンザA型ウイルスにはH1、H2、H5およびH6サブタイプが含まれる。このペプチドはまた天然タンパク質に見出されないアミノ酸構築ブロックを組み込みこれはそれらの環状構造と同様に、そうでなければ血流からペプチド薬物を迅速に除去することができる酵素に対して比較的耐性であった。 P7と命名された4つのペプチドの中で最も最適化されたものは、マウスまたはヒト血漿に曝露されたとき、またはマウスに注入されたときに数時間生存した。「これらのペプチドは、薬物のような安定性を有し、動物モデルにおける抗ウイルス効果のさらなる試験のための良い候補となり、」研究の共同筆頭著者である博士ラメシュワー・U・カダム、ウィルソン研究所の上級ポスドク研究員は語ります。Janssenの主任科学者Jarek Juraszekと一緒にいます。ペプチドは模倣するように設計された抗体と同様に、インフルエンザウイルスの主要エンベロープタンパク質赤血球凝集素の下部にある疎水性ステム溝と呼ばれる部位に結合する。この部位の分子構造は、ウィルスが宿主細胞に浸透して感染を開始させる形状シフトプロセスにおいて重要な役割を果たすので、インフルエンザ株の中ではあまり変化しない傾向がある。 Kadam博士の構造評価によりペプチドがこの形状変化を防止し、それによって宿主細胞の浸透を妨げることが見出された。「感染の第1段階を標的とする治療は、感染の後期段階を標的とする既存の抗インフルエンザ薬を補完するだろう」とカダム博士は述べた。これらのペプチドは、それらが基づく抗体として包括的にそれらのウイルス標的に結合しない。例えば、グループ2のインフルエンザA型ウイルスでは、標的部位の重要な部分を遮断する赤血球凝集素上の糖分子を追い払う、または回避するより嵩張る抗体の能力が欠けていた。しかしKadamはさらなる研究により1型および2型インフルエンザAおよびインフルエンザB型株でさえも活性を有するペプチドが得られる可能性があると述べた。「抗体についての構造情報を利用して、ほとんど同じ分子の結合親和性とインフルエンザウィルスに対する中和の幅を持つ分子を作ることができたのは画期的なことです」とカダム博士は述べています。ウィルソン博士は、このような小分子でもこのような結果を得ることができるとの懐疑的な意見がありましたが、この研究は可能であることを証明しています。紙の他の共著者はBoerriesブランデンブルク、クリストフ・バイック、ヴィム・シェペンズ、バート・ケストレイン、バート・ストープス、ロブ・ブリーケン、ジャン・バーモンド、ウーター・グーシャー、チャン・タング、ロナルド・ボーゲルズ、ロバート・フリーセン、ジャアップ・ガウズミットと共同シニア研究者マリア・バンましたDongen【BioQuick News:Scientists Develop Broad-Spectrum Peptide Inhibitors of Influenza Virus】
 動物の複雑さを決定する遺伝子、人間をミバエやウニよりも複雑な生き物にしている遺伝子が初めて突き止められた。ある動物の細胞が他の動物の類似の細胞よりもかなり複雑にできているということがあるのはなぜか、その秘密は特定のタンパク質と、そのタンパク質が細胞核内の動きを調節する能力にあるらしいことが明らかにされた。イギリスのUniversity of Portsmouthの生化学者、Dr. Colin Sharpeと同僚研究者の研究論文は、2017年9月25日付PLoS One誌オンライン版に掲載されている。このオープンアクセス論文は、「Relating Protein Functional Diversity to Cell Type Number Identifies Genes That Determine Dynamic Aspects of Chromatin Organisation As Potential Contributors to Organismal Complexity (タンパク質の機能多様性を細胞タイプの数と関連させることで、クロマチン構成の動的状態を決定する遺伝子を生物複雑性の要因となる可能性を突き止める)」と題されている。Dr. Sharpeは、「ほとんどの人が、ほ乳類、特に人間は虫やミバエよりも複雑だという考えにうなずくが、その理由をほんとうに知っている人はいない。長年、私も他の者もその疑問が頭から離れなかった。動物の複雑さを測る一般的な尺度の一つとして細胞の種類の数がある。しかし、遺伝子レベルでどのようにして複雑な生命体が構成されるのかについてはほとんど分かっていない。多細胞動物では遺伝子総数はわずかな違いしかなく、ゲノム中の遺伝子の数が動物の複雑さを決める因子とは考えられない。そうすると、他の因子を考えなければならない」と述べている。Dr. SharpeとMRes学生のDaniela Lopes Cardosoは、人、マカーク・サルから線虫、ミバエまで9種の動物のゲノム解析データを大量に調査し、それぞれが遺伝子レベルでどれほどの多様性を持っているかを計算した。その結果、少数のタンパク質が、他のタンパク質や細胞核内のDNAのパッケージであるクロマチンとの相互作用に優れていることに気づいた。Dr. Sharpeは、「その少数のタンパク質こそ、動物の複雑さの度合いが大きく異なる要因として考えられるようだ。私達は、DNAに直接作用して他の遺伝子を調節する遺伝子を見つけられものと予想していたがそうではなかった。実際にはクロマチンと相互作用する遺伝子を見つけたのだった。この研究の結果から、特定のタンパク質が相互作用しあって細胞核中のクロマチンの構成を動的に調節する能力が高くなることが動物の複雑さの決めてであることが示唆されている」と述べている。
動物の複雑さを決定する遺伝子、人間をミバエやウニよりも複雑な生き物にしている遺伝子が初めて突き止められた。ある動物の細胞が他の動物の類似の細胞よりもかなり複雑にできているということがあるのはなぜか、その秘密は特定のタンパク質と、そのタンパク質が細胞核内の動きを調節する能力にあるらしいことが明らかにされた。イギリスのUniversity of Portsmouthの生化学者、Dr. Colin Sharpeと同僚研究者の研究論文は、2017年9月25日付PLoS One誌オンライン版に掲載されている。このオープンアクセス論文は、「Relating Protein Functional Diversity to Cell Type Number Identifies Genes That Determine Dynamic Aspects of Chromatin Organisation As Potential Contributors to Organismal Complexity (タンパク質の機能多様性を細胞タイプの数と関連させることで、クロマチン構成の動的状態を決定する遺伝子を生物複雑性の要因となる可能性を突き止める)」と題されている。Dr. Sharpeは、「ほとんどの人が、ほ乳類、特に人間は虫やミバエよりも複雑だという考えにうなずくが、その理由をほんとうに知っている人はいない。長年、私も他の者もその疑問が頭から離れなかった。動物の複雑さを測る一般的な尺度の一つとして細胞の種類の数がある。しかし、遺伝子レベルでどのようにして複雑な生命体が構成されるのかについてはほとんど分かっていない。多細胞動物では遺伝子総数はわずかな違いしかなく、ゲノム中の遺伝子の数が動物の複雑さを決める因子とは考えられない。そうすると、他の因子を考えなければならない」と述べている。Dr. SharpeとMRes学生のDaniela Lopes Cardosoは、人、マカーク・サルから線虫、ミバエまで9種の動物のゲノム解析データを大量に調査し、それぞれが遺伝子レベルでどれほどの多様性を持っているかを計算した。その結果、少数のタンパク質が、他のタンパク質や細胞核内のDNAのパッケージであるクロマチンとの相互作用に優れていることに気づいた。Dr. Sharpeは、「その少数のタンパク質こそ、動物の複雑さの度合いが大きく異なる要因として考えられるようだ。私達は、DNAに直接作用して他の遺伝子を調節する遺伝子を見つけられものと予想していたがそうではなかった。実際にはクロマチンと相互作用する遺伝子を見つけたのだった。この研究の結果から、特定のタンパク質が相互作用しあって細胞核中のクロマチンの構成を動的に調節する能力が高くなることが動物の複雑さの決めてであることが示唆されている」と述べている。
 LSU Health New Orleans, Neuroscience Center of ExcellenceのBoyd ProfessorとDirectorを兼任するNicolas Bazan (photo), MD, PhDの率いる研究グループは、傷害や疾患に反応して細胞間情報伝達と神経炎症/免疫活動を同調させる、これまで知られていなかったクラスの化学物質を脳の中に見つけた。このクラスの化学物質は、elovanoids (ELVs) と呼ばれ、オメガ3極長鎖多価不飽和脂肪酸 (VLC-PUFAs, n-3) で構成されている生理活性的な化学的伝達物質である。
LSU Health New Orleans, Neuroscience Center of ExcellenceのBoyd ProfessorとDirectorを兼任するNicolas Bazan (photo), MD, PhDの率いる研究グループは、傷害や疾患に反応して細胞間情報伝達と神経炎症/免疫活動を同調させる、これまで知られていなかったクラスの化学物質を脳の中に見つけた。このクラスの化学物質は、elovanoids (ELVs) と呼ばれ、オメガ3極長鎖多価不飽和脂肪酸 (VLC-PUFAs, n-3) で構成されている生理活性的な化学的伝達物質である。