膵臓がんは、肺がん、大腸がんに次いで米国で3番目に死亡率の高いがんだが、その発生頻度ははるかに低くなっている。また、膵臓がんの幹細胞は、化学療法や新しい免疫療法などの従来の治療や標的治療に対して急速に耐性を獲得するため、効果的な治療が最も困難ながんの一つでもある。その結果、膵臓がんと診断された人の5年生存率はわずか10%だ。
カリフォルニア大学サンディエゴ校(UCSD)医学部とサンフォード再生医療コンソーシアムの研究者が率いる国際研究チームは、最も耐性の高い膵臓がん細胞が、通常は腫瘍を抑制するタンパク質群の1つを利用して、がん細胞が治療を回避してより速く成長するのを助けることにより、治療に抗する別の方法を明らかにした。
この論文は「Smarcd3は膵臓管状腺癌における代謝ランドスケープのエピジェネティックな調節因子である(Smarcd3 Is an Epigenetic Modulator of the Metabolic Landscape in Pancreatic Ductal Adenocarcinoma)」と題されている。
これまでの研究で、膵臓がんの治療抵抗性は、腫瘍細胞の不均一性、特に治療抵抗性を促す幹細胞の特性によって、従来の薬剤に対する反応が異なるために起こることが分かっている。今回の研究では、主任研究者のタニシュタ・レヤ博士(元UCSD医科大学薬学・医学教授、がん生物学部長)らが、ゲノム上の変化(遺伝子そのものに特有の変化)ではなく、エピゲノム(ゲノムに何をすべきかを伝える多数のタンパク質)の変化が、耐性化を促進している可能性について検討した。
現在、コロンビア大学生理学・細胞生物物理学教授、ハーバート・アーヴィング総合がんセンター・トランスレーショナル・リサーチ副所長のレヤ博士は、「膵臓がん幹細胞は、従来の治療法に抵抗し腫瘍の再発を促す攻撃的ながん細胞で、エピジェネティクス制御により自己保護し生存と成長を促進している。我々は、がん幹細胞が治療抵抗性を理解するために使用する基本的なツールやメカニズムを明らかにし、それを回避する方法を探したいと考えた。」と述べている。
レヤ博士らはSMARCD3に着目した。SMARCD3はDNAとタンパク質が混在して染色体を形成するクロマチンを制御するSWI/SNFファミリーのメンバーであり、発生における幹細胞の機能に必要なタンパク質であると考えられている。しかし、SWI-SNFサブユニットはしばしば腫瘍抑制因子として働くのに対し、SMARCD3はがんにおいて増幅されており、特に膵臓がん幹細胞に多く、ヒトの病気では発現が上昇または増加していることが判明した。また、膵臓がんのモデルでSMARCD3を欠失させると、このタンパク質の消失によって腫瘍の成長が抑えられ、特に化学療法を行った場合の生存率が改善された。
「重要なことは、SMARCD3が、がんの治療抵抗性や予後不良に関連する脂質や脂肪酸の代謝を制御することを見出したことだ。我々のデータは、治療抵抗性の膵臓がん細胞が、抗がん剤治療を回避して活発に増殖できるような代謝環境を確保するために、SMARCD3が必要であることを示唆している。このことから、SMARCD3は治療薬として期待できる新しいターゲットと言える。」と、レヤ博士は語っている。
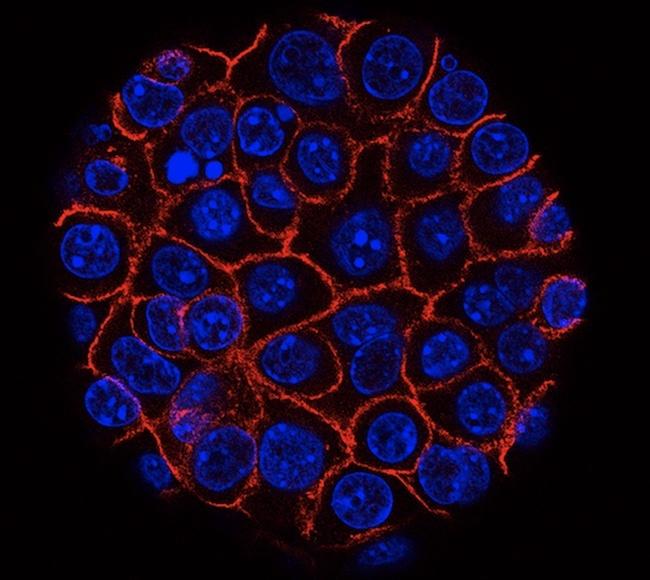
イメージ:
膵臓がん細胞(核は青色)が膜(赤色)に包まれた球体として成長している様子を示している。(Credit: National Cancer Institute)