UCSFの研究者ら、妊娠初期に活性化しマウスの出産時期に影響する分子タイマーを発見
一般的な人間の妊娠期間は40週とされていますが、多くの親がご存じのように、これはあくまで目安に過ぎません。赤ちゃんは予測困難なタイミングで生まれることが多く、正常な妊娠期間は38週から42週の範囲とされています。また、全出産の10%は在胎37週未満の「早産」に該当し、この場合、さまざまな合併症のリスクが高まります。このたび、カリフォルニア大学サンフランシスコ校(UCSF)の研究者らは、マウスにおいて出産時期の制御に関与する「分子タイマー」を発見しました。驚くべきことに、このタイマーは妊娠の最初の数日に子宮内で活性化されます。もし同様の分子機構がヒトにも当てはまるとすれば、早産リスクのある女性を特定するための新しい検査法や、そのリスクを軽減する介入手段の開発につながる可能性があります。
「早産は世界的に非常に大きな問題ですが、そのメカニズムは長らく不明でした。我々の研究が、その根本的な仕組みに光を当てるきっかけになればと願っています。」と語るのは、UCSF臨床検査医学教授であり、本研究の責任著者であるエイドリアン・アールバッカー博士(Adrian Erlebacher MD, PhD)です。本研究成果は2025年1月21日付で『Cell』誌に掲載されました。論文タイトルは「KDM6B-Dependent Epigenetic Programming of Uterine Fibroblasts in Early Pregnancy Regulates Parturition Timing in Mice(妊娠初期における子宮線維芽細胞のKDM6B依存性エピジェネティックプログラミングがマウスの出産時期を制御する)」です。
妊娠中のDNAパッケージング
妊娠を通じて、女性の体では大規模な生物学的変化が起こり、子宮内では数百もの遺伝子の活性が増減します。
アールバッカー博士とその研究室のメンバーは、遺伝子の活性を調節するタンパク質「KDM6B」に注目していました。彼らは、妊娠中にKDM6Bが陣痛への移行に関与する遺伝子群を制御するのではないかと考えました。
チームは、KDM6Bを阻害すると、マウスの妊娠期間が長くなり、出産が通常より遅れることに気付きました。
当初、科学者らはKDM6Bが妊娠後期に子宮上皮細胞(ホルモンを産生し、陣痛を誘発することが知られている)における遺伝子を活性化するのではないかと考えていました。しかし、さまざまな細胞型に対して詳細な解析を行ったところ、KDM6Bが妊娠期間に与える影響は、異なる細胞型である線維芽細胞に関連していることがわかりました。線維芽細胞は構造を担う細胞で、通常は陣痛の調節に関与するとは考えられていませんでした。さらに、KDM6Bは妊娠の最初の数日にこれらの線維芽細胞を制御していました。
「我々の発見は、出産時期の調節における子宮線維芽細胞の意外な役割を浮き彫りにしています。」と語るのは、UCSFで大学院生としてこの研究を主導したタラ・マッキンタイア博士(Tara McIntyre, PhD)です。「これは全く予想外の発見であり、労働開始を促す細胞やプロセスに関する我々の理解を根本から覆すものでした。」
分子タイマーの可能性?
KDM6Bは、ヒストンと呼ばれるDNAを細胞内で整理・パッケージングする構造からメチル基を除去することで機能します。この作用によりDNAが他の因子にとってアクセスしやすくなり、周囲の遺伝子の発現が活性化されます。
マウスを使ったさらなる実験により、受精直後に子宮の線維芽細胞内で特定の遺伝子周辺のヒストンにメチル基がより多く付加されることが明らかになりました。このメチル化によりこれらの遺伝子は不活性なままとなり、妊娠の維持が可能になります。
妊娠が進行するにつれて、これらヒストンのメチル化レベルはゆっくりと、しかし着実に減少していきます。そして、メチル化が十分に低下すると、近傍の遺伝子――たとえば陣痛に関連する遺伝子――が活性化されるのです。この減少過程はKDM6Bを必要とせず、まるで「タイマー」のように機能します。
「基本的に起こっていることは、このタイマーが妊娠初期に巻かれ、その後徐々に解けていくということです。」とアールバッカー博士は説明します。
「ヒストンのメチル化が十分に減ると、近くの遺伝子がオンになるのです。」
研究チームがKDM6Bを阻害した際には、妊娠初期に特定の遺伝子近傍のヒストンに過剰なメチル化が生じました。この「初期設定点」が高すぎるため、メチル化が進行しても遺伝子の活性化が間に合わず、陣痛の開始が遅れることとなりました。
シグナルは早産と関連する可能性
今回の研究では早産そのものを直接的に扱ったわけではありませんが、新たに発見された分子タイマーは、ヒトの妊娠期間の長さを制御する役割を担っている可能性があります。
「ここからの最大の疑問は、これらのプロセスが人間にも当てはまるかどうかです。」とアールバッカー博士は語ります。「もしそうなら、妊娠期間を予測したり制御したりする手段になるかもしれません。」
仮に、今回明らかとなった分子シグナルがヒトで乱れることがあるとすれば、それは早産のリスクと関連している可能性があると彼のチームは考えています。たとえば、一部の女性では妊娠開始時点でヒストンのメチル化レベルが通常より低いことがあり得ます。その場合、メチル化の「侵食」が早く進行しすぎて、陣痛に関連する遺伝子が早期に活性化されてしまう可能性があります。
アールバッカー博士は、これまでの早産研究の多くが、妊婦が実際に陣痛を迎える直前のタイミングに焦点を当てていたことを指摘します。今回の研究結果は、妊娠のはるか初期段階こそが重要であることを示しており、新たな研究の方向性を切り開く可能性を示唆しています。
著者について
本研究の他の著者には、UCSF所属のオマー・バルデス(Omar Valdez)、ネイサン・コチャー(Nathan Kochhar)、ブリタニー・デヴィッドソン(Brittany Davidson)、ブシュラ・サマド(Bushra Samad MS)、ロンフイ・チウ(Longhui Qiu MB)、アレクシス・コンブ(Alexis Combes PhD)らが含まれます。また、MDアンダーソンがんセンター所属のケネス・フー博士(Kenneth Hu PhD)も共著者です。
画像;末尾の他の画像とキャプションを参照。
[News release] [Cell abstract]
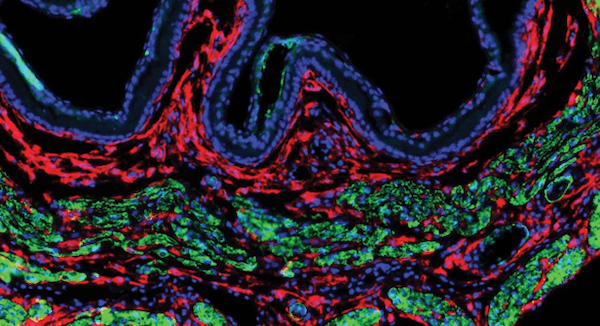
画像;上の画像では、マウスの子宮から採取した子宮線維芽細胞が赤く示されている。UCSFの科学者たちは、これらの細胞の出産関連遺伝子が、妊娠中に一時的に分子フラグで口止めされていることを発見した。これらのフラグは妊娠が継続するにつれて徐々に取り除かれ、出産の時期になると消える。その時点で、出産関連遺伝子がオンになり、子宮線維芽細胞が出産プロセスを活性化する。 (Credit: Omar Valdez/Erlebacher Lab)



