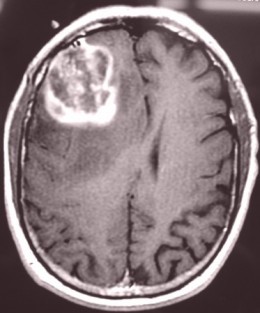
外傷からの感染や、脳卒中など脳損傷の治癒過程は、膠芽腫の成長を促進する可能性がある。 2021年1月4日にNature Cancerのオンラインで公開されたこの調査結果は、トロント大学病院、ザ・ホスピタル・フォー・シック・チルドレン(SickKids)およびプリンセスマーガレット癌センターの学際的な研究者チームによって報告された。 この研究者らは、膠芽腫として知られる一般的な脳腫瘍に焦点を当てた、カナダ全土の癌に立ち向かうカナダドリームチームの一員だ。「我々のデータは、脳内の特定の細胞の突然変異が損傷によって変化して腫瘍を引き起こす可能性があることを示唆している」とトロント大学テマーティ医学部の脳神経外科部門の責任者であり、SickKids の発達および幹細胞生物学プログラムの上級科学者でもあるドリームチームリーダーのPeter Dirks 医学博士は述べている。
テマーティ医学部およびトロント大学ドネリー細胞生体分子研究センターの分子遺伝学教授であるGary Bader 博士、およびテマーティ医学部の医学生物物理学の准教授であるTrevor Pugh 博士もこの研究を主導した。
調査結果は、診断後の平均寿命が15か月で、現在治療の選択肢が限られている膠芽腫患者の新しい治療法につながる可能性がある。 このNature Cancerの論文は、「発達および損傷反応の勾配転写状態は、膠芽腫の不均一性を支える機能的脆弱性を定義する(Gradient of Developmental and Injury Response Transcriptional States Defines Functional Vulnerabilities Underpinning Glioblastoma Heterogeneity.)」と題されている。
この結果に基づき、この研究者らは、「神経膠芽腫は、神経創傷応答転写プログラムに基づき神経膠芽腫幹細胞から成長する。 これは、新しい治療法開発の有望なターゲットだ。」と提案する。
「膠芽腫は、治癒を止めることのない傷と考えることができる」とDirks博士は述べた。 「これが癌の発生と成長の仕方について我々に教えてくれる。そしてそれは傷害と炎症反応に焦点を当てることによって治療についての全く新しい考えを開くものだ。」
この研究者らは、最新のシングルセルRNAシーケンスと機械学習技術を適用して、神経膠芽腫幹細胞の分子構成をマッピングした。これは、Dirks博士のチームが、治療後の腫瘍の発生と再発の原因であることを以前に示したものだ。
彼らは、炎症の分子的特徴を持ち、患者の腫瘍内の他の癌幹細胞と混ざり合っている神経膠芽腫幹細胞の新しい亜集団を発見した。 いくつかの神経膠芽腫は、損傷により失われた細胞を置き換える新しい細胞を生成する通常の組織治癒プロセスが突然変異によって脱線したときに形成され始めることを示唆している(おそらく患者が症候性になる何年も前に)。 変異細胞が創傷治癒に関与すると、正常な制御が壊れて腫瘍の成長が促進されるため、増殖を止めることはできない。
「目標は、膠芽腫幹細胞を殺す薬を特定することだ」と、大学院生のBader 博士は述べた。 「しかし、これらの細胞をより効果的に標的化できるようにするためには、まずこれらの細胞の分子的性質を理解する必要があった。」
研究チームは26人の患者の腫瘍から神経膠芽腫幹細胞を収集し、ラボでそれらを拡張して、分析に十分な数の希少細胞を取得した。 約70,000の細胞が、個々の細胞でどの遺伝子がオンになっているのかを検出するシングルセルRNAシーケンスによって分析された。これは、Pugh 博士の研究室の大学院生であるLaura Richards 氏が主導した取り組みだ。
このデータは、広範な疾患の不均一性を示した。つまり、各腫瘍には分子的に異なる癌幹細胞の複数の亜集団が含まれており、既存の治療法ではすべての異なるサブクローンを一掃できないため、再発する可能性がある。
よく見ると、各腫瘍には、「発達」および「傷害反応」と呼ばれる2つの異なる分子状態のいずれか、または2つの間の勾配があることが明らかになった。
発達状態は神経膠芽腫幹細胞の特徴であり、出生前の脳内で急速に分裂している幹細胞の状態に似ている。
しかし、後者の状態は驚きだった。 研究者らは、免疫経路のアップレギュレーションと、創傷治癒過程を示すインターフェロンやTNF-αなどの炎症マーカーを示したため、これを「傷害反応」と名付けた。
これらの免疫シグネチャーは、バルク細胞測定を探す古い方法では見逃されたが、新しいシングルセル技術のおかげで取得できた。
一方、トロント大学のStephane Angers 教授の研究室が主導した実験では、2つ異なるタイプの遺伝子ノックアウトに対して脆弱であることが明らかになり、以前は膠芽腫と見なされなかった炎症に関連する治療標的が明らかになった。
最終的に、2つの状態の相対的な混合は患者固有であることがわかった。これは、各腫瘍が勾配の発達端または損傷反応端のいずれかに偏っていることを意味する。 研究者らは現在、これらの偏りを調整された治療法に向けることを目指している。
「我々は現在、この勾配のさまざまなポイントで効果的な薬を探している」と、オンタリオ癌研究所のゲノミクスディレクターでもあるPugh 博士は述べた。 「ここには、精密医療が患者の腫瘍を単一細胞レベルで解剖し、同時に複数の癌幹細胞サブクローンを取り出すことができるドラッグカクテルを設計するリアルな機会がある。」
BioQuick News:Glioblastoma Could Be Linked to Combination of Mutational Change in Key Cells and Healing Process After Brain Injury, New Study Suggests; Findings May Lay Foundation for Precision Medicine Efforts to Treat Deadly Disease