ノースカロライナ大学(UNC)チャペルヒル校の科学者らは、ヒトの消化管から採取した個々の単一細胞で発現する遺伝子の配列を決定し、新しい細胞型の特徴を発見するとともに、栄養吸収や免疫防御などの重要な細胞機能についての知見を得た。緊張すると腸はそれを感じるかもしれない。唐辛子を食べると腸が反乱を起こすかもしれないが、ある人は何を食べても美味しく感じる。ある人はイブプロフェンを飲んでも何も影響がないが、ある人は腹から出血し、痛みの緩和ができないかもしれない。それはなぜだろうか?その答えは、我々は皆違うからだ。では、具体的にどのように違うのか、そしてその違いは健康や病気に対してどのような意味を持つのか。これらに答えるのは難しいのだが、UNC医科大学のスコット・マグネス博士の研究室では、興味深い科学的な答えを発見した。
マグネス研究員は、3人の臓器提供者から採取したヒトの消化管全体を用いて、腸のすべての領域で細胞の種類がどのように異なるか、細胞の機能を明らかにし、これらの細胞間および個人間の遺伝子発現の違いを初めて明らかにしたのである。2022年2月14日にCellular and Molecular Gastroenterology and Hepatology誌にオンライン掲載されたこの研究は、腸の健康の様々な側面を、これまで以上に高解像度でより正確に探求するための扉を開くものだ。この論文は「健康な成人小腸と結腸上皮の近位から遠位までの調査(A Proximal-to-Distal Survey of Healthy Adult Human Small Intestine and Colon Epithelium by Single-Cell Transcriptomics)」と題されている。
「我々の研究室では、栄養吸収、寄生虫からの保護、食行動や腸の運動を制御する粘液やホルモンの生成など、重要なプロセスにおける各細胞タイプの機能を知ることが可能であることを示した」「我々はまた、腸内膜が受容体やセンサーを通して環境とどのように相互作用するか、そして、薬がどのように異なる細胞種と相互作用するかについて学んだ。」と、UNC-NC州立合同生物工学科の准教授で論文の主執筆者のマグネス博士は述べている。
敏感な腸
よくある医薬品のCMで、下痢や嘔吐、腸管出血などの副作用が起こる可能性があることを、声優が楽しげに語るナレーションを思い浮かべてほしい。マグネス研究室では、こうした副作用がなぜ起こるのかを、個々の細胞、その機能、場所、遺伝子のレベルまで掘り下げて理解しようとしている。
この研究でマグネス研究室が注目したのは、腸と大腸の内部を他のものから分離している単細胞の厚い層である上皮である。他の細胞集団や微生物叢と同様、上皮は人間の健康にとって非常に重要であり、長年にわたって科学者らはその研究を続けてきた。しかし、これまでは、消化管のごく一部(通常は大腸や小腸の限られた部位)から、米粒大の小さな生検を採取することしかできなかった。
「このような探査は、宇宙からアメリカを見て、マサチューセッツ、オクラホマ、カリフォルニアで起こっていることだけを調査するようなものだ」と、マグネス博士は言う。「この国について本当に知るためには、すべてを見たいと思った。」
マグネス博士は、マグネス研究室の研修生である共同筆頭著者、ジョセフ・バークラフ博士と大学院生、ジャレット・ブリトン氏に信頼を寄せている。
「我々は、細胞の位置を特定するだけでなく、どの種類の細胞がどのような働きをするのか、そしてその理由を正確に知りたいと考えている」「つまり、地図に例えると、『あ、ノースカロライナ州だ』というだけではダメなのだ。バーベキューがおいしいのはどこなのか。できるだけ多くのことを知るために、地上の景色を見たいのだ」と、バークラフ博士は語っている。
以前は、研究者は、すべての上皮細胞のタイプを識別し、これらの細胞のいくつかの一般的な特徴を学ぶために、それらの米サイズの生検をマッシュアップしていた。マグネス博士のアプローチは、下部消化管(小腸と大腸)のあらゆる部分から何千もの個々の細胞を採取してアトラスを作成し、それぞれの細胞が発現する遺伝子を通じて、これらの細胞の潜在的役割を研究することであった。このようなことがすべてわかれば、腸管上皮に関する科学的知識が深まり、他の科学者が生物学や病気、医薬品の副作用という不幸なシナリオにおける各細胞の機能を探求するきっかけになると期待される。
マグネス博士が、このように個々の細胞を深く掘り下げるために必要としたのは、より優れた技術とヒトの消化管全体であった。
データの生物学
UNC チャペルヒル校は、数年前に最先端の RNA 配列解析技術を取得し、UNC 消化器病・生物学センターを通じて Advanced Analytics Core Facility を設立し、最先端の機器を使用できる研究者、スタッフ、ポスドク、 学生などの科学的・知的能力を開発した。
マグネス研究員は、HonorBridgeの臓器提供サービスとの研究契約を通じて、ヒトの消化管を入手した。腸が移植用に摘出され、より優先順位の高いグループから要求されない場合、HonorBridgeのスタッフがマグネスグループと調整して、移植用の臓器を研究用に提供するのである。
回収から6〜8時間後、マグネス研究所は長さ15〜30フィートほどの無傷の腸管を受け取る。上皮層は、細胞の厚さが1個しかないにもかかわらず、長くつながった1つの組織であるため、これを除去する。そして、酵素を使って上皮を個々の細胞に分解する。今回の研究では、3人のドナーの臓器について、この作業を繰り返した。
遺伝子発現の特徴を明らかにするために、マグネス教授のグループはまず、各細胞を分離したままRNAを抽出し、各腸の細胞がどの遺伝子をどの程度発現しているかのスナップショットを撮るシングルセルシークエンシングを実行した。
「各細胞から得られる画像は、その細胞が作り出すあらゆる種類の遺伝子のモザイクであり、この遺伝子の相補性が、その細胞がどの種類の細胞であるか、また潜在的に何をしているかを示す『サイン』を作り出す」「幹細胞なのか、粘液細胞なのか、ホルモン産生細胞なのか、免疫シグナル伝達細胞なのか。」と、マグネス博士は語っている。
また、バークラフ博士は、「消化管全体の細胞の種類の違いを見ることができ、3人の異なる人の同じ種類の細胞で異なる遺伝子発現レベルを見ることができる。個々の細胞でオン・オフされる遺伝子の異なるセットを見ることができるのだ。このようにして、例えば、ある特定の食物や薬物に対して毒性を示す人と示さない人がいる理由を理解することができるかもしれない」と述べている。
この種の研究の大きな問題は、生成されるデータ量が膨大であることだ。シングルセルシーケンスでは、たった1つの細胞で約11,000の『リード』、つまり遺伝子産物の個別サンプルを採取する。また、何千もの個別細胞で、それぞれオンまたはオフになる2万以上のヒト遺伝子の異なる組み合わせを採取する。このため、12,590個の細胞について140,000,000のデータポイントを作成し、科学者が膨大な量の情報を理解できるように可視化する必要がある。
「人間の脳は2次元しか理解できないので、3次元は難しい」とマグネス博士は言う。「さらに時間が経過すると、1つの細胞が何をしようとしているのかを理解するのはさらに難しくなる。我々の実験が生み出したデータ量は、基本的に数百万次元を一度に処理するものだった」。
ブリトン氏は、データをフィルタリングして、消化管のあらゆる部分の細胞集団を含む管理可能なデータセットを作り出すために、計算技術を考案した。そして、マグネス博士をはじめとする研究者がすでに把握していた各細胞の種類をもとに、ブリトン氏は各領域の細胞の種類を計算で特定することができた。そして、これらのデータを人間が理解し解釈できるようにプロットした。
膨大なデータを整理することで、それぞれの細胞タイプについて多くのことを知ることができた。例えば、40年前に発見された『タフト細胞』は、細胞の表面に毛束があるように見えることからこの名がついた。
この細胞は、舌の味蕾(みらい)と同じような遺伝子を発現していることが判明した。他の研究者らは、この房状細胞が虫の感染を感知して、免疫系にシグナルを送り、戦争を始めることを発見した。マグネス研究室は、房細胞が、他の種類の腸の内容物を感知して『味わう』ために重要だと考えられる一連の遺伝子を発現していることを明らかにし、必要であれば腸が免疫系にシグナルを送ることができるようにしたのである。これは、腸内に寄生虫がいるかどうかを感知する機能よりも、はるかに広範な機能であると考えられる。
「我々は、細胞の種類と、それらが発現する遺伝子の一つ一つを個別に記述しただけでなく、潜在的な機能も調べた」「腸管粘液というのは、細胞を保護するための複雑な混合物だが、どの細胞が、どの程度、消化管のどの部位で、様々なムチン蛋白質を発現しているのかを明らかにしたのだ。食べ物を消化する特定の酵素が発現している場所を調べた。抗炎症遺伝子が発現している細胞や、シナプス遺伝子を調べたところ、腸はおそらく神経とつながっていて、体の他の部分と会話ができるようになっていることが分かった。アクアポリンという、腸管膜を通して水を運ぶのに関与するタンパク質を調べた」とバクラフ博士は述べている。
マグネス博士のグループが発見したのは、生検サンプルを寄せ集めても、これまで評価されなかった、全く新しいレベルの潜在的機能のバリエーションだった。
研究者らは、他の細胞や分子、腸内環境とのコミュニケーションに用いられる細胞表面タンパク質である上皮レセプターをすべて探索した。マグネス博士らは、どの受容体がどの種類の細胞で最も多く発現しているかを調べ、細胞が栄養素や微生物、毒素、薬物などの腸内物質とどのように相互作用しているかを新たに描き出したのである。
「我々が知る限り、3人の完全なドナーから採取したヒトの腸の長さに渡ってこの種の分析を行ったのは、我々が初めてだ。」「我々は、それぞれの細胞の種類を見て、どの医薬品が、どの細胞の種類に影響を与えるかを個別に予測することができる。」と、ブリトン氏は述べた。
例えば、炎症性腸疾患(IBD)の治療薬の一群がある。これらの薬は、炎症を誘発する特定の免疫細胞という特定のターゲットを叩くように設計されている。しかし、マグネス研究員は、上皮細胞の中には、標的となる免疫細胞と同じ遺伝子を発現しているものがあることを突き止めた。この発見は、上皮細胞には意図しない『オフターゲット』作用が存在し、副作用につながる可能性があることを示している。
「これは知られていなかったことだ」とバクラフ博士は述べた。「多くの薬剤が消化器系の悪い副作用を持っている。そしてそれは、薬が消化管全長に渡って個々の細胞に影響を及ぼしているからかもしれない。我々は、これらのレセプターがどこで最も発現しているか、どの細胞タイプで発現しているかを明らかにしている。」
このような知識は、マグネス研究所の初期研究の成果の一つに過ぎない。
「我々は発見したことを科学、医学、薬学の分野で活用してもらいたいと考えている」とマグネス博士は述べている。「我々は、各細胞タイプに整然と対応する分析的アプローチを採用し、多くの科学者にとって読みやすくアクセスしやすいスプレッドシートを作成し、この種の高解像度、高精度アプローチで発見できるいくつかの事例を示した。」
この研究は、国立衛生研究所、キャサリン・E・ブラード慈善信託、クローン病・大腸炎財団、UNC-チャペルヒルの大学癌研究基金から資金提供を受けている。
[News release] [Cellular and Molecular Gastroenterology and Hepatology article] [Cellular and Molecular Gastroenterology and Hepatology abstract]
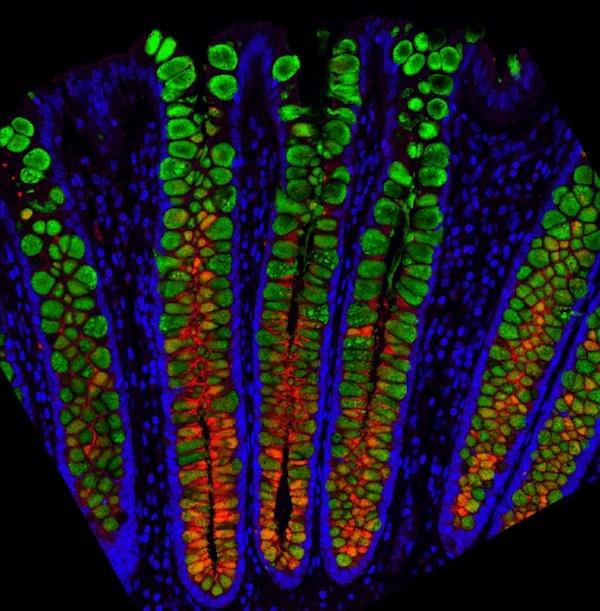
トップ画像
クリプト常在血管の杯細胞にはMUC5b(赤)、すべての杯細胞にはMUC2(緑)というタンパク質が存在する。マグネスグループは、大腸を保護する粘液層に寄与するムチン蛋白質を蛍光染色した。ここでは、固定したヒト結腸の薄切片を2つの異なるムチンタンパク質で染色している。MUC2は緑色、MUC5Bは赤色で、すべての核は青色で染色されている。これは、大腸の小嚢の底部と頂部で粘液の含有量が異なる可能性があることを示しており、単一細胞の遺伝子配列決定から得られた結果を裏付けるものである。(Credit: Magness Lab, UNC School of Medicine)
グラフィカルアブストラクト



