狂犬病ウイルスは毎年59,000人を殺し、その犠牲者の多くは子供だ。一部の被害者(特に子供達)は、手遅れになるまで気づかないことが多い。その他の人々にとって、高額な狂犬病治療プランは論外だ。平均3,800ドルの費用が掛かる治療は誰もが利用可能ではなく、世界中のほとんどの人々に考えられない経済的負担をもたらする。一方で狂犬病ワクチンは治療よりもはるかに手頃な価格で投与が簡単だ。しかし、これらのワクチンには大きな欠点もある。
「狂犬病ワクチンは生涯にわたる保護を提供しない。ペットに3歳まで毎年接種する必要がある。」 「現在、人間と家畜のための狂犬病ワクチンは、死んだウイルスから作られている。しかし、この不活化プロセスにより、分子の形が崩れる可能性がある。そのため、これらのワクチンは免疫系に適切な形を示していない。より良い形でより構造化されたワクチンを作った場合、免疫はより長く続くだろうか?」とラホーヤ免疫学研究所(LJI)のエリカ・オルマン サファイア教授は述べている。
パスツール研究所のエルヴェ・ブーリィ博士が率いるチームと協力して、サファイア教授と彼女のチームは、より良いワクチン設計への道を発見したという。Science Advances で2022年6月17日に公開された新研究で、この研究者らは、脆弱な「三量体」の形で狂犬病ウイルス糖タンパク質を調べた最初の高解像度研究の1つを共有している。このオープンアクセス論文は、「狂犬病ウイルス糖タンパク質三量体が融合前特異的中和抗体に結合した構造(Structure of the Rabies Virus Glycoprotein Trimer Bound to a Prefusion-Specific Neutralizing Antibody.)」と題されている。
「狂犬病糖タンパク質は、狂犬病がその表面に発現する唯一のタンパク質だ。つまり、感染時に中和抗体の主要な標的になるだろう」「狂犬病は我々が知っている中で最も致命的なウイルスだ。 それは我々の歴史の大部分を占めている。我々は何百年もの間、その曲者と一緒に暮らしてきた」と、LJIの社長兼CEOを兼務するサフィア博士は付け加えた。
「しかし、科学者はその表面分子の組織化を観察したことがない。 より効果的なワクチンと治療法を作るためにその構造を理解すること、そして狂犬病やそのような他のウイルスがどのように細胞に侵入するかを理解することが重要だ。」と、研究の筆頭著者を務めるLJIポスドクのヘザー・キャラウェイ博士は述べている。
シェイプシフター
科学者は、狂犬病ワクチンが長期的な予防を提供しない理由を正確には知らないが、その形状変化タンパク質が問題であることは知っている。
スイスアーミーナイフのように、狂犬病糖タンパク質には、必要に応じて展開して上向きに反転する配列がある。 糖タンパク質は、融合前(宿主細胞と融合する前)と融合後の形態の間を行き来する可能性がある。 また、三量体構造(3つのコピーが束になっている)からモノマー(1つのコピー自体)に変化して、バラバラになることもある。
この形を変えることは狂犬病に一種の不可視のマントを与える。 ヒト抗体は、タンパク質上の単一の部位を認識するように作られている。 タンパク質がそれらの部位を隠したり動かしたりするために変化するとき、これらは従うことができない。
この新研究は、抗体保護の標的となる正しい糖タンパク質の形態の重要な画像を科学者に提供するものだ。
ついに糖タンパク質を捕獲
キャラウェイ博士は3年間にわたって、狂犬病の糖タンパク質を三量体の形で安定化および凍結するために取り組んだ。この「融合前」の形態は、糖タンパク質がヒト細胞に感染する前にとる形だ。
キャラウェイ博士は、糖タンパク質をヒト抗体と組み合わせた。これにより、ウイルス構造が抗体攻撃に対して脆弱な1つの部位を特定することができた。次に、研究者は、LJIの最先端の低温電子顕微鏡装置を使用して糖タンパク質の3D画像をキャプチャした。
新しい3D構造は、研究者がこれまでに見たことのない、いくつかの重要な機能を強調している。重要なことに、この構造は、融合ペプチドと呼ばれるウイルス構造の2つの重要な部分を示しており、実際にどのように見えるかを示している。これらの2つの配列は、糖タンパク質の下部をウイルス膜にリンクするが、感染中に標的細胞に投射する。これらのシーケンスの安定した画像を取得することは非常に困難だ。実際、他の狂犬病研究者は、糖タンパク質の画像を取得するためにそれらを切断しなければならなかった。
キャラウェイ博士は、界面活性剤分子に狂犬病糖タンパク質を取り込むことでこの問題を解決した。 「これにより、感染中に融合配列が上向きにスナップする前に、融合配列がどのように付着しているかを確認できる」とサファイア教授は述べている。
科学者はこのウイルスの構造を明確に把握しているので、ウイルスを標的とする抗体の作り方を体に伝えるワクチンをより適切に設計できる。
「4つ以上の異なるタンパク質の形にさらされるのではなく、免疫システムは実際には1つ、つまり正しいものを見る必要がある」とキャラウェイ博士は語る。 「これはより良いワクチンにつながる可能性がある。」
ウイルスファミリーの防止
サファイア教授は、より強力で幅広い免疫が、獣医や野生生物労働者などの動物と定期的に接触している人々や、誤って猛威を振るう動物と接触する可能性のある何十億もの人々を助けることができると期待している。狂犬病は南極大陸を除くすべての大陸で風土病であり、犬、アライグマ、コウモリ、スカンクなどの多くの種に感染する。
この新研究はまた、狂犬病や人間と他の哺乳類の間で広がる可能性のある同様のウイルスを含むリッサウイルス属全体から保護するためのワクチンへの扉を開くかもしれない。
次のステップは、中和抗体とともに狂犬病ウイルスとその近縁種のより多くの画像をキャプチャすることだ。キャラウェイ博士は、科学者がこれらの構造のいくつかを解決することに取り組んでいると言う。これは、リッサウイルスが共通して持っている抗体標的を明らかにする可能性がある。
「以前はこのようなコンフォメーション状態の狂犬病ウイルスのこれらの構造がなかったため、広域ワクチンを設計することは困難だった」とキャラウェイ博士は述べた。
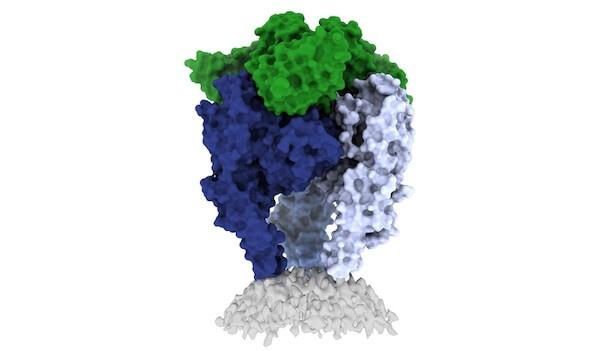
画像
ラホーヤ免疫学研究所とパスツール研究所の科学者らは、狂犬病ウイルス糖タンパク質の構造に光を当てている。(クレジット:画像提供: Heather Callaway, PhD, LJI)
[News release] [Science Advances article]