今後の医薬品開発の方向性に関して、私は創薬の今後について、核酸医薬とAIを用いた低分子・中分子創薬と、再生医療を応用し作成したiPS細胞を利用した創薬スクリーニングで見つかったリード化合物をDDS技術で疾患ターゲット部位に送る方法が中心になってくると話しました。リード化合物をDDSの技術で疾患のターゲット部位に送る方法が確立すると、個別化医療の目的がほぼ達成されると考えます。
リード化合物の探索は核酸医薬、AIと再生医療の応用で時間とコストは軽減されますが、医薬品開発のところに、DDS化する部分が新たに加わることで時間とコストが掛かります。
そこで、今の医薬品開発の流れをもう一度見直してみましょう。厚生労働省が「臨床研究に関する現状と最近の動向」で医薬品開発にプロセスを以下の図で示しています。
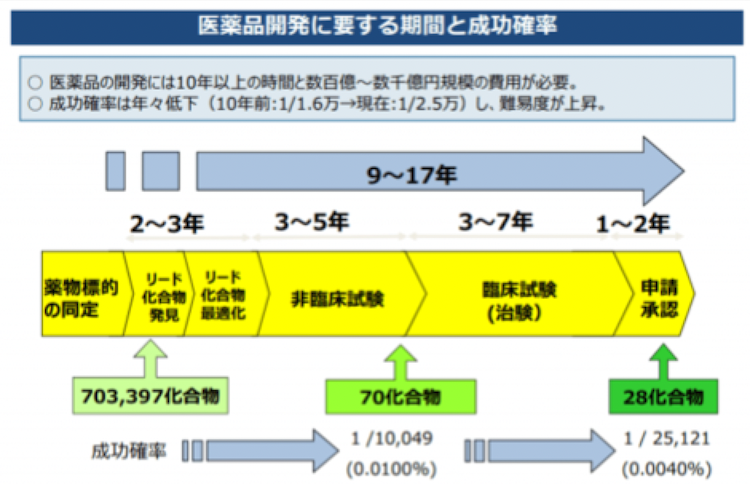
ここで示されているように、医薬品開発には9年から17年の年月が必要です。更に最近は副作用の少ない疾患に選択的な医薬品が求められているため、今まで以上に開発に時間が掛かっています。
リード化合物の探索は時間とコストが軽減されてきていますが、改善されるには「薬物標的の同定」から「リード化合物の最適化」の部分です。ところが、医薬品開発で圧倒的に時間が掛かるのが「非臨床試験」と「臨床試験」の部分で、更に医薬品のDDS化が進むと「非臨床試験」の部分が複雑になり時間も、製剤化のコストも更に掛かると予想されます。
また、上記の図では医薬品の成功確率が10年前と比較して非常に低下していると指摘しています。これは「薬物標的の同定」から「リード化合物の最適化」の部分へのAI技術の活用が少なからず起因していると私は考えています。なぜならば、AI技術を用いたリード化合物の探索と最適化は、疾患の目的プロテインと低分子化合物(リガンド)とのバインデングアッセイが中心になります。私が現役のころ数多く経験したのですが、プロテインと低分子化合物とのバインデングアッセイは、脂溶性の高い化合物ほど活性が高くなる傾向があり、この方法で選んだリード化合物は一般的に体内動態が悪いことが多いのです。私はこのことが医薬品の成功確率が10年前と比較して、非常に低下させているのではないかと考えているのです。
しかし、近年はHT―アドミニストレーションの応用と、再生医療での疾患細胞を用いたアッセイで、これらの問題はかなり改善してきたと思います。更にDDS化の方法を用いることで、脂溶性が高く体内動態が悪いリード化合物でも、DDSに付けることで、DDSが目的の疾患細胞にリード化合物を運んでくれますので、体内動態の悪いリード化合物には、DDS化は非常に有効な手段であると考えています。
それでは、次回は医薬品開発で圧倒的に時間が掛かるのが「非臨床試験」と「臨床試験」の部分の改善策を考えて見ることにします。




