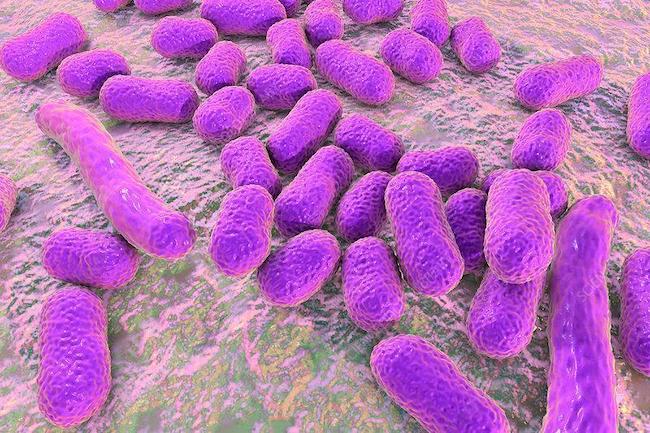
マサチューセッツ工科大学(MIT)とマクマスター大学(カナダ)の研究者は、最新のニュースによれば、人工知能のアルゴリズムを活用して、薬剤耐性感染症の主要な原因となる一種の細菌に対抗できる新たな抗生物質を発見しました。この発見により、肺炎や髄膜炎などの深刻な感染症を引き起こすアシネトバクター・バウマンニ(画像)という細菌に対して有効な治療薬が開発され、将来的に患者の治療に使用される可能性があります。
アシネトバクター・バウマンニは、イラクやアフガニスタンの負傷兵の感染症の主な原因となっており、病院内でも長期間生存し、抗生物質耐性遺伝子を環境から取り込むことができる特性を持っています。この細菌について、マクマスター大学の生化学・医科学助教授であり、かつてMITのポスドクであったJonathan Stokes博士は次のように述べています。「アシネトバクターは、病院のドアノブや器具の表面などで長時間生存でき、環境から抗生物質耐性遺伝子を取り込む能力を持っています。」
研究チームは、約7,000種類の化合物からなる新しい薬剤候補のライブラリを利用し、機械学習モデルを訓練して、これらの化合物がアシネトバクター・バウマンニの増殖を抑制するかどうかを評価しました。その結果、特定の化合物が細菌の増殖を効果的に抑制することが明らかになりました。
「今回の発見は、AIが新規抗生物質の探索を大幅に加速・拡大できるという前提をさらに裏付けるものです。」と、マサチューセッツ工科大学(MIT)の医用工学・科学研究所(IMES)および生物工学科のテルマー教授であるJames Collins博士は語ります。「この研究が、アシネトバクター・バウマンニのような問題のある病原菌に対抗するためにAIを利用できることを示していることに興奮しています。」
Collins博士とStokes博士は、2023年5月25日にNature Chemical Biology誌に掲載されたこの新しい研究の上級著者です。論文の筆頭著者は、マクマスター大学大学院生のGary Liu氏とDenise Catacutan氏、そして最近マクマスターを卒業したKhushi Rathod氏です。この論文のタイトルは、「Deep Learning-Guided Discovery of an Antibiotic Targeting Acinetobacter baumannii(ディープラーニングを用いたAcinetobacter baumanniiを標的とした抗生物質の発見)」と題されています。
ドラッグ・ディスカバリー
過去数十年間において、多くの病原性細菌が既存の抗生物質に対する耐性を強化する一方で、新しい抗生物質の開発はほとんど進んでいません。
数年前、MITのRegina Barzilay教授(この研究の著者でもあります)、James Collins博士、およびJonathan Stokes博士は、この増大する問題に対処するため、パターン認識能力を持つ機械学習という人工知能の一形態を活用することを決意しました。彼らはMITのAbdul Latif Jameel Clinic for Machine Learning in Healthの共同責任者でもあります。Collins博士とBarzilay博士は、この手法を用いて、既存の薬とは異なる化学構造を持つ新しい抗生物質を見つけることができると期待しています。
最初のデモンストレーションでは、機械学習アルゴリズムを用いて、大腸菌の増殖を抑制する化学構造を特定するための訓練を行いました。その結果、1億種類以上の化合物の中から、「ハリシン」と名付けられた分子が発見されました。この分子は、大腸菌だけでなく、治療に耐性を持つ他の数種類の細菌も殺すことができることが判明しました。この名前は、架空の人工知能システムである「2001年宇宙の旅」に由来しています。
「この論文では、複雑な抗生物質の探索において機械学習アプローチが有効であることを示し、その後、私たちは多剤耐性菌感染症の最も深刻な敵であるアシネトバクターに注目しました」と、Stokes博士は述べています。
研究チームは、まず実験皿で培養されたアシネトバクター・バウマンニに約7,500種類の化合物を接触させ、微生物の増殖を抑制できる化合物を調査しました。各分子の構造を計算モデルに入力し、それぞれが細菌の増殖を抑制できるかどうかもモデルに伝えました。これにより、アルゴリズムが増殖抑制に関連する化学的特徴を学習することができました。
学習が完了したモデルを用いて、研究者たちはBroad InstituteのDrug Repurposing Hubから送られてきた6,680種類の化合物セットを分析しました。この分析には約2時間かかり、数百のトップヒットが得られました。そこから、既存の抗生物質やトレーニングデータの分子とは異なる構造を持つ化合物を中心に、実験的にテストする240種類を選びました。
その結果、9種類の抗生物質が見つかり、その中の1種類が非常に強力であることがわかりました。この化合物はもともと糖尿病治療薬の候補として研究されていましたが、アシネトバクター・バウマンニを殺す効果が非常に高いことが明らかになりました。ただし、緑膿菌や黄色ブドウ球菌、カルバペネム耐性腸内細菌科など他の種類の細菌には効果がありませんでした。
このような「狭いスペクトル」での殺菌能力は、細菌が抗生物質に対して急速に耐性を獲得するリスクを最小限に抑えるために望ましい特徴です。また、この抗生物質のおかげで、ヒトの腸内に生息する有益な細菌(例:クロストリジウム・ディフィシル)が保護され、日和見感染症の抑制に貢献する可能性もあります。
「抗生物質を全身的に使用する必要がある場合、重要なことは、重大な細菌異常が発生し、既に病気の患者が二次感染にさらされることを最小限に抑えることがStokes博士の指摘です。狭いスペクトルの抗生物質は、選択的に特定の病原菌を標的とするため、他の有益な細菌や病原菌に対する損傷を最小限に抑えることができます。これは、広範な抗菌活性を持つ広域抗生物質を使用する場合に比べて、治療上の副作用や二次感染のリスクを軽減することができます。
新たなメカニズム
アバウシンという薬剤がアシネトバクター・バウマンニに対して効果的であることがマウスを用いた実験で示され、さらに様々な薬剤耐性を持つアシネトバクター・バウマンニ株にも有効であることが実験室で確認されました。この薬剤は、細胞内部から細胞外皮にタンパク質を輸送するプロセスであるリポタンパク質輸送を阻害することによって細胞を殺すことが明らかにされました。特に、この薬剤はLolEというタンパク質を阻害することが分かっています。
この薬剤がアシネトバクター・バウマンニを選択的に攻撃することは驚きであり、研究チームはアシネトバクター・バウマンニが他のグラム陰性菌とは異なるリポタンパク質輸送を行っている可能性があると考えています。そのため、アバウシンがこの菌に対して特異的な効果を示すのかもしれません。
現在、Stokes博士の研究室は他の研究者と協力して、この化合物の薬効を最適化し、将来的に患者に使用できるように開発を進めています。また、研究チームは同じモデリング手法を使用して、他の種類の薬剤耐性感染症に対する抗生物質の候補を特定する予定です。これにより、AIと機械学習を活用した新たな抗生物質の発見と開発において、より幅広い範囲での応用が期待されます。
この研究は、以下の機関やプログラムから資金提供を受けました:
1. David Braley Center for Antibiotic Discovery
2. Weston Family Foundation
3. Audacious Project
4. C3.ai Digital Transformation Institute
5. Abdul Latif Jameel Clinic for Machine Learning in Health (MIT)
6. DTRA (Defense Threat Reduction Agency) Discovery of Medical Countermeasures Against New and Emerging Threats program
7. DARPA (Defense Advanced Research Projects Agency) Accelerated Molecular Discovery program
8. Canadian Institutes of Health Research
9. Genome Canada
10. McMaster University Faculty of Health Sciences
11. Boris Family
12. Marshall Scholarship
13. Energy Department Biological and Environmental Research program
これらの機関やプログラムの助成によって、研究チームは研究を進めるための資金や支援を受けたことが示されています。
この記事は、MITサイエンスライターのAnne Trafton氏が執筆したMITニュースリリースに基づいています。