「老化に伴うエクソソームによるmiRNA誘導線維化の隣接細胞への移行について(Senescence-Associated Exosome Transfer miRNA-Induced Fibrosis to Neighboring Cells)」と題された新しい研究論文が2023年3月15日、Agingの15巻5号で発表された。「これは、老化関連エクソソームが、隣接する細胞の浸潤特性を活性化する強力な分泌表現型メディエーターとして機能することを示している。」と著者は述べている。
放射線誘発性線維症は、がんの治療法として最も一般的な放射線治療の副作用である。しかし、放射線は、照射組織に存在する正常細胞においても、p53を介した細胞周期停止、p21の発現延長、老化の進展などを引き起こす。骨髄由来の間葉系幹細胞は、炎症組織や線維化組織への自然なトロピズム(向性)を持つため、原発腫瘍部位に蓄積される。
間葉系幹細胞は低線量の電離放射線に対して極めて敏感であり、傍観者的な放射線影響の結果として老化を獲得する。老化した細胞は代謝的に活発であるが、サイトカイン、線維化促進成長因子、エクソソームの過剰分泌に関連する強力な老化に伴う分泌表現型を発達させる。
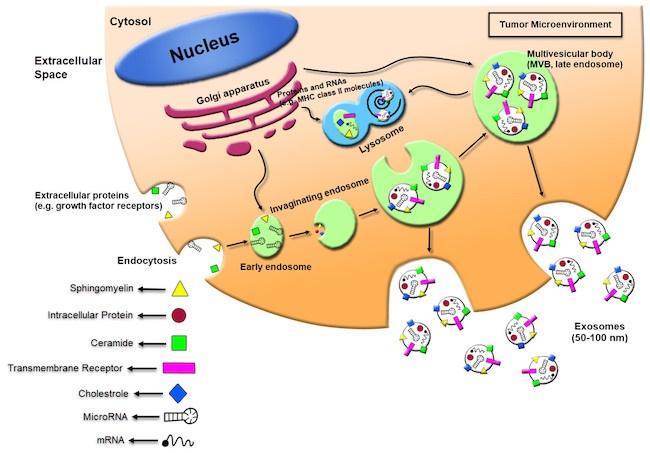
統合パスウェイ解析により、放射線誘発性老化は、間葉系幹細胞の細胞周期、細胞外マトリックス、トランスフォーミング成長因子β(TGF-β)シグナル、小胞媒介輸送遺伝子を有意に強化することが明らかになった。エクソソーム は細胞から分泌されるナノベシクル(細胞外小胞のサブクラス)で、細胞間コミュニケーションに重要なタンパク質、RNA、マイクロRNA(miRNA)などの生体物質を含んでいる。 さらに分泌された エクソソームのmiRNA含有量解析から、放射線による老化がmiRNAプロファイルを特異的に変化させていることがわかった。
「実際、目立ったmiRNAのいくつかは、TGF-βや下流遺伝子を直接標的にしていた。」- 著者
この新しい研究では、放射線による老化の傍観者効果を調べるために、研究者らは、正常間葉系幹細胞を老化関連エクソソームで処理した。
その結果、これらの調節された遺伝子はTGF-β経路に関連し、未処理の間葉系幹細胞と比較して、老化関連エクソソーム処理した間葉系幹細胞ではα平滑筋アクチン(老化・活性化した細胞で増えるタンパク質)およびKi-67(増殖マーカー)の両方の発現が上昇することが判明した。その結果、老化関連エクソソームは、TGF-β経路の活性化を介して筋線維芽細胞の表現型に影響を与える独自のmiRNAコンテンツを有していることが明らかになった。このことから、老化関連エクソソームは、がん関連線維化に大きな役割を果たす強力な分泌表現型因子であることが明らかになった。
「我々のオミックスとエクソソームマイクロアレイの統合解析により、老化した間葉系幹細胞は、差のある転写遺伝子を持ち、固有の転写後カーゴを含むベシクルを分泌することが示された。続いて、これらのエクソソーム miRNAが、疾患進行中の細胞間コミュニケーションにおいて重要な役割を果たし得ることを実証した。」と著者は説明している。
Aging-USについて
2009年に創刊されたAgingは、老化研究およびがんを含む加齢関連疾患の全分野において、一般的な関心と生物学的意義を持つ論文を掲載し、現在は、年齢依存性症候群としてのCOVID-19脆弱性に特に焦点を当てている。Agingのトピックは、従来の老年学にとどまらず、細胞・分子生物学、ヒトの老化関連疾患、モデル生物における病理学、シグナル伝達経路(例:p53、サーチュイン、PI-3K/ACT/mTORなど)、これらのシグナル伝達経路を調節するアプローチなどを含むが、これに限定されない。
[News release] [Aging article]