核酸医薬品はアンチセンスのヴィトラミューンが1998年に承認されて、その後2004年にRNAアプタマーのマキュジェンが承認されましたが、その後ヴィトラミューンが発売中止になり、それ以降核酸医薬はあまり開発が進んできませんでした。このことは、前から話しているように核酸医薬の安定性に問題があったからです。そして、このころから急速に開発が進んだ競合品の抗体医薬の市場導入により、核酸医薬は医薬市場で厳しい状態になり、更に核酸医薬の多くが臨床試験で有効性を証明できませんでした。そこで、siRNAに関してAlnylam社と資本提携をしていたRoche社が核酸医薬から完全撤退し、Novartis社もAlnylam社との提携を終了し、Merck社のsiRNA医薬からmiRNA医薬開発へのシフト、更にPfizer社は核酸医薬開発ユニットの解散など、メガファーマの核酸医薬からの撤退が相次ぎました。
しかし、最近は2013年に世界初の全身投与型のアンチセンス核酸医薬のホモ結合型家族性高コレステロール血症を対象としたmipomersenがアメリカで承認され、2016年にはDDS技術を利用せずに化学修飾により血中安定性を実現した、デュシャンヌ型筋ジストロフィーに対するeteplirsenなどが承認されてきました。更に2018年にAlnylam社より、DDS技術を導入したsiDNA医薬patisiranがアミロイドーシスの核酸原因遺伝子の標的治療薬としてアメリカで承認されました。このように、最近では合成アミノ酸や化学修飾などを用いて核酸医薬品の安定性が高められ、更にDrug Delivery System(DDS)により体内安定性とターゲットへの薬剤の輸送が可能となりました。これからは核酸医薬の分野でDDSが必要不可欠な技術になっていくと考えられます。
それでは、標的細胞へのDDSを用いた核酸輸送はどのように考えたらよいでしょうか。私は3つの方法があると考えています。
まず一つは核酸医薬品が化学的修飾などで安定性が高ければ、核酸医薬品に標的リガンドをつけるAntibody-drug conjugate(ADC)やPeptide-Drug Conjugate(PDC)などを利用する方法と、機能性高分子ポリマーなどの機能性分子を付ける方法が良いと考えられます。
次に核酸医薬品の体内での安定性に問題がある場合は、高分子ミセル・脂質ナノ粒子やエクソソームなどのDDSキャリアで保護して標的細胞に輸送するのが良いと思います。
更に、核酸医薬を標的細胞内のターゲットであるミトコンドリアや細胞核に輸送したい場合は、DDSキャリアで標的細胞に輸送し、更に機能性分子を付けてミトコンドリアや細胞核に送る2段階のDDSを考える必要があるのではないでないでしょうか。
この標的細胞への核酸医薬の送達を図にしたのが以下の図1です。
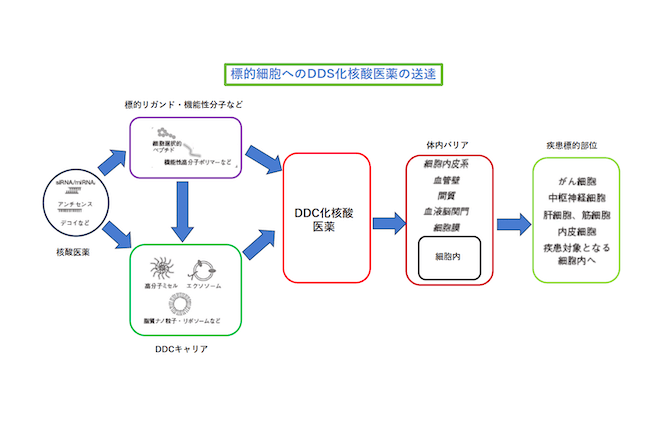
図1の示すように上記の3つの方法で核酸医薬をDDS化することで、体内バリアを通り疾患標的細胞に薬物を送ることが可能になると考えられます。癌、感染症などのように標的細胞に送るだけで効果を発揮する場合は体内バリアだけを考えればよいです。
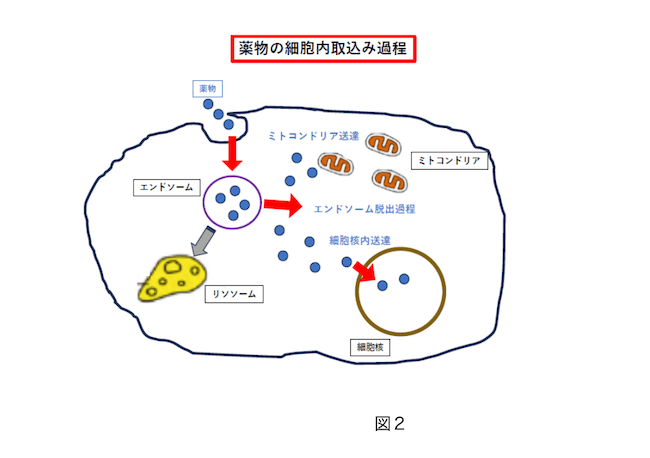
しかし、薬物が細胞内のミトコンドリアや細胞核に作用する場合や、リソソームを利用する場合は、薬物の細胞内への取り込み過程を表した図2のように、エンドソームからどのように放出するかなどの細胞内バリアも考慮に入れる必要があります。
更に、核酸医薬のDDSを考えるにあたって、核酸医薬の安定性、標的リガンド・機能性分子やDDSキャリア多くの場合に化学的修飾が必要で、それを行うには優秀な合成化学者の協力が不可欠と考えられます。
今回は核酸医薬にDDS技術の必要性に関しての私の考えをまとめてみました。そこで、次回は今まで説明していなかった、機能性分子とDDSキャリアについて話すことにします。