今年の夏からいろいろと忙しくて、「創薬よ何処へ」の構想を考える余裕が無くて、半年遅れの投稿になってしまい申し訳ございませんでした。
前回は今後の医薬品開発の方向性として、リード化合物をDDS技術で疾患ターゲットに薬物を送る方法が主流になると話しました。しかし、このような医薬品開発で圧倒的に時間が掛かるのが動物を使った毒性・薬理・安全性試験「非臨床試験」と、人を対象とした「臨床試験」の部分です。特にDDS技術を利用した場合、「非臨床・臨床試験」はリード化合物、DDS化合物とリード化合物・DDSの合剤の3種類の試験を行う必要があり、以前から、医薬品開発で非臨床・臨床試験に時間が掛かることが課題になっていました。更に、非臨床試験から臨床試験に入る際に、動物種間差で開発を断念するケースが多いことも問題になっていました。
このような医薬品開発の状況を改善するために、最近では動物を使わない毒性・安全性試験の開発が進められました。日本では経済産業省が中心になり、毒性関連ビッグデータを用いた化学物質の安全性予測システム(AI-SHIPS)プロジェクトが、東京大学の船津公人教授がプロジェクトリーダとなり、2017年から進められて2022年3月で完成し、現在は利用できる段階に入って、創薬開発の非臨床試験に応用するまで進んでいます。
更に、人のIPS細胞に毒性評価用レポーター遺伝子を導入した毒性・安全性試験の開発も進んでおり、この毒性試験では動物種間差がなく、直接臨床試験に移行することが可能であると考えられます。
このように、AI-SHIPSとIPS細胞を用いることで非臨床・臨床試験が簡略化でき、殆ど動物や人の試験をすることなく治験に持っていくことも可能になってくると考えられます。
リード化合物をDDS技術で疾患ターゲットに薬物を送る創薬開発も、時間がかかりますが、上記の非臨床・臨床試験を用いることで、今後は医薬品開発の効率が上がるのではないかと考えられます。
最後に、経済産業省も次世代創薬システムの開発で以下の図に示すような提案を以前していますが、これにIPS細胞を有効に活用することで、更に、効率の良い医薬品開発が可能になると思います。
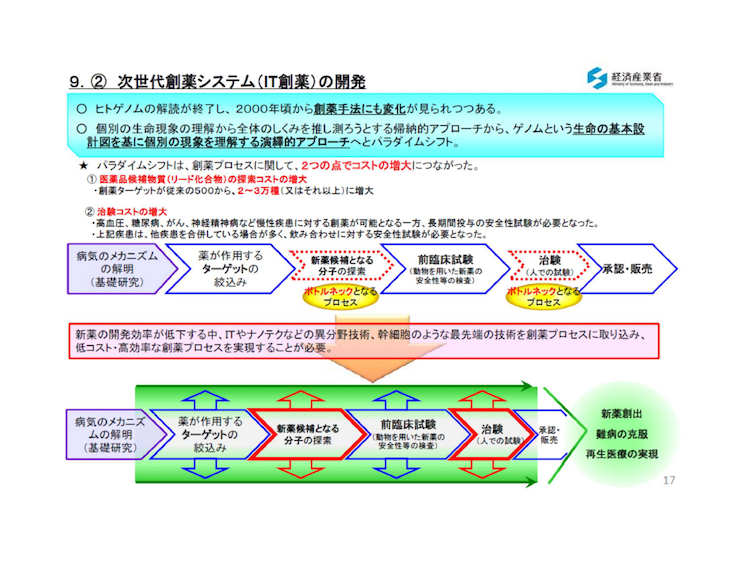
以上で、「創薬よ何処へ」も私としては今回でほぼ完結したように思います。ただ、サイクリックペプタイド創薬など、特許に触れる部分が多い創薬には詳しく触れてきませんでした。その点は申し訳ございませんでした。
これからの創薬の方向については見守っていくことになりますので、定期的な投稿でなく、書く課題が出てきた際に、投稿したいと思います。
それでは、皆さん良いお年をお迎えください。




