こんにちは! 質量分析屋の高橋です。 前回まで、マススペクトルから得られる質量情報について、いくつか解説してきました。今回は、その一環として“窒素ルール”について解説します。窒素ルールとは、C, H, N, O, P, S, ハロゲン元素などから成る一般的な有機化合物において、
・窒素原子を0個または偶数個含むと、化合物のノミナル質量は偶数になる
・窒素原子を奇数個含むと、化合物のノミナル質量は奇数になるという規則のことです。
これは、質量分析のみならず、化学において化合物の分子量や分子質量を計算する時に役立つ規則です。質量分析においては、マススペクトル上に観測されているイオンのm/z値およびそのイオン種から、その分子に窒素原子が含まれているかを判断する際に役立ちます。EIで得られる奇数電子イオンとESIやAPCIで得られる偶数電子イオンでは、質量の扱い方が少し異なりますので、注意が必要です。
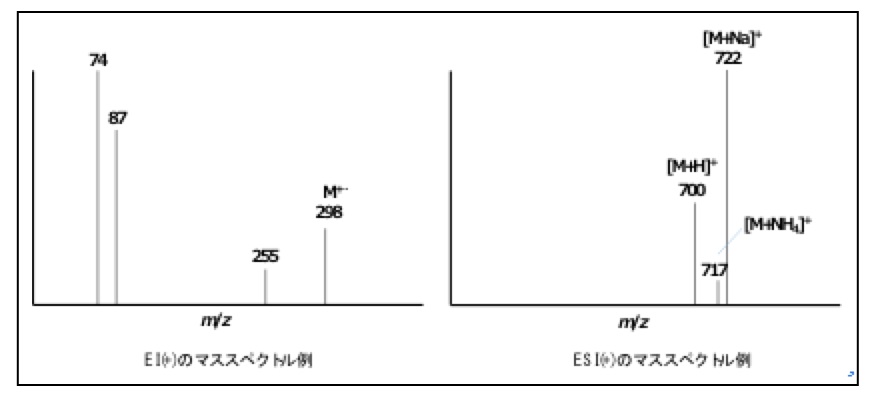
例えば下図(左)の例のように、電子イオン化(EI)で得られたマススペクトルの最も大きなm/z値で観測されている298がM+・である場合、元の分子のノミナル質量も298ですから、窒素原子を0個または偶数個含んでいることになります。
また、下図(右)の正のエレクトロスプレーイオン化(ESI(+))により得られたマススペクトルの例では、m/z 700に観測されているイオンが[M+H]+であることが分かりますので、元の分子のノミナル質量は699となり、窒素原子を奇数個含むことが分かります。 後に、高分解能質量分析計により得られた精密なm/z値からの組成推定について解説しますが、その際にも窒素ルールは役立ちます。



